Задачи урока.
Закрепить умение определять степени окисления атома элемента по химической формуле соединения и научить учащихся составлять формулы соединений по известным степеням окисления атомов элементов.
Оборудование: периодическая система химических элементов Д. И. Менделеева, таблица электроотрицательности химических элементов.
Базовые понятия химическая связь, электроотрицательность, полярность связи, и термины: валентность, степень окисления.
Тип урока: комбинированный
Структура урока
- Организационный этап – 1 - 2 минуты.
- Актуализация опорных знаний – 5 минут
- Изучение нового материала. – 20 минут
- Самые типичные степени окисления некоторых химических элементов.
- Несовпадение величин валентности и степени окисления.
- Составление формул соединений по известным степеням окисления.
- Самостоятельная работа учащихся. – 15 минут
- Домашнее задание – 2 минуты
- Подведение итогов урока – 1 - 2 минуты
Ход урока
Организационный момент
Актуализация опорных знаний учащихся
Беседа.
Что такое степень окисления атома элемента в соединении?
Что такое электроотрицательность?
Что вам известно о переменной валентности химических элементов?
Укажите алгоритм расчета зарядов атомов в бинарных соединениях
Изучение нового материала.

Самостоятельная работа учащихся.
Объяснить механизм образования связи между:
I В стронцием и флуором
II В цезием и оксигеном
Определить степени окисления элементов:
Составить формулы соединений по известным степеням окисления:
I В карбона(+4, +2, - 4) с оксигеном и гидрогеном
II В фосфора(+5, +3, - 3) с оксигеном и гидрогеном
В каких из указанных ниже веществ центральный элемент может проявлять только восстановительные свойства, или только окислительные, или те и другие?
Домашнее задание: изучить параграф. Выполнить упражнения.
Итог урока.

 Получите свидетельство
Получите свидетельство Вход
Вход


 Самые типичные степени окисления хим. элементов
Самые типичные степени окисления хим. элементов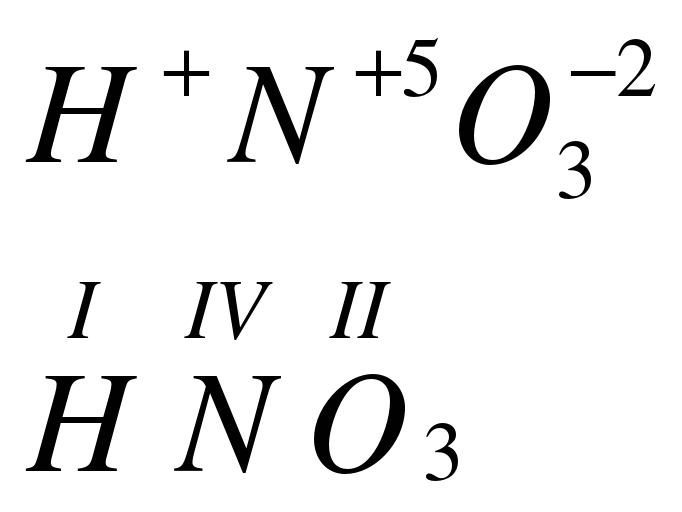 Степень окисления нитрогена=+5
Степень окисления нитрогена=+5 O
O
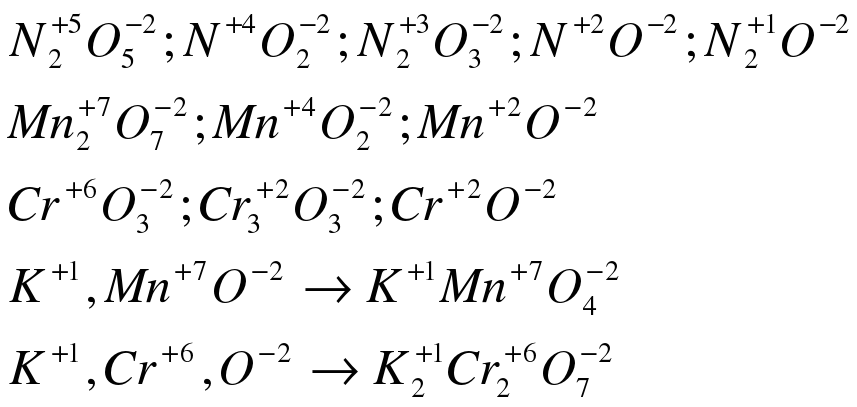









 Урок химии по теме "Степень окисления. Урок №2" (49.5 КB)
Урок химии по теме "Степень окисления. Урок №2" (49.5 КB)
 0
0 1207
1207 126
126 Нравится
0
Нравится
0










