Проект "Такая знакомая сода" был опубликован в журнале "Химия для школьников" (№3, 2011 год; авторы проекта учащиеся 9 класса ГОУ СОШ№1935 г. Москвы- Камнева А., Панюшкина П., Стекольникова Т., руководители: Е.В.Гуменная, заместитель директора по УВР, М.Г.Снастина, учитель химии.) Данная работа мне очень понравилась и я к этому проекту решила создать презентацию.
Задачи проекта:
описать известные методы промышленного получения соды;
исследовать среду водных растворов (рН) карбоната и гидрокарбоната натрия; изменение рН раствора гидрокарбоната натрия после кипячения;
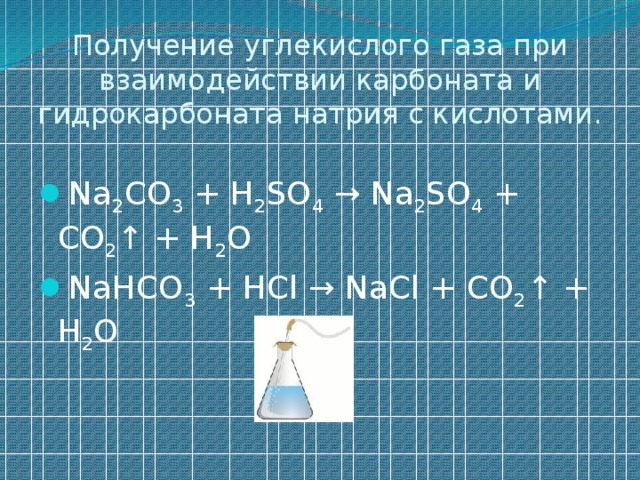
получить углекислый газ и показать его применение для « тушения» горящей свечи;
провести реакции ионного обмена карбоната и гидрокарбоната натрия с некоторыми солями ;
получить мыло из стеариновой кислоты и карбоната натрия;
объяснить результаты проведенных реакций на основе изученного на уроках;
Описать некоторые способы применения карбоната и гидрокарбоната натрия в быту.
Немного истории.
В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
Способ Хоу
Разработан китайским химиком Хоу (Hou Debang) в 1930-х годах. Отличается от процесса Сольве тем, что не использует гидроксид кальция.
Получение стекла.
Стекло — твердотельное состояние аморфных веществ. Термин также используется в названиях оптических материалов, имеющих свойства, характерные для стекла — светопропускание (прозрачность), светопреломление, анизотропность и др. Стеклом называются все аморфные тела, получаемые путем переохлаждения расплава, независимо от их химического состава и температурной области затвердевания, и обладающие в результате постепенного увеличения вязкости механическими свойствами твердых тел, причем процесс перехода из жидкого состояния в стеклообразное должен быть обратимым.
Стекло появилось более 3000 тыс. лет тому назад. Из него было сделано много вещей и будет сделано еще больше. Не смотря на то, что все знаю на бытовом уровне, что такое стекло, нет точного научного определения этого материала.

 Получите свидетельство
Получите свидетельство Вход
Вход












 NaOH + H 2 CO 3 " width="640"
NaOH + H 2 CO 3 " width="640"































 Такая знакомая сода (2.46 MB)
Такая знакомая сода (2.46 MB)
 0
0 1476
1476 136
136 Нравится
0
Нравится
0









