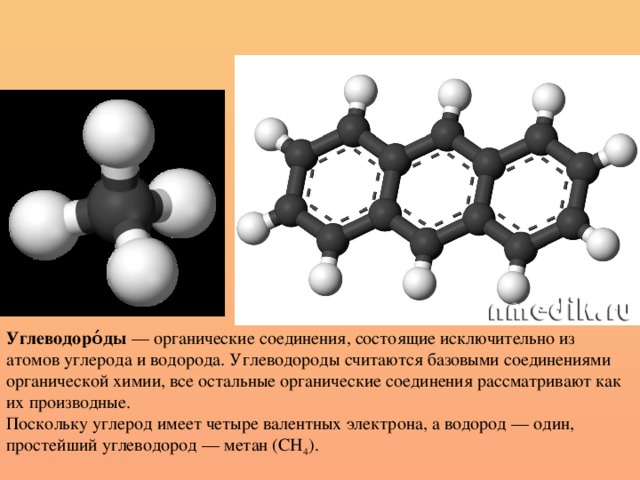
Углеводороды - органические соединения, состоящие исключительно из атомов углерода и водорода.
Углеводороды считаются базовыми соединениями органической химии, все остальные органические соединения рассматривают как их производные.
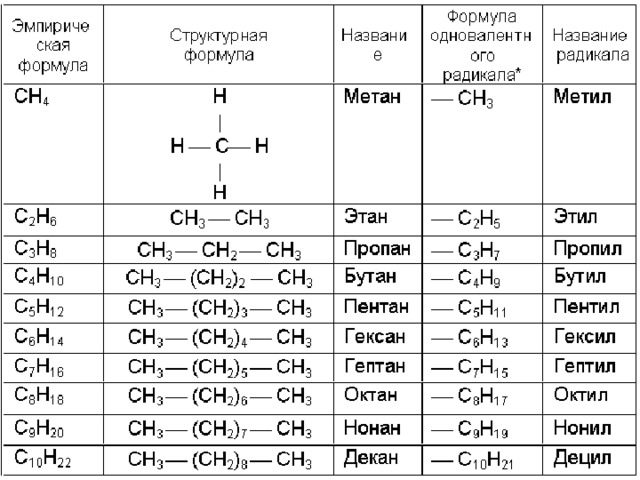
Поскольку углерод имеет четыре валентных электрона, а водород - один, простейший углеводород - метан (CH4).
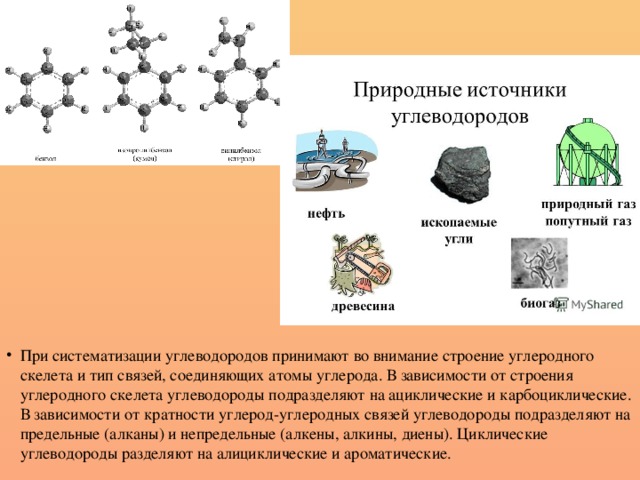
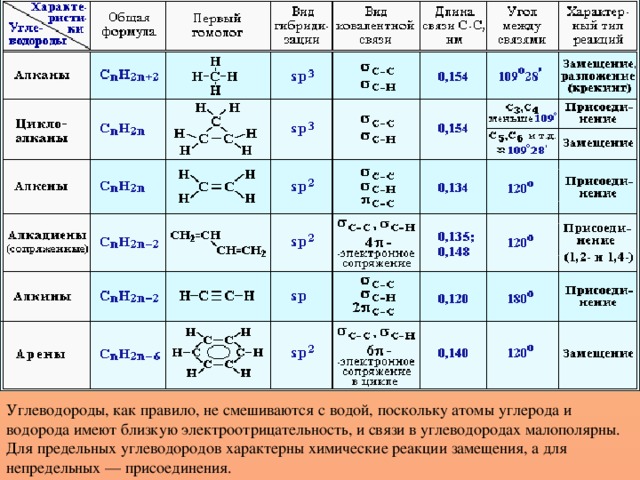
При систематизации углеводородов принимают во внимание строение углеродного скелета и тип связей, соединяющих атомы углерода.

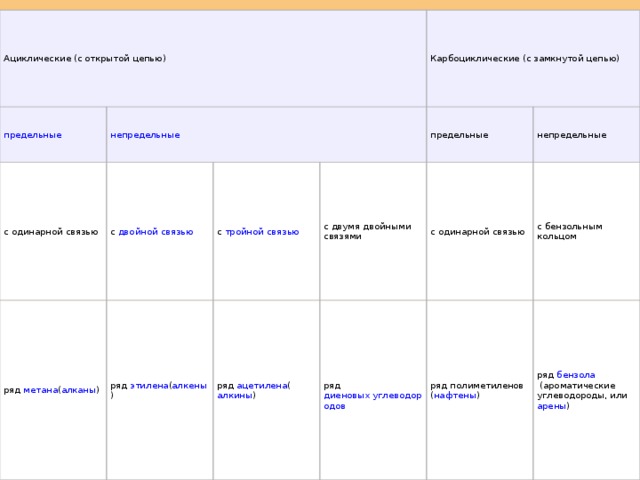
В зависимости от строения углеродного скелета углеводороды подразделяют на ациклические и карбоциклические.
В зависимости от кратности углерод-углеродных связей углеводороды подразделяют на предельные (алканы) и непредельные (алкены, алкины, диены).
Циклические углеводороды разделяют на алициклические и ароматические.
Углеводороды, как правило, не смешиваются с водой, поскольку атомы углерода и водорода имеют близкую электроотрицательность, и связи в углеводородах малополярны. Для предельных углеводородов характерны химические реакции замещения, а для непредельных — присоединения.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Презентация по химии на тему "Углеводороды" (0.54 MB)
Презентация по химии на тему "Углеводороды" (0.54 MB)
 0
0 2559
2559 348
348 Нравится
0
Нравится
0







