
БЕЛКИ метапредметный урок-исследование в 10 классе учитель Дунаева И.И.


Меняя каждый миг свой образ прихотливый,
Капризна, как дитя и призрачна, как дым,
Кипит повсюду жизнь в тревоге суетливой,
Великое смешав с ничтожным и смешным... (Семен Надсон)
«Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, при чём с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка.» (Ф.Энгельс)

Белки
Задачи урока
Изучить:
- состав
- строение белков
- функции
- влияние окружающей среды


- Глицин РНК Рецепторы
- Аланин ДНК Антитела
- Аспирин АЛА Вирусы
- Метиламин
- Этиламин
- Анилин


Наиболее важными
соединениями, которые входят в состав живых организмов, являются
белки (протеины).

Белки – природные полимеры
- Белки образованы всего двадцатью разными аминокислотами, общая формула которых:
R – CHNH 2 – COOH
Внимание! Все аминокислоты белков – это альфа-аминокислоты.
Полимерные цепи белков состоят из десятков тысяч, миллионов и больше остатков аминокислот.
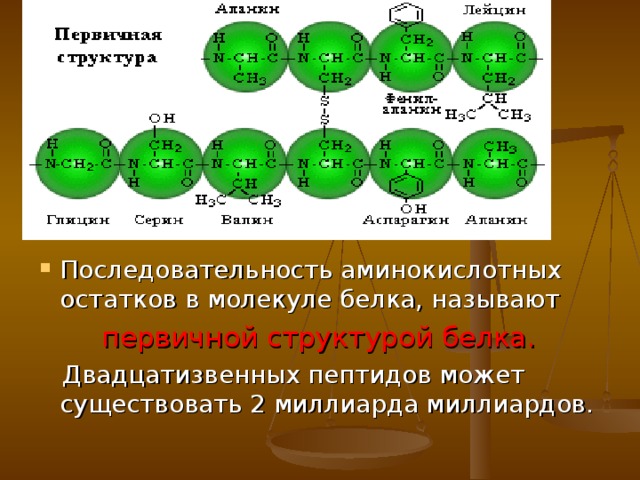
первичной структурой белка.

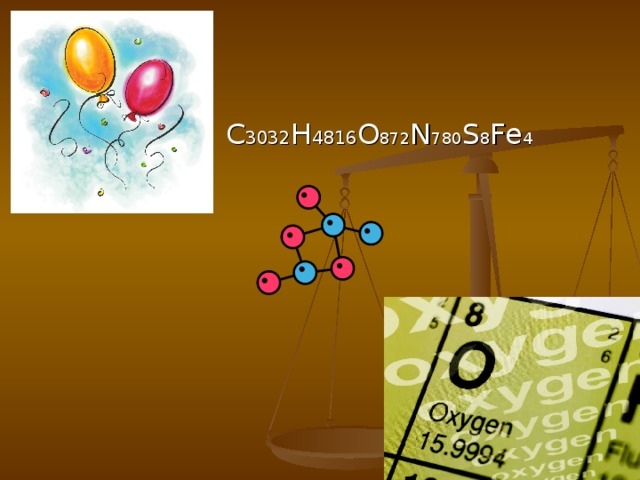
Для белковых тел характерны огромные молекулярные массы.
У вируса желтухи шелковичного червя М r = 916000000
Отсюда и почти макроразмеры некоторых молекул белков.
(при М r = 350000 длина молекул- 0,3 мкм, а при М r = 1000000000 –1мм
Длинная молекула не может быть строго линейной. В результате изгибания и
сворачивания молекулы образуется спиралевидная структура.

- В молекулах белков имеют место ионные взаимодействия между карбоксильными и аминогруппами различных аминокислотных остатков, а также образуются дисульфидные мостики. Эти взаимодействия приводят к появлению третичной структуры.
- Третичная структура миоглобина.
(размер молекулы 4,5 Х
3,5 Х 2,5 нм)

Белки с молекулярной массой больше 50000 состоят из нескольких полипептидных цепей, каждая из которых имеет первичную, вторичную и третичную структуры.
Глобула
(гемоглобин)

Функции белков
- Строительная
- Ферментативная (каталитическая)
- Транспортная
- Защитная
- Двигательная
- Регуляторная
- Запасающая
- Токсическая
- Энергетическая

Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей. Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислотных остатков в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке яиц белок не меняет свой цвет.

Качественные реакции на белки
Биуретовая реакция
- С солями меди ( II ) в присутствии щелочи белки дают фиолетовую окраску. Это качественная реакция на пептидную группу.
Ксантопротеиновая реакция
- При действии азотной кислоты – белки окрашиваются в желтый цвет.

Разрушение структуры белка – денатурация
Какими по вашему могут быть причины денатурации белков?

Причины денатурации белков
- Повышение температуры
- Влияние солей тяжелых металлов
- Влияние алкоголя
- Влияние кислот и щелочей

- Почему жители крупных городов часто имеют проблемы с кожей – дерматиты, полиносы?
- Почему нельзя сушить кожаную обувь, прислонив её непосредственно к батарее?




Ответьте на вопросы
1.В чем причина несовместимости тканей при пересадке органов от одного организма к другому?
2.Научное название белков.
3.Из чего построены молекулы белков?
4.Сколько структур белка существует?
5.Структура белка, свернутая в спираль?
6.Как называется связь - NH – CO - ?
7.Разрушение структуры белка.
8.Реакции, определяющие наличие белка?
9.Пищевые продукты с большим содержанием белка.
10.Самая неустойчивая структура белка?

- Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей. Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание . Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислот в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы . Содержание белка в яйце меньше , чем в молоке и молочных продуктах. При варке белок не меняет свой цвет.

СПАСИБО ЗА ВНИМАНИЕ
Молодцы!


- Белки
- Необходимые, важные
- Регулируют, защищают, запасают
- Белки=жизнь

“ Я всегда говорил и не устаю повторять, что мир бы не мог существовать, если бы был так просто устроен”.


 Получите свидетельство
Получите свидетельство Вход
Вход








































 Презентация к уроку химии на тему "Белки" (1.55 MB)
Презентация к уроку химии на тему "Белки" (1.55 MB)
 0
0 1344
1344 93
93 Нравится
0
Нравится
0






