Согласовано Утверждаю
Зам.директора по УВР Директор
__________ (_) ______________(
«___»_________________2013г. «___»_______________2013г.
РАБОЧАЯ ПРОГРАММА
по __________химии___________________________________
______________ класса МБОУ г.Астрахани «СОШ №36»
Составлена учителем химии
Мальцевой Е.М.
Рассмотрена и согласована на заседании МО
Протокол №_
Председатель МО_______________(_____________)
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
Рабочая программа учебного курса химии для 8 класса (далее – Рабочая программа) составлена на основе Примерной программы основного общего образования по химии и программы курса химии для учащихся 8 классов общеобразовательных учреждений автора О. С. Габриеляна (2010 года).
Программа рассчитана на 102 часа, в том числе на контрольные и практические работы.
Содержание программы направлено на освоение учащимися знаний, умений и навыков на базовом уровне, что соответствует Образовательной программе школы. Она включает все темы, предусмотренные федеральным компонентом государственного образовательного стандарта основного общего образования по химии и авторской программой учебного курса.
Рабочая программа построена на основе концентрического подхода, особенность
которого состоит в вычленении дидактической единицы (в данной программе таковой является «химический элемент») и дальнейшем усложнении и расширении ее (здесь таковыми выступают формы существования (свободные атомы, простые и сложные вещества).
Преобладающей формой текущего контроля выступает письменный (самостоятельные и контрольные работы) и устный опрос (собеседование).
Для реализации Рабочей программы используется учебно-методический комплект,
включающий: учебник (Габриелян О. С.. Химия 8 класс. Учебник для общеобразовательных учреждений – М.: Дрофа, 2013. – 286 с.); Рабочая тетрадь к учебнику О.С.Габриеляна , авт: О.С.Габриелян, С.А.Сладков-М.: «Дрофа», 2013.-207 с.; методическое пособие для учителя (Габриелян О. С.. Программа курса химии для 8-11 классов общеобразовательных учреждений – М.: Дрофа, 2007. – 78 с.)., методическое пособие для учителя: Примерное поурочное тематическое планирование (8класс)(О.С.Габриелян, А.В.Купцова, «Дрофа», 2013.-222 с.)
Цели и задачи изучения предмета
Изучение химии на базовом уровне на ступени основного общего образования в 8 классе направлено на достижение следующих целей:
применение полученных знаний и умений для безопасного использования веществ и материалов в быту, сельском хозяйстве и на производстве, решения практических задач в повседневной жизни, предупреждения явлений, наносящих вред здоровью человека и окружающей среде.
Ведущими идеями предлагаемого курса являются:
Материальное единство веществ природы, их генетическая связь;
Причинно-следственные связи между составом, строением, свойствами и применением веществ;
Познаваемость веществ и закономерностей протекания химических реакций;
Объясняющая и прогнозирующая роль теоретических знаний для фактического материала химии элементов;
Конкретное химическое соединение представляет собой звено в непрерывной цепи превращений веществ, оно участвует в круговороте химических элементов и в химической эволюции;
Законы природы объективны и познаваемы, знание законов дает возможность управлять химическими превращениями веществ, находить экологически безопасные способы производства и охраны окружающей среды о загрязнений.
Наука и практика взаимосвязаны: требования практики – движущая сила науки, успехи практики обусловлены достижениями науки;
Развитие химической науки и химизации народного хозяйства служат интересам человека и общества в целом, имеют гуманистический характер и призваны способствовать решению глобальных проблем современности.
Концепция, заложенная в содержании учебного предмета
Данная программа построена по концентрической концепции.
Отличительные особенности рабочей программы по сравнению с авторской
В инвариантной части Базисного учебного плана на учебный предмет «Химия» в 8 классе выделено 2 часа в неделю. Мы проводим 3 часа в неделю за счёт вариативной части.
Основное содержание курса химии 8 класса составляют сведения о химическом элементе и формах его существования — атомах, изотопах, ионах, простых веществах и важнейших соединениях элемента (оксидах и других бинарных соединениях, кислотах, основаниях и солях), о строении вещества (типологии химических связей и видах кристаллических решеток), некоторых закономерностях протекания реакций и их классификации.
Поурочно-тематический план по объему скорректирован в соответствии с федеральным компонентом государственного образовательного стандарта основного общего образования и требованиями, предъявляемыми к уровню подготовки выпускников основной школы и включает вопросы теоретической и практической подготовки учащихся.
Данная программа содержит все темы, включенные в федеральный компонент содержания образования.
Сроки реализации.
Данная рабочая программа по предмету рассчитана на реализацию в 2013-2014 учебном году.
Формы, методы, технологии обучения
При преподавании курса химии я использую следующие технологии обучения: технологии сотрудничества, разноуровневого обучения, деятельностного подхода, метод проекта, ИКТ, здоровьесберегающие технологии и игровые технологии.
При использовании ИКТ учитываются здоровьесберегающие аспекты урока.
Авторские цифровые образовательные ресурсы: презентации PowerPoint к урокам,
Оборудование:
- компьютеры;
- мультимедийный проектор;
Используемое программное обеспечение:
- ActivBoard.
- Word
- PowerPoint
Для приобретения практических навыков и повышения уровня знаний в рабочую программу включены лабораторные опыты и практические работы, предусмотренные Примерной и авторской программами. Программа О.С. Габриеляна включает все лабораторные работы, предусмотренные Примерной программой.
Значительное место в содержании курса отводится химическому эксперименту. Он открывает возможность формировать у учащихся специальные предметные умения работать с веществами, выполнять простые химические опыты, учит школьников безопасному и экологически грамотному обращению с веществами в быту и на производстве.
Предполагаемые результаты обучения
Программа предусматривает формирование у учащихся общеучебных умений и навыков, универсальных способов деятельности и ключевых компетенций: умение самостоятельно и мотивированно организовывать свою познавательную деятельность; использование элементов причинно-следственного и структурно-функционального анализа; определение сущностных характеристик изучаемого объекта; умение развернуто обосновывать суждения, давать определения, приводить доказательства; оценивание и корректировка своего поведения в окружающем мире.
При выполнении творческих работ формируется умение определять адекватные способы решения учебной задачи на основе заданных алгоритмов, комбинировать известные алгоритмы деятельности в ситуациях, не предполагающих стандартного применения одного из них, мотивированно отказываться от образца деятельности, искать оригинальные решения. Учащиеся должны научиться представлять результаты индивидуальной и групповой познавательной деятельности в форме исследовательского проекта, публичной презентации. Реализация поурочно-тематического плана обеспечивает освоение общеучебных умений и компетенций в рамках информационно-коммуникативной деятельности.
Требования к уровню подготовки обучающихся включают в себя как требования, основанные на усвоении и воспроизведении учебного материала, понимании смысла химических понятий и явлений, так и основанные на более сложных видах деятельности: объяснение физических и химических явлений, приведение примеров практического использования изучаемых химических явлений и законов. Требования направлены на реализацию деятельностного, практико-ориентированного и личностно ориентированного подходов, овладение учащимися способами интеллектуальной и практической деятельности, овладение знаниями и умениями, востребованными в повседневной жизни, позволяющими ориентироваться в окружающем мире, значимыми для сохранения окружающей среды и собственного здоровья.
Формы текущего контроля и промежуточной аттестации
Текущий контроль - позволяет дать оценку результатам повседневной работы. В процессе данного вида контроля устанавливается не только результат предшествующей работы, качество усвоения знаний, умений, навыков, но и готовность учащихся к восприятию нового материала. Текущий контроль как наиболее оперативная и динамичная проверка результатов позволяет выяснить сдвиг в развитии учеников и содействует организации ритмичной работы учащихся. Основная цель данного контроля – анализ хода формирования ЗУН, что дает учителю и ученику возможность своевременно отреагировать на недостатки, выявить их причины, принять необходимые меры к устранению, возвратиться к еще не усвоенным правилам, операциям и действиям.
Устный контроль – предназначен для проверки умения воспроизводить изученное, обосновывать отдельные понятия, законы, явления.
При фронтальной работе опрашивается весь класс. Желающие отвечают на вопросы с места, уточняя, дополняя друг друга.
Индивидуальная форма представляет ответы на серию вопросов. Ученики следят за ответами друг друга, расширяют, углубляют их, дают про себя оценку уровню сформированности знаний
Беседа — форма организации урока, при которой ограниченная дидактическая единица передается в интерактивном информационном режиме для достижения локальных целей воспитания и развития.
Письменный контроль - осуществляется в конкретные отрезки времени. Находясь в жестком лимите времени, ученики должны проявить готовность мобилизовать усилия, знания и умение на безошибочное выполнение работы. Уроки письменного контроля обладают большой мобилизирующей силой, требуя от каждого ученика проявления наибольшей активности в выполнении предложенных заданий, что содействует формированию ответственного отношения к учебе.
Контрольная работа – используется при фронтальном текущем и итоговом контроле с целью проверки знаний, умений школьников по достаточно крупной и полностью изученной теме программы.
Предлагая проверочные контрольные работы, педагогу необходимо учитывать индивидуальные особенности детей. Учащимся предлагаются учебные задания в соответствии с их учебными возможностями, уровнем подготовки. Например, учащиеся могут решить более простую или сложную задачу, если рассчитывать трудность заданий таким образом, чтобы они были ориентированы на зону ближайшего развития учащегося.
Практическая работа, лабораторная работа – используется для формирования практических умений по проведению и описанию опытов, наблюдений, исследований с целью закрепления теоретических знаний
Формами промежуточной аттестации являются задания, нацеленные на проверку трех уровней усвоения.
1 уровень воспроизведения (вопросы репродуктивного характера). Обучаемый может воспроизвести (повторить) информацию, операции, действия, решить типовые задачи, рассмотренные при обучении. Он обладает знанием-копией.
2 уровень умений и навыков (вопросы на установление последовательности, соответствия, задачи на применение ЗУН в стандартной ситуации). На этом уровне усвоения обучаемый умеет выполнять действия, общая методика и последовательность (алгоритм) которых изучены на занятиях, но содержание и условия их выполнения новые.
3 уровень применения ЗУН в нестандартной ситуации, прогнозирования, творчества (проблемные, исследовательские задачи).
- ТРЕБОВАНИЯ К УРОВНЮ ПОДГОТОВКИ УЧАЩИХСЯ
В результате изучения химии ученик должен
знать/понимать
основные формы существования химического элемента (свободные атомы, простые и сложные вещества); основные сведения о строении атомов элементов малых периодов; основные виды химических связей; типы кристаллических решеток; факторы, определяющие скорость химических реакций и состояние химического равновесия; типологию химических реакций по различным признакам; сущность электролитической диссоциации; названия, состав, классификацию и свойства важнейших классов неорганических соединений в свете теории электролитической диссоциации и с позиций окисления-восстановления; важнейшие химические понятия, основные законы химии, основные теории химии, важнейшие вещества и материалы.
Уметь
а) применять следующие понятия: химический элемент, атом, изотопы, ионы, молекулы; простое и сложное вещество; аллотропия; относительная и молекулярная масса, количество вещества, молярная масса, молярный объем, число Авогадро; электроотрицательность, степень окисления, окислительно-восстановительный процесс; химическая связь, ее виды и разновидности; химическая реакция и ее классификации; скорость химической реакции и факторы ее зависимости; обратимость химических реакций, химическое равновесие и условия его смещения; электролитическая диссоциация, гидратация молекул и ионов; ионы, их классификация и свойства; электрохимический ряд напряжений металлов;
б) разъяснять смысл химических формул и уравнений; объяснять действие изученных закономерностей (сохранение массы веществ при химических реакциях); определять степени окисления атомов химических элементов по формулам их соединений; составлять уравнения реакций, определять их вид и характеризовать окислительно-восстановительные реакции, определять по составу (химическим формулам) принадлежность веществ к различным классам соединений и характеризовать их химические свойства, в том числе и в свете теории электролитической диссоциации; устанавливать генетическую связь между классами неорганических соединений и зависимость между составом вещества и его свойствами;
в) обращаться с лабораторным оборудованием; соблюдать правил техники безопасности; проводить простые химические опыты; выполнять химический эксперимент наблюдать за химическими процессами и оформлять результаты наблюдений;
г) производить расчеты по химическим формулам и уравнениям с использованием изученных понятий.
использовать
приобретённые знания и умения в практической деятельности и повседневной жизни.
УЧЕБНО-ТЕМАТИЧЕСКИЙ ПЛАН
| № | Наименование темы/раздела | Всего часов | В том числе |
| Теория | Практика | Контроль |
|
| Введение | 7 | 5 | 1 | 1 |
| 1 | Атомы химических элементов. | 12 | 11 |
| 1 |
| 2 | Простые вещества. | 9 | 8 |
| 1 |
| 3 | Соединения химических элементов | 18 | 15 | 2 | 1 |
| 4 | Изменения, происходящие с веществами. | 18 | 15 | 2 | 1 |
| 5 | Растворение. Растворы. Свойства растворов электролитов. | 28 | 23 | 4 | 1 |
| 6 | Портретная галерея великих химиков (Повторение) | 7 | 6 | 0 | 1 |
| 7 | Учебные экскурсии | 3 | 3 | 0 | 0 |
|
| Итого | 102 | 86 | 9 | 7 |
СОДЕРЖАНИЕ
Введение (7 ч)
Химия — наука о веществах, их свойствах и превращениях.
Понятие о химическом элементе и формах его существования: свободных атомах, простых и сложных веществах.
Превращения веществ. Отличие химических реакций от физических явлений. Роль химии в жизни человека. Хемофилия и хемофобия.
Краткие сведения из истории возникновения и развития химии. Период алхимии. Понятие о философском камне. Химия в XVI в. Развитие химии на Руси. Роль отечественных ученых в становлении химической науки — работы М. В. Ломоносова, А. М. Бутлерова, Д. И. Менделеева.
Химическая символика. Знаки химических элементов и происхождение их названий. Химические формулы. Индексы и коэффициенты. Относительные атомная и молекулярная массы. Расчет массовой доли химического элемента по формуле вещества.
Периодическая система химических элементов Д. И. Менделеева, ее структура: малые и большие периоды, группы и подгруппы (главная и побочная). Периодическая система как справочное пособие для получения сведений о химических элементах.
Расчетные задачи. 1. Нахождение относительной молекулярной массы вещества по его химической формуле. 2. Вычисление массовой доли химического элемента в веществе по его формуле.
Практические работы: Приемы обращения с лабораторным оборудование. Нагревание вещества на открытом пламени.
ТЕМА 1 Атомы химических элементов (12 ч)
Атомы как форма существования химических элементов. Основные сведения о строении атомов. Доказательства сложности строения атомов. Опыты Резерфорда. Планетарная модель строения атома.
Состав атомных ядер: протоны и нейтроны. Относительная атомная масса. Взаимосвязь понятий «протон», «нейтрон», «относительная атомная масса».
Изменение числа протонов в ядре атома — образование новых химических элементов.
Изменение числа нейтронов в ядре атома — образование изотопов. Современное определение понятия «химический элемент». Изотопы как разновидности атомов одного химического элемента.
Электроны. Строение электронных оболочек атомов химических элементов № 1—20 периодической системы Д. И. Менделеева. Понятие о завершенном и незавершенном электронном слое (энергетическом уровне).
Периодическая система химических элементов Д. И. Менделеева и строение атомов: физический смысл порядкового номера элемента, номера группы, номера периода.
Изменение числа электронов на внешнем электронном уровне атома химического элемента — образование положительных и отрицательных ионов. Ионы, образованные атомами металлов и неметаллов. Причины изменения металлических и неметаллических свойств в периодах и группах.
Образование бинарных соединений. Понятие об ионной связи. Схемы образования ионной связи.
Взаимодействие атомов химических элементов-неметаллов между собой — образование двухатомных молекул простых веществ. Ковалентная неполярная химическая связь. Электронные и структурные формулы.
Взаимодействие атомов химических элементов-неметаллов между собой — образование бинарных соединений неметаллов. Электроотрицательность. Понятие о ковалентной полярной связи.
Взаимодействие атомов химических элементов-металлов между собой — образование металлических кристаллов. Понятие о металлической связи.
Демонстрации. Модели атомов химических элементов. Периодическая система химических элементов Д. И. Менделеева.
Практическая работа: 1. Приемы обращения с лабораторным оборудованием. Нагревание вещества на открытом пламени.
ТЕМА 2 Простые вещества (9ч)
Положение металлов и неметаллов в периодической системе химических элементов Д. И. Менделеева. Важнейшие простые вещества — металлы: железо, алюминий, кальций, магний, натрий, калий. Общие физические свойства металлов.
Важнейшие простые вещества — неметаллы, образованные атомами кислорода, водорода, азота, серы, фосфора, углерода. Способность атомов химических элементов к образованию нескольких простых веществ — аллотропия. Аллотропные модификации кислорода, фосфора и олова. Металлические и неметаллические свойства простых веществ. Относительность деления простых веществ на металлы и неметаллы.
Постоянная Авогадро. Количество вещества. Моль. Молярная масса. Молярный объем газообразных веществ. Кратные единицы количества вещества — миллимоль и киломоль, миллимолярная и киломолярная массы вещества, миллимолярный и киломолярный объемы газообразных веществ.
Расчеты с использованием понятий «количество вещества», «молярная масса», «молярный объем газов», «постоянная Авогадро».
Расчетные задачи. 1. Вычисление молярной массы веществ по химическим формулам. 2. Расчеты с использованием понятий «количество вещества», «молярная масса», «молярный объем газов», «постоянная Авогадро».
Демонстрации. Получение озона. Образцы белого и серого олова, белого и красного фосфора. Некоторые металлы и неметаллы количеством вещества 1 моль. Модель молярного объема газообразных веществ.
ТЕМА 3 Соединения химических элементов (18 ч)
Степень окисления. Определение степени окисления элементов по химической формуле соединения. Составление формул бинарных соединений, общий способ их называния.
Бинарные соединения неметаллов: оксиды, хлориды, сульфиды и др. их состав и названия. Составление их формул. Представители оксидов: вода, углекислый газ и негашеная известь. Представители летучих водородных соединений: хлороводород и аммиак.
Основания, их состав и названия. Растворимость оснований в воде. Таблица растворимости гидроксидов и солей в воде. Представители щелочей: гидроксиды натрия, калия и кальция. Понятие о качественных реакциях. Индикаторы. Изменение окраски индикаторов в щелочной среде.
Кислоты, их состав и названия. Классификация кислот. Представители кислот: серная, соляная и азотная. Изменение окраски индикаторов в кислотной среде.
Соли как производные кислот и оснований. Их состав и названия. Растворимость солей в воде. Представители солей: хлорид натрия, карбонат и фосфат кальция.
Аморфные и кристаллические вещества.
Межмолекулярные взаимодействия. Типы кристаллических решеток: ионная, атомная, молекулярная и металлическая. Зависимость свойств веществ от типов кристаллических решеток.
Вещества молекулярного и немолекулярного строения. Закон постоянства состава для веществ молекулярного строения.
Чистые вещества и смеси. Примеры жидких, твердых и газообразных смесей. Свойства чистых веществ и смесей. Их состав. Массовая и объемная доли компонента смеси. Расчеты, связанные с использованием понятия «доля».
Расчетные задачи. 1. Расчет массовой и объемной долей компонентов смеси веществ. 2. Вычисление массовой доли вещества в растворе по известной массе растворенного вещества и массе растворителя. 3. Вычисление массы растворяемого вещества и растворителя, необходимых для приготовления определенной массы раствора с известной массовой долей растворенного вещества.
Демонстрации. Образцы оксидов, кислот, оснований и солей. Модели кристаллических решеток хлорида натрия, алмаза, оксида углерода (IV). Взрыв смеси водорода с воздухом. Способы разделения смесей. Дистилляция воды.
Лабораторные опыты. 1. Знакомство с образцами веществ разных классов. 2. Разделение смесей.
Практические работы: 3. Анализ почвы и воды. 5. Приготовление раствора сахара и расчет его массовой доли в растворе
ТЕМА 4. Изменения, происходящие с веществами (18 ч)
Понятие явлений как изменений, происходящих с веществами.
Явления, связанные с изменением кристаллического строения вещества при постоянном его составе, — физические явления. Физические явления в химии: дистилляция, кристаллизация, выпаривание и возгонка веществ, центрифугирование.
Явления, связанные с изменением состава вещества, — химические реакции. Признаки и условия протекания химических реакций. Понятие об экзо- и эндотермических реакциях. Реакции горения как частный случай экзотермических реакций, протекающих с выделением света.
Закон сохранения массы веществ. Химические уравнения. Значение индексов и коэффициентов. Составление уравнений химических реакций.
Расчеты по химическим уравнениям. Решение задач на нахождение количества вещества, массы или объема продукта реакции по количеству вещества, массе или объему исходного вещества. Расчеты с использованием понятия «доля», когда исходное вещество дано в виде раствора с заданной массовой долей растворенного вещества или содержит определенную долю примесей.
Реакции разложения. Понятие о скорости химических реакций. Катализаторы. Ферменты.
Реакции соединения. Каталитические и некаталитические реакции. Обратимые и необратимые реакции.
Реакции замещения. Электрохимический ряд напряжений металлов, его использование для прогнозирования возможности протекания реакций между металлами и растворами кислот. Реакции вытеснения одних металлов из растворов их солей другими металлами.
Реакции обмена. Реакции нейтрализации. Условия протекания реакций обмена в растворах до конца.
Типы химических реакций (по признаку «число и состав исходных веществ и продуктов реакции») на примере свойств воды. Реакция разложения — электролиз воды. Реакции соединения — взаимодействие воды с оксидами металлов и неметаллов. Понятие «гидроксиды». Реакции замещения — взаимодействие воды с щелочными и щелочноземельными металлами. Реакции обмена (на примере гидролиза сульфида алюминия и карбида кальция).
Расчетные задачи. 1. Вычисление по химическим уравнениям массы или количества вещества по известной массе или количеству вещества одного из вступающих в реакцию веществ или продуктов реакции. 2. Вычисление массы (количества вещества, объема) продукта реакции, если известна масса исходного вещества, содержащего определенную долю примесей. 3. Вычисление массы (количества вещества, объема) продукта реакции, если известна масса раствора и массовая доля растворенного вещества.
Демонстрации. Примеры физических явлений: а) плавление парафина; б) возгонка иода или бензойной кислоты; в) растворение перманганата калия; г) диффузия душистых веществ с горящей лампочки накаливания. Примеры химических явлений: а) горение магния, фосфора; б) взаимодействие соляной кислоты с мрамором или мелом; в) получение гидроксида меди (II); г) растворение полученного гидроксида в кислотах; д) взаимодействие оксида меди (II) с серной кислотой при нагревании; е) разложение перманганата калия; ж) взаимодействие разбавленных кислот с металлами; з) разложение пероксида водорода; и) электролиз воды.
Лабораторные опыты. 1. Сравнение скорости испарения воды и спирта по исчезновению их капель на фильтровальной бумаге. 2. Окисление меди в пламени спиртовки или горелки. 3. Помутнение известковой воды от выдыхаемого углекислого газа. 4. Получение углекислого газа взаимодействием соды и кислоты. 5. Замещение меди в растворе хлорида меди (II) железом.
Практические работы: 2. Наблюдение за горящей свечой. 4. Признаки химических реакций
ТЕМА 5 Растворение. Растворы. Свойства растворов электролитов (28 ч)
Растворение как физико-химический процесс. Понятие о гидратах и кристаллогидратах. Растворимость. Кривые растворимости как модель зависимости растворимости твердых веществ от температуры. Насыщенные, ненасыщенные и пересыщенные растворы. Значение растворов для природы и сельского хозяйства.
Понятие об электролитической диссоциации. Электролиты и неэлектролиты. Механизм диссоциации электролитов с различным типом химической связи. Степень электролитической диссоциации. Сильные и слабые электролиты.
Основные положения теории электролитической диссоциации. Ионные уравнения реакций. Условия протекания реакции обмена между электролитами до конца в свете ионных представлений.
Классификация ионов и их свойства.
Кислоты, их классификация. Диссоциация кислот и их свойства в свете теории электролитической диссоциации. Молекулярные и ионные уравнения реакций кислот. Взаимодействие кислот с металлами. Электрохимический ряд напряжений металлов. Взаимодействие кислот с оксидами металлов. Взаимодействие кислот с основаниями — реакция нейтрализации. Взаимодействие кислот с солями. Использование таблицы растворимости для характеристики химических свойств кислот.
Основания, их классификация. Диссоциация оснований и их свойства в свете теории электролитической диссоциации. Взаимодействие оснований с кислотами, кислотными оксидами и солями. Использование таблицы растворимости для характеристики химических свойств оснований. Разложение нерастворимых оснований при нагревании.
Соли, их классификация и диссоциация различных типов солей. Свойства солей в свете теории электролитической диссоциации. Взаимодействие солей с металлами, условия протекания этих реакций. Взаимодействие солей с кислотами, основаниями и солями. Использование таблицы растворимости для характеристики химических свойств солей.
Обобщение сведений об оксидах, их классификации и химических свойствах.
Генетические ряды металлов и неметаллов. Генетическая связь между классами неорганических веществ.
Окислительно-восстановительные реакции. Окислитель и восстановитель, окисление и восстановление.
Реакции ионного обмена и окислительно-восстановительные реакции. Составление уравнений окислительно-восстановительных реакций методом электронного баланса.
Свойства простых веществ — металлов и неметаллов, кислот и солей в свете представлений об окислительно-восстановительных процессах.
Демонстрации. Испытание веществ и их растворов на электропроводность. Движение окрашенных ионов в электрическом поле. Зависимость электропроводности уксусной кислоты от концентрации. Взаимодействие цинка с серой, соляной кислотой, хлоридом меди (II). Горение магния. Взаимодействие хлорной и сероводородной воды.
Лабораторные опыты. 1. Реакции, характерные для растворов кислот (соляной или серной). 2. Реакции, характерные для растворов щелочей (гидроксидов натрия или калия). 3. Получение и свойства нерастворимого основания, например гидроксида меди (II). 4. Реакции, характерные для растворов солей (например, для хлорида меди (II). 5. Реакции, характерные для основных оксидов (например, для оксида кальция). 6. Реакции, характерные для кислотных оксидов (например, для углекислого газа).
Практические работы: 6. Ионные реакции. 7. Условия протекания химических реакций между ратворами электролитов до конца. 8. Свойства кислот, оснований, оксидов и солей. 9. Решение экспериментальных задач.
.
ТЕМА 6 Портретная галерея великих химиков (6 часов)
Повторение материала 8 класса
ТЕМА 7 Учебные экскурсии (3 часа)
ПРАКТИЧЕСКАЯ ЧАСТЬ ПРОГРАММЫ
В 8 классе проводится 9 практических работ согласно инструктивным карточкам, изложенным в учебнике: Габриелян О. С.. Химия 8 класс. Учебник для общеобразовательных учреждений – М.: Дрофа, 2013. – 286 с.
Для выполнения домашних заданий используется: ГабриелянО.С.. Химия.8: Рабочая тетрадь к учебнику О.С. Габриеляна «Химия.8». – М.: Дрофа, 2013. – 207с.
УЧЕБНО-МЕТОДИЧЕСКИЕ СРЕДСТВА
Реализация программы обеспечивается учебными и методическими пособиями
Используемый учебник: Габриелян О.С. Химия 8 класс. Учебник для общеобразовательных учреждений. – М.: Дрофа, 2013. – 286с. (имеется в федеральном перечне учебников, рекомендованных Министерством образования Российской Федерации к использованию в образовательном процессе в общеобразовательных учреждениях на 2013/2014 учебный год)
Для учащихся:
ГабриелянО.С.. Химия.8: Рабочая тетрадь к учебнику О.С. Габриеляна «Химия.8». – М.: Дрофа, 2013
Для учителя:
Рябов М.А. Тесты по химии: 8 класс: к учебнику О.С. Габриелян «Химия.8». – М.: изд-во «Экзамен», 2009
Горковенко М.Ю. Химия. 8 класс. Поурочные разработки к учебникам химии. – М.: ВАКО, 2009.
MULTIMEDIA – поддержка курса:
www.him.1september.ru
www.edios.ru
www.km.ru/educftion
Химия. 8-11 класс. Виртуальная лаборатория. – Мультимедиа, МарГТУ, 2002
Химия.8 (3 диска). – Просвещение, 2002
Демонстрационное поурочное планирование «Неорганическая химия». Изд. «Учитель»-2009г
Дидактический и раздаточный материал Химия 8-9 класс. Изд. «Учитель»-2009г
Мультимедийное учебное пособие нового образца «Химичя-8класс». Изд.»Просвещение»-2009г.
Электронные уроки и тесты. «Химия в школе»- 5 дисков. Изд. «Просвещение-МЕДИА», 2005г
«Химия»-8 класс.-1С: школа, 2005
Тесты «Химия 8-11 класс Изд. «Учитель» 2008 г
Химия Интерактивные творческие задания (8-9), Изд.ООО «Уральский элктронный завод» , 2004
Приложение
Характеристика цифровой отметки и словесной оценки.
Итоговая отметка не может быть простым среднеарифметическим данным по текущей проверке. Следует не допускать тенденции формального «накопления» отметок, ориентировки на «среднюю» отметку, выведенную путем арифметических подсчетов. Она выставляется с учетом фактического уровня подготовки, достигнутого учеником к концу определенного периода. При этом ученик имеет право исправить плохую отметку, получить более высокие баллы и повысить свою успеваемость.
С учетом современных требований к оценочной деятельности в школе вводится четырехбальная система цифровых оценок (отметок). Отменяется оценка «очень плохо» (отметка «1»).
Нормы оценок (итоговые и текущие) по предметам соответствует общим требованиям.
Критерии оценки ЗУН учащихся
Балл «5» ставится, когда ученик обнаруживает усвоение обязательного уровня и уровня повышенной сложности учебной программы; выделяет главные положения в изученном материале и не затрудняется при ответах на видоизмененные вопросы; свободно применяет полученные знания на практике; не допускает ошибок в воспроизведении изученного материала, а также в письменных работах, выполняет их уверенно и аккуратно.
Балл «4» ставится, когда ученик обнаруживает усвоение обязательно и частично повышенного уровня сложности учебной программы; отвечает без особых затруднений на вопросы учителя; умеет применять полученные знания на практике; в устных ответах не допускает серьезных ошибок, легко устраняет отдельные неточности с помощью дополнительных вопросов учителя, в письменных работах делает незначительные ошибки.
Знания, оцениваемые «5» и «4» баллами, как правило, характеризуются высоким понятийным уровнем, глубоким усвоением фактов и вытекающих из них обобщений.
Оценка «3» ставится, когда ученик обнаруживает усвоение обязательного уровня учебной программы, но испытывает затруднения при его самостоятельном воспроизведении и требует дополнительных уточняющих вопросов учителя; предпочитает отвечать на вопросы воспроизводящего характера и испытывает затруднение при ответах на видоизмененные вопросы; допускает ошибки в письменных работах. Знания, оцениваемые баллом «3», зачастую, находятся на уровне представлений, сочетающихся с элементами научных понятий.
Балл «2» ставится, когда у ученика имеются отдельные представления об изученном материале, но все же большая часть обязательного уровня учебной программы не усвоена, в письменных работах ученик допускает грубые ошибки.
СРЕДСТВА КОНТРОЛЯ
Запланировано проведение 7 письменных контрольных работ.
Контрольная работа №1
по теме: Атомы химических элементов.
I вариант
Распределить по четырём столбикам в зависимости от вида химической связи:
NaBr, Ti, Br2,MgCl2, SiO2, N2, Li2S, Ca, Fe, H2S
Написать схему образования веществ, формулы которых подчёркнуты в первом задании.
Дать характеристику элемента № 17 согласно положению в Периодической системе Д.И.Менделеева и строению атома.
Что такое электроотрицательность? Атомы каких элементов проявляют это свойство? Привести примеры.
Определите относительную молекулярную массу (Мr) вещества, имеющего формулу HNO3.
II вариант
Распределить по четырём столбикам в зависимости от вида химической связи:
BaBr2, Hg, Cl2, CH4, KJ, O3, F2, Na2O, Mg, SO3
Написать схему образования веществ, формулы которых подчёркнуты в первом задании.
Дать характеристику элемента № 19 согласно положению в Периодической системе Д.И.Менделеева и строению атома.
Какой вид химической связи называется металлической? Какие свойства имеют вещества с металлической связью? Почему?
Определите относительную молекулярную массу (Мr) вещества, имеющего формулу КNO3.
Контрольная работа №2
по теме: Соединения химических элементов.
I вариант
Из перечня формул выпишите отдельно формулы оксидов, оснований, солей и кислот. Дайте им названия. Укажите степень окисления каждого элемента.
NaOH, Cu2O, FeCl3, HNO3
2. Задача.
В 300г воды растворили 150 г серной кислоты. Найдите массовую долю
кислоты в полученном растворе.
3. Задача.
Слили два раствора соляной кислоты: 120г 15%-го и 200г 5%-го.
Рассчитайте массовую долю кислоты в полученном растворе.
II вариант
Из перечня формул выпишите отдельно формулы оксидов, оснований, солей и кислот. Дайте им названия. Укажите степень окисления каждого элемента.
LiOH, CaO, AlCl3, H2SO4
Задача.
В 40 г воды растворили 15г соли. Найдите массовую долю соли в полученном
растворе.
Задача.
Слили два раствора фосфорной кислоты: 350г 20%-го и 100г 10%-го.
Рассчитайте массовую долю кислоты в полученном растворе.
Контрольная работа №3 по теме: «Изменения, происходящие с веществами»
K. (8) -3. 1
Задание 1
▲ Расставьте коэффициенты в схемах реакций, укажите их тип:
а) Cu + O2 → CuO; б) CaCO3 → CaO + CO2;
в) Zn + HCL → ZnCL2 + H2; г) CuO + HCL → CuCL2 + H2O.
▄ Даны схемы реакций: а) гидроксид железа (III) → оксид железа (III) + вода;
б) нитрат бария + сульфат железа (III) → сульфат бария + нитрат железа (III);
в) алюминий + серная кислота → сульфат алюминия + водород;
г) оксид фосфора (V) + вода → фосфорная кислота.
Запишите уравнения реакций, укажите типы химических реакций.
● Даны схемы реакций: а) гидроксид алюминия → оксид алюминия + вода;
б) нитрат бария + сульфат натрия → …;
в) соляная кислота + алюминий → …;
г) оксид серы (VI) + вода → …
Запишите уравнения реакций, укажите типы химических реакций.
Задание 2. Решить задачу:
▲ Рассчитайте объём водорода (н.у.), полученного при взаимодействии цинка массой 13 г с избытком соляной кислоты. Уравнение химической реакции: Zn + 2HCL = ZnCL2 + H2
▄ Технический цинк массой 7 г, содержащий 7 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
● Технический цинк массой 650 мг, содержащий 20 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
Задание 3
Запишите уравнения реакций переходов:
S → SO2 → H2SO3
К.(8) – 3.2.
Задание1
▲ Расставьте коэффициенты в приведённых ниже схемах химических реакций, укажите их типы: а) Cu(OH)2 → CuO + H2O; б) HCL + Na2O → NaCl + H2O;
в) KBr + CL2 → KCL + Br2; г) Zn + O2 → ZnO.
▄ Даны схемы реакций: а) гидроксид меди (II) → оксид меди (II) + вода;
б) хлорид бария + сульфат натрия → сульфат бария + хлорид натрия;
в) серная кислота + магний → сульфат магния + водород;
г) оксид углерода (IV) + вода → угольная кислота.
Запишите уравнения реакций, укажите типы химических реакций.
● Даны схемы реакций: а) гидроксид цинка → оксид цинка + вода;
б) нитрат бария + сульфат калия → …;
в) соляная кислота + магния → …
г) оксид азота (V) + вода →…
Запишите уравнения реакций, укажите типы химических реакций.
Задание 2. Решить задачу:
▲ Рассчитайте объём водорода (н.у.), полученного при взаимодействии магния массой
12 г с избытком соляной кислоты. Уравнение химической реакции:
Mg + 2HCL = MgCL2 + H2
▄ Технический магний массой 40 г, содержащий 10 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
● Технический цинк массой 240 мг, содержащий 10 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
Задание3. Запишите уравнения реакций переходов: P → P2O5 → H3PO4
К.8 (3) – 3.
Задание1
▲ Расставьте коэффициенты в приведённых ниже схемах химических реакций, укажите их типы: а) H2О → O2 + H2; б) КОН + Н3 РO4 → К3РО4+ H2O;
в) Fe + CL2 → FeCL3; г) Zn O + H2 → Zn + H2O.
▄ Даны схемы реакций: а) карбонат кальция → оксид углерода (IV) + оксид кальция;
б) сульфат меди (II) + гидроксид натрия → гидроксид меди (II) + сульфат натрия;
в) соляная кислота + цинк → хлорид цинка + водород;
г) оксид серы (VI) + вода → серная кислота.
Запишите уравнения реакций, укажите типы химических реакций.
● Даны схемы реакций: а) карбонат магния → оксид магния + углекислый газ;
б) оксид кальция + вода → …;
в) серная кислота + цинк →…;
г) гидроксид натрия + фосфорная кислота → …
Задание 2. Решить задачу:
▲ Рассчитайте объём водорода (н.у.), полученного при взаимодействии железа массой
112 г с избытком соляной кислоты. Уравнение химической реакции:
Fe + 2HCL = FeCL2 + H2
▄ Техническое железо массой 21 г, содержащее 20 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
● Техническое железо массой 560 мг, содержащее 10 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
Задание 3. Запишите уравнения реакций переходов:
Li → Li2O → LiOH.
К.(8)-3. 4.
Задание 1.
▲ Расставьте коэффициенты в приведённых ниже схемах химических реакций, укажите
их типы: а) BaCL2 + AgNO3 → AgCl + Ba(NO3)2; б) Al(OH)3 → AL2O3 + H2O;
в) H2 + CL2 → HCL; г) Fe + CuSO4 → FeSO4 + Cu.
▄ Даны схемы реакций: а) гидроксид железа (II) → оксид железа (II) + вода;
б) хлорид цинка + нитрат серебра → хлорид серебра + нитрат цинка;
в) сульфат меди (II) + железо → сульфат железа (II) + медь;
г) оксид лития + вода → гидроксид лития.
Запишите уравнения реакций, укажите типы химических реакций.
● Даны схемы реакций: а) гидроксид железа (II) → оксид железа (II) + вода;
б) гидроксид натрия + азотная кислота → …;
в) оксид серы (IV) + вода → …;
г) нитрат ртути (II) + медь →….
Запишите уравнения реакций, укажите типы химических реакций.
Задание2. Решить задачу:
▲ Рассчитайте объём водорода (н.у.), полученного при взаимодействии алюминия массой
5,4 г с избытком соляной кислоты. Уравнение химической реакции:
2 AL+ 6HCL = 2 ALCL3 + 3 H2
▄ Алюминий массой 13,5 г, содержащий 20 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
● Алюминий массой 270 мг, содержащий 10 % примесей, растворили в избытке соляной кислоты. Рассчитайте объём выделившегося водорода (н.у.).
Задание 3. Запишите уравнения реакций переходов:
Ca → CaO → Ca(OH)2
Контрольная работа № 4 по теме:
«Электролиты. Электролитическая диссоциация».
( 8 класс)
▲ 1.Составьте формулы указанных веществ:
1 вариант 2 вариант
хлорид алюминия, оксид магния, гидроксид натрия, хлорид железа (II),
кислород, серная кислота, нитрат железа(III), оксид азота (IV), азотная кислота,
оксид углерода (II), гидроксид калия; сульфат алюминия, оксид натрия, цинк.
Составьте уравнения электролитической диссоциации сильных электролитов.
▲ 2. Допишите уравнения реакций в молекулярном виде, составьте уравнения в ионном в
виде:
1 вариант 2 вариант
а) MgCL2 + NaOH → a) NaOH + H2SO4 →
б) K2CO3 + HNO3→ б) ZnSO4 + KOH →
в) Ba(OH)2 + HCL → в) Na2CO3 + HCL →
▄ 3. Растворы каких электролитов можно взять для получения указанных веществ?
1 вариант 2 вариант
а) MgCO3; а) Н2О;
б) Н2О. б) Cu(OH)2.
Напишите уравнения реакций в молекулярном и ионном видах.
▄ 4. Напишите молекулярные уравнения, соответствующие данным сокращенным
ионным уравнениям.
1 вариант 2 вариант
а) Zn2++ 2 OH- → Zn(OH)2↓; a) CO32- + 2 H +→ CO2↑+ H2O;
б) 2 Н++ S2-→ H2S↑. б) Ba 2+ + SO4 2-→BaSO4↓.
● 5. Какие из ионов не могут одновременно находиться в растворе? Почему? Ответ подтвердите уравнениями реакций в ионном виде.
1 вариант 2 вариант
Ba 2+, H+, CL-, OH-, SO4 2-. H+, CL-, OH-, Mg 2+, NO3-.
На отметку «5» необходимо выполнить 1,2, 3 (или 4) и 5-е задания;
на отметку «4» необходимо выполнить 1, 2 и 3-е (или 4-е) задания;
на отметку «3» необходимо выполнить 1-е и 2-е задания.
Также запланированы уроки обобщения и контроля знаний, на которых учащимся предлагается выполнять задания подобного типа:
Обобщение и систематизация знаний по теме «Простые вещества»
I вариант
1. Сколько молекул содержат:
а) 4 моль вещества
б) 2 кмоль вещества
в) 3 ммоль вещества?
2. Сколько молекул содержится в 32г кислорода (О2) ?
3. Найдите массу 30 ∙ 1023 молекул кислорода (О2) .
4. Какая масса 4 моль воды (Н2О)?
5. Сколько моль составляют 40 г гидроксида натрия (NaOH)?
6. Найдите массу 44,8 л кислорода (О2)
7. Какой объём при нормальных условиях займут:
а) 3 моль водорода (Н2)
б) 3 г водорода (Н2) ?
На «3» - любые две задачи
На «4» - любые пять задач
На «5» - все задачи
Разрешается пользоваться справочником формул
II вариант
1. Сколько молекул содержат:
а) 3 моль вещества
б) 6 кмоль вещества
в) 1 ммоль вещества?
2. Сколько молекул содержится в 64г кислорода (О2) ?
3. Найдите массу 12 ∙ 1023 молекул водорода (Н2) .
4. Какая масса 4 моль оксида азота (NО)?
5. Сколько моль составляют 80 г гидроксида натрия (NaOH)?
6. Найдите массу 22,4 л кислорода (О2)
7. Какой объём при нормальных условиях займут:
а) 3 моль кислорода (О2) ?
б) 3 г кислорода (О2) ?
На «3» - любые две задачи
На «4» - любые пять задач
На «5» - все задачи
Разрешается пользоваться справочником формул
Тестовая проверка знаний:
Тест по химии «Основные химические понятия»
1. Относительная молекулярная масса воды
А) 18 В) 46 С) 2 Д) 21
2. Относительная масса кислорода
А)16 В)2 5 С) 34 Д) 24
3.Относительная масса азотной кислоты
А) 234 В) 98 С)63 Д) 56
4. Реакция, протекающая между двумя сложными веществами, где их атомы меняются местами называют
А) синтез В) анализ С) обмен Д) замещение
5. Вещества, состоящие из атомов ме и гидроксогруппы ОН называют
А) простыми В) основаниями С) солями Д) изотопами
6. Вещества, состоящие из разных видов атомов называют
А) сложными В) простыми С) изомерами Д) гомологами
7. Формулы оксидов находятся в ряду
А)H2CO3, H3PO4 MgSO4 В) CuO, HNO3 ,CaCO3
С) H2S, H3BO3, H2SiO3 Д) H2O, Fe2O3, MgO
8. Вещества, состоящие из атомов водорода и кислотных остатков называют
А) кислоты В) соли С) основания Д) оксиды
9. Выберите формулы оснований ряду
А) MgO, SO3 С) Ca(OH)2, Al(ОН)3
В) H2S, CaSO3 Д) F2O, HF
10. Автор закона «Один моль любого газа при н.у. занимает объем 22,4 литра»
А) Менделеев В) Лавуазье
С) Авогадро Д) Бекетов
11. Характерным физическим свойством ме не является
А) металлический блеск, электропроводность В) взаимодействие с кислотами
С) проводимость тока Д) ковкость
12. Единица измерения количества вещества называется
А) килограмм В) моль
С) литр)моль Д) ампер
13. Сколько литров содержится в 1 моль кислорода при н.у.
А) 22,4 л. В) 44,8л.
С) 4,48 л. Д) 12,6 л.
14. Какое количество атомов находится в 2моль азотной кислоты
А) 6,02*10 23 частиц В) 3,02 *10*23 частиц
С) 12,04*10*23 частиц Д) 0 частиц
15. 4 моль водорода прореагировало с кислородом.Сколько грамм воды получили
А) 18 гр. В)36 гр.
С) 34 гр. Д) 72 гр
16. 23 г натри вступило в реакцию с серной кислотой.Сколько литров газа получили
А) 22,4 л. В) 44,8 л.
С) 11,2л Д) 87 л.
17. Назовите ме , которые не реагируют с соляной кислотой
А)Au,Cu, Ag В) Ca, Fe, Mg
С) Na, Li, Ra Д) Ba, Ra, Al
18. Выберите только неактивные ме
А) алюминий, цинк, железо В) натрий, калий. литий
С) золото, ртуть, платина Д) натрий, цезий, магний
Календарно – тематическое планирование по химии 8 класс (О.С. Габриелян) – 3 часа в неделю.
| № | Дата | Тип урока | Тема урока | Элементы содержания | Вид контроля, самостоятельной работы. Требования к уровню подготовки уч-ся | Оборудование
| Домашнее задание: |
| Введение (6ч+ 1 ч. Практическая работа) |
| 1/1 |
| Вводный | Предмет химии. Вещества.Вводный инструктаж по охране труда и технике безопасности на уроках химии и при работе в лаборатории | Вводный инструктаж по технике безопасности. Предмет изучения химии. Понятие о химическом элементе и формах его существования: свободных атомах, простых и сложных веществах. | Устная и письменная работа с учебником: § 1; стр.10 Знать: понятие химия, вещество, химический элемент, атом. Молекула. Простое вещество, сложное вещество, свойства веществ Уметь: различать понятия тело и вещество, простое вещество и химический элемент, описывать свойства веществ.
| Презентация. Шаростержневые модели водорода, азота. Воды, углекислого газа. Х.Э: вода, сахар, уксусная к-та, изделия из алюминия, стекла, железа. Л.1: Сравнение свойств твердых кристаллических веществ и растворов. | Введение § 1, №2-4 §2, упр 3,4,6 |
| 2/2 |
| Комбинированный | Превращения веществ. Роль химии в жизни человека. | Физические и химические явления. Отличие химических реакций от физических явлений. Краткие сведения из истории возникновения и развития химии. | Устный опрос. Письменный опрос: индивидуальные задания. Устная и письменная работа с учебником: §3, №1,2, Знать: понятия физические явления, химические явления, химические реакции Уметь: отличать физические явления от химических по определенным признакам | Х.Э: карбонат кальция, соляная кислота, сульфат меди(, гидроксид натрия, индикаторы, известковая вода, пробирки. Спиртовка, прибор для получения газа. Видеоопыты: реакция горения, дым без огня. Д: Взаимодействие мрамора с кислотой и помутнение известковой воды Л.2: Сравнение скорости испарения с фильтровальной бумаги воды, одеколона и спирта | § 3, Упр.3- 5 §4, упр 1-3
|
| 3/3 |
| Урок –практическая работа | Практическая работа №1. Приемы обращения с лабораторным оборудование. Нагревание вещества на открытом пламени. | Правила ТБ и ОТ при работе в кабинете химии и химической лаборатории. Лабораторное оборудование. | Практическая работа №1. С тр. 198-204 Знать: правила ТБ и ОТ при работе в химической лаборатории; лабораторное оборудование. Уметь:наливать жидкости и засыпать твердые вещества в пробирку; работать со спиртовкой; нагревать вещества на открытом пламени, применяя лабораторный штатив и держатель для пробирок; описывать наблюдения и делать выводы. | Наборы раздаточного материала для практической работы. Инструкции по ТБ и ТО | Оформить практическую работу. |
| 4/4 |
| Комбинированный | Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов. | Первоначальные представления о ПСХЭ Д.И.Менделеева и её структуре. Химические знаки(символы) Х.Э., их произношение и написание | Письменная с/р:химический диктант. Устная и письменная работа с учебником: §5, таблица 1. Знать:структуру ПСХЭ-периоды, группы, подгруппы, символы х.э. и их произношение. Уметь:определять период, группу, подгруппу, порядковый номер х.э. в ПСХЭ
| Презентация. ПСХЭ Д.И.Менделеева. | § 5, №4-5, Выучить знаки х.э. Выучить таблицу №1
|
| 5/5 |
| Комбинированный | Химические формулы. Относительная атомная и относительная молекулярная массы. | Атомная единиуа массы, относительная атомная масса. Химическая формула и коэффициент. Относительная молекулярная масса. Закон постоянства состава вещества. Запись химических формул и вычисление относительной молекулярной массы. | Письменная с/р:химический диктант. Устная и письменная работа с учебником: §6,.№1,3 Знать: поняте относительная молекулярная и атомная массы, молекулярная формула, индекс, коэффициент. Закон постоянства состава вещества Уметь:определять относительную атомную массу х.э.; записывать химические формулы; вычислять относительную молекулярную массу по химической формуле; характеризовать вещество по химической формуле. | Презентация. ПСХЭ, справочные таблицы. План характеристики вещества по химической формуле. | § 6, упр.2,4,5,
|
| 6/6 |
|
| Вычисления по химической формуле | Характеристика вещества по химической формуле. Вычисления по химической формуле | Устный опрос. Письменный опрос: индивидуальные задания. Устная и письменная работа с учебником: §6, Знать: алгоритм вычисления массовой доли элемента по х.ф., установления простейшей формулы вещества по массовым долям элементов. Уметь: характеризовать вещество по х.ф.; осуществлять вычисления по химической формуле. | Презентация. ПСХЭ. План характеристики вещества по Х.ф.. Алгоритм решения расчетных задач по установлению формулы вещества. | § 6, упр.6,8,
|
| 7/7 |
| Урок контроля знаний | Обобщающий урок по теме «Химия-наука о веществах». Проверочная работа№1. Химическая формула. Вычисления по химической формуле. | Выявление знаний. Умений учащихся степени усвоения ими материала по теме «Химическая формула. Вычисление по химической формуле» | Проверочная работа №1. Знать: теоретический материал (урок1-5) Уметь: применять полученные знания и умения | Справочные таблицы | Повт. § 1-6 |
| Тема 1. Атомы химических элементов (12ч). |
| 8/1 |
| Урок изучения нового материала | Основные сведения о строении атомов. Состав атомных ядер. | Атомы как форма существования химических элементов. Основные сведения о строении атомов. Доказательства сложности строения атомов. Опыты Резерфорда. Планетарная модель строения атома.Состав атомных ядер: протоны, нейтроны.
| Устная и письменная работа с учебником: §7, 8 Знать: понятие радиоактивность, электронейтральность атома, элементарные частицы в составе атомаи их основные характеристики; физический смысл порядкового номера х.э. Уметь: определять состав атома х.э. по его порядковому номеру в ПСХЭ. | ПСХЭ. | §7, упр 2.4.6.7,
|
| 9/2 |
| Комбинированный урок | Измение в составе ядер атомов. Изотопы | Изотопы как разновидности атомов одного химического элемента.Изотопы водорода. Современное определение понятия «химический элемент». | Устная и письменная работа с учебником: § 8 Знать: понятия ядерные процессы, изотопы, химический элемент; сходство и различие атомов изотопов водорода по составу. Уметь: сравнивать состав атома х.э. с составом атома его изотопа | ПСХЭ Л.3: моделирование принципа действия сканирующего микроскопа | §8, №1-3 |
| 10-11/3-4 |
| Комбинированный урок | Электроны. Строение электронных оболочек атомов химических элементов № 1—20 периодической системы Д. И. Менделеева | Электроны. Главное квантовое число. Строение электронных уровней атомов химических элементов малых периодов. Понятие о завершенном электронном уровне. | Устная и письменная работа с учебником: § 9 Знать: понятия электронная оболочка, энергетический уровень, завершенный энергетический уровень, электронное облако, электронная формула. Уметь: составлять схемы строении электронных оболочек атомов х.э.1.2.3-го периода ПСХЭ, электронные формулы атомов х.э. 1-3 периодов ПСХЭ
| Таблица «Строение атомов х.э.. ПСХЭ. | § 9, упр.1-5. Сосавить э.ф. химических элементов малых периодов.
|
| 12/5 |
| Урок совершенствования знаний, умений и навыков | Металлические и неметаллические свойства элементов. Изменение свойств химических элементов по группам и периодам. | ПСХЭ : физический смысл порядкового номера элемента. Номера группы, номера периода. | Устная и письменная работа с учебником: § 10 до слов : «Каков же результат...» Знать: определения понятия «Элемент- металл», «Элемент-неметалл» Уметь: Объяснять закономерности изменения свойств х.э. в периодах и группа (главных подгруппах) ПСХЭ. Составлять характеристики химических элементов по положению в ПСХЭ. | ПСХЭ | §10,№ 1(б), 2(б,в)
|
| 13-14/6-7 |
| Урок изучения нового материала. | Ионная химическая связь. | Изменение числа электронов на внешнем энергетическом уровне атома х.э.- образование положительных и отрицательных ионов. Ионы. Образованные атомами металлов и неметаллов. Причина изменения металлических и неметаллических свойств в периодах и группах. Образование бинарных соединений. Понятие об ионной связи. Схемы образования ионной связи | Устная и письменная работа с учебником: §10 до конца. Знать: определения «Ионная связь», «Ионы». Уметь: составлять схемы образования ионной связи. Определять тип химической связи по формуле вещества. Приводить примеры веществ с ионным типом связи. Устанавливать причинно-следственные связи: состав вещества- вид химической связи. | Презентация: механизм образования ионной связи. Модели молекул веществ с ионным типом связи. Алгоритм составления электронной схемы образования ионной связи. | §10, №2-3 |
| 15/8 |
| Комбинированный урок | Взаимодействие атомов элементов-неметаллов между собой. Ковалентная неполярная связь. | Электроотрицательность(ЭО)-свойство неметаллических элементов. Изменение ЭО в периодах и группах ПСХЭ. Ряд ЭО. Механизм образования ковалентной неполярной химической связи между атомами элементов с одинаковой ЭО. Кратность и длина связи | Устный опрос. Письменный опрос: инд. Задания. Работа с учебником: §11 Знать: определение понятия «ковалентная неполярная связь»(к.н.с.) Уметь составлять схемы образования к.н.с. Определять тип х.с. по формуле вещества. Устанавливать причинно-следственные связи: состав вещества- вид химической связи. | Презентация: механизм образования и ковалентной неполярной связи. | §11, № 1-3.5 |
| 16/9 |
| Комбинированный урок | Взаимодействие атомов элементов-неметаллов между собой. Ковалентная полярная связь | Изменение ЭО в периодах и группах, главных подгруппах ПСХЭ. Механизм образования ковалентной полярной химической связи между атомами элементов с разной ЭО. Форма молекулы в пространстве. | Устный опрос. Письменный опрос: инд. Задания. Работа с учебником: §12 Знать: понятия ковалентная полярная связь, частичный заряд; механизм образования ковалентной полярной связи Уметь: характеризовать неметаллические элементы по их ЭО и образованию ковалентной полярной связи; определять соединения с ковалентной полярной связью и объяснять механизм её образования. | ПСХЭ. Справочные таблицы «Ковалентная полярная связь» Алгоритм составления электронной схемы образования к.п.с. Л.4: Изготовление моделей молекул бинарных соединений. | §12, упр1.2.5.6
|
| 17/10 |
| Комбинированный урок | Металлическая химическая связь | Металлическая связь. Механизм образования металлической химической связи. Сходство металлической связи с ковалентной и ионной связями и её отличие. | Устный опрос. Письменный опрос: инд. Задания. Работа с учебником §13 Знать: понятия металлическая связь, обобществленные электроны Уметь: характеризовать металлические элементы по особенностям строения их атомов; определять соединения с металлической связью и объяснять механизм её образования. | ПСХЭ. Таблица «Металлическая связь». Л.5: изготовление модели, иллюстрирующей свойства металлической связи. ЦОР: химическая связь | §13, упр 1-4 |
| 18/11 |
| Урок обобщающего повторения | Обобщение и повторение по теме «Атомы химических элементов» | Строение атома химического элемента, изотопы. Строение электронных оболочек атомов, электронная формула. Механизмы образования ковалентной полярной и неполярной связи. Ионной и металлической связи. Характеристика х.э. на основании его положения в ПСХЭ и строения атома. | Знать: теоретический материал(урок7-16) Уметь: определить вид х.с. и объяснять механизм образования; предполагать вид х.с., и объяснять её механизм | ПСХЭ | Повторить §7-13 |
| 19/12 |
| Урок контроля знаний | Контрольная работа №1.Атомы химических элементов. | Выявление знаний. Умений учащихся. Степени усвоения материала по главе 1. | Контрольная работа №1 |
|
|
| Тема 2. Простые вещества ( 9 ч.)
|
| 20/1 |
| Урок изучения нового материала | Просты вещества- металлы | Положение металлов и неметаллов в периодической системе химических элементов Д. И. Менделеева. Важнейшие простые вещества — металлы: железо, алюминий, кальций, магний, натрий, калий. Общие физические свойства металлов. Аллотропия, аллотропия модификации олова. | Письменная и устная работа с учебником: §14 Знать: понятие аллотропия, строение атомов металлов; особенности металлической связи; физические свойства металлов; аллотропные видоизменения олова; значение металлов в жизни человека. Уметь: характеризовать металлы по их положению в ПСХЭ, строению атома; описывать физические свойства металлов. | Реактивы: белое и серое олово. Д: Коллекция «Металлы и их сплавы». Презентация «Металлы- простые вещества» Л.6.: Ознакомление с коллекцией металлов | §14, упр 1,3,4 |
| 21/2 |
| Урок изучения нового материала | Простые вещества-неметаллы. | Особенности строения атомов неметаллов. Важнейшие простые вещества — неметаллы, образованные атомами кислорода, водорода, азота, серы, фосфора, углерода. Способность атомов химических элементов к образованию нескольких простых веществ — аллотропия. Аллотропные модификации кислорода, фосфора и олова. Металлические и неметаллические свойства простых веществ. Относительность деления простых веществ на металлы и неметаллы. | Письменная и устная работа с учебником: §15 Знать: строение атомов неметаллов; вид х.с. между атомами неметаллов; физические свойства неметаллов сравнении с металлами; аллотропные видоизменения кислорода и углерода; значение неметаллов в жизни человека Уметь: характеризовать неметаллы по их положению в ПСХЭ, строению атома; описывать физические свойства неметаллов. | Д: Получение кислорода и озона.(видиоопыт) Л.7.: Ознакомление с коллекцией неметаллов. | §15, упр 3.4
|
| 22/3 |
| Комбинированный урок | Количество вещества. Молярная масса. | Количество вещества и единица его измерения-моль. Молярная масса. Взаимосвязь массы, числа частиц и количества вещества. | Письменная и устная работа с учебником: §16 Знать: единицу количества измерения вещества моль. постоянную Авогадро; формулу вычисления количества вещества по числу структурных единиц вещества и постоянной Авогадро, формулу вычисления количества вещества по молярной массе вещества и массе вещества. Уметь: вычислять молярную массу по формуле соединения. Массу вещества и число структурных частиц по известному количеству вещества, используя единицы измерения -моль. ммоль, кмоль | ПСХЭ, Справочные таблицы. Презентация «Алгоритм вычисления количества вещества по молярной массе вещества и массе вещества» | § 16 Выучить определения, формулы, упр1 |
| 23/4 |
| Урок совершенствования знаний, умений и навыков | Вычисление молярной массы веществ по химическим формулам. | Расчеты с использованием понятий «количество вещества», «молярная масса», «постоянная Авогадро» | Уметь: Решать задачи с использование понятий «количество вещества», «молярная масса», «постоянная Авогадро» | Д: Некоторые металлы и неметаллы с количеством вещества 1 моль | § 16, выучить формулы, упр2.3.4 |
| 24/5 |
| Урок изучения нового материала | Молярный объем газообразных веществ. | Нормальные условия (н.у.)Молярный объем газообразных веществ. Кратные единицы измерения –миллимолярный и килломолярный объемы газообразных веществ. Расчеты с использованием понятий «количество вещества», «молярная масса», «Молярный объем газов», «Постоянная Авогадро». | Письменная и устная работа с учебником: §17 Знать: молярный объем газов количеством вещества 1 моль (н.у); формулу вычисления количества вещества по молярноу объему и количеству вещества. Уметь: вычислять количество вещества по известному объему газа и молярному объему, используя ед. Изм- л\моль, мл/ммоль, м3/кмоль
| Справочная таблица. Д: молярный объем газов газообразных веществ | §17 Упр 4,5 |
| 25/6 |
| Урок совершенствования знаний, умений и навыков | Взаимосвязь понятий: масса, объем, количество молекул. Относительная плотность газов. | 1 и2 Следствия закона Авогадро. Относительная плотность газов. | Письменная инд. и групповая работа. Знать: формулы и выводы из закона Авогадро: молярный объем, относительная плотность газов. Уметь: вычислять относительную плотность газов. | Справочные таблицы. | § 17. Выучить определения, формулы |
| 26/7 |
| Урок совершенствования знаний, умений и навыков | Решение задач с использование понятий «количество вещества», «постоянная Авогадро», «молярная масса», «молярный объем газов» | Расчеты с использование понятий «количество вещества», «постоянная Авогадро», «молярная масса», «молярный объем газов» | Письменная инд. и групповая работа. Знать: формулу вычисления количества вещества по молярной массе вещества и массе вещества. формулы и выводы из закона Авогадро: молярный объем, относительная плотность газов. Уметь: решать задачи с использование понятий «количество вещества», «постоянная Авогадро», «молярная масса», «молярный объем газов»
| Справочный материал. Карточки с инд. Заданием. | § 17.упр 4.5. |
| 27/8 |
| Урок совершенствования знаний, умений и навыков | Обобщение и систематизация знаний по теме «Простые вещества»
| Расчеты с использованием понятий «молярный объем газов», «постоянная Авогадро». | Письменная инд. и групповая работа. Знать: формулу количества вещества по молярной массе вещества и массе вещества, формулы и выводы из закона Авогадро: молярный объем, относительная плотность газов. Уметь: решать задачи с использование понятий «количество вещества», «постоянная Авогадро», «молярная масса», «молярный объем газов»
|
| Повт. § 14-17 подготовка к контр. работе |
| 28/9 |
| Урок контроля знаний | Контрольная работа.№2 Простые вещества. | Выявление знаний. Умений учащихся. Степень усвоения материала по главе 2. | Письменная инд. работа. Знать: теоретический материал (урок 21-24) Уметь: применять полученные знаний и умения
| Справочный материал. ПСХЭ |
|
| Тема 3. Соединения химических элементов (16 ч. + 2 ч пр. р.) |
| 29,/1 |
| Урок изучения нового материала | Степень окисления. (СО).Основы номенклатуры бинарных соединений. | Степень окисления. Определение степени окисления элементов по химической формуле соединения. Составление формул бинарных соединений, общий способ их названия. Бинарные соединения металлов и неметаллов: оксиды. Хлориды, сульфиды и пр. Составление их формул. | Письменная и устная работа с учебником: §18 Знать: понятия бинарные соединения, степень окисления, химическая номенклатура. Уметь: определять СО элементов в бинарных соединениях; составлять формулы бинарных соединений по СО элементов; называть бинарные соединения. Применяя химическую номенклатуру. | ПСХЭ. Ряд ЭО. | § 18, №1.2 Выучить определение, алгоритм составления формул бинарных соединений. |
| 30-31/2-3 |
| Комбинированный урок | Оксиды. Летучие водородные соединения. | Бинарные соединения неметаллов: оксиды, летучие водородные соединения, их состав и названия. Представители оксидов: вода, углекислый газ, негашеная известь. Представители летучих водородных соединений: хлороводород и аммиак. | Устный опрос. Письменный опрос: индивидуальные задания. Обучающая письменная работа с учебником.: § 19 №1,5,6 Знать: понятия оксиды, водородные соединения; нахождение в природе; физические свойства, область применения важнейших оксидов и водородных соединений. Уметь: составлять формулы оксидов металлов, оксидов неметаллов, водородных соединений и назвать их; определять по составу принадлежность его к классу оксидов или водородных соединений. | ПСХЭ, ряд ЭО, Д: образцы соединений: негашеная известь, оксида кремния, раствора аммиака, соляной кислоты. Л.8: Ознакомление с коллекцией оксидов. Л.9: Ознакомление со свойствами аммиака. | § 19, №2-4, записи в тетради. |
| 32-33/4-5 |
| Комбинированный урок | Основания. | Основания, их состав и названия. Растворимость оснований в воде. Представители щелочей. Таблица растворимости гидроксидов и солей в воде. Понятие об индикаторах и качественных реакциях. | Письменная самостоятельная работа. Устная и письменная работа с учебником § 20. Табл. №4; №1,2,5(а). Знать: понятия гидроксид-ион, основания, щелочи, гашенная известь, известковая вода, индикаторы; физические свойства и области применения важнейших оснований; способы определения растворимости оснований индикаторами; правила ОТ и ТБ при работе со щелочами. Уметь: составлять формулы оснований и называть их; определять по составу соединения принадлежность его к классу оснований; индикаторами определять растворимые основания- щелочи; работать с растворами щелочей, соблюдая правила ТО и ТБ. | ПСХЭ. Д: образцы оснований. Кислотно-щелочные индикаторы и изменения их окраски в щелочной среде. Л.10: Качественная реакция на углекислый газ. | § 20, упр. 3-4, 5(б) |
| 34-35/6-7 |
| Комбинированный урок | Кислоты. | Кислоты, их состав и названия. Классификация кислот. Качественное определение кислот индикаторами. Физические свойства кислот. Значение в жизни человека. Применение серной, сернистой, угольной кислоты .Правила ОТ и ТБ при работе с растворами кислот. Определение СО элементов в соединениях. | Устный опрос. Письменный опрос: инд. Задания. Устная и письменная работа с учебником: § 21.№ 1,3.5(а) Знать: понятия кислотный остаток, кислоты, простой ион, сложный ион, основность, кислородосодержащие кислоты, бескислородные кислоты; физические свойства и области применения важнейших кислот; способы определения растворов кислот индикаторами; правила ОТ и ТБ при работе с кислотами. Уметь: составлять формулы кислот и называть их; определять по составу кислоты, принадлежность их к классу кислот; индикаторами определять растворы кислот; растворять их в воде, соблюдая правила ТО и ТБ. . | ПСХЭ. Ряд ЭО. Реактивы: индикаторы, растворы щелочей, кислот. Л.11: Определение рН раствора кислоты и щелочи. Л.12. Определение рН лимонного сока и яблока на срезе плодов. | § 21. №2,4,5(б)Выучить названия кислот |
| 36-37/8-9 |
| Комбинированный урок | Соли. | Соли как производные кислот и оснований. Их состав и названия. Номенклатура солей. Растворимость солей в воде. Физические свойства, значение в жизни человека и применение хлорида натрия, карбоната кальция, фосфата кальция. Определение СО элементов в соединениях | Письменная самостоятельная работа6 тест. Устная и письменная работа с учебником: § 22 Знать: понятия соли; физические свойства и области применения солей- хлорида натрия, карбоната кальция, фосфата кальция. Уметь: составлять формулы солей и называть их; определять по составу соли, принадлежность их к классу солей; составлять формулы солей по названию; | ПСХЭ. Ряд ЭО. Таблица растворимости. Реактивы: растворы щелочей и кислот, индикаторы. Д: образцы солей. Л.13.: Ознакомление с коллекцией солей. | § 22, №1-3 Выучить формулы и названия солей, |
| 38/10 |
| Урок совершенствования знаний, умений и навыков | Обобщение знаний о классификации сложных веществ. | Классификация сложных веществ по составу. Составление формул и названий оксидов, оснований, кислот и солей. Решение экспериментальных задач на распознавание растворов кислот и щелочей. | Устный опрос. Письменный опрос. Знать: классификацию сложных неорганических веществ по составу на оксиды, основания, кислоты и соли, с использованием различных форм классификации. Уметь: Сравнивать оксиды, кислоты, основания и соли по составу. Определять принадлежность неорганических веществ к данному классу соединений. Определять валентности и СО элементов в веществах. Представлять информацию по теме в виде таблиц, опорного конспекта.
| ПСХЭ. Таблица растворимости. Реактивы: растворы кислот, солей и оснований. Индикаторы. |
|
| 39/11 |
| Урок изучения нового материала | Аморфные и кристаллические вещества. | Аморфные и кристаллические вещества. Межмолекулярные взаимодействия. Типы кристаллических решеток: ионная, атомная, молекулярная и металлическая. Зависимость свойств веществ от типов кристаллических решеток. Вещества молекулярного и немолекулярного строения. Закон постоянства состава для веществ молекулярного строения. | Письменная самостоятельная работа: тест. Устная и письменная работа с учебником: § 23 табл. 6, №1.2 Знать: понятия агрегатное состояние вещества, аморфные вещества, кристаллические вещества. Атомная к.р., ионная к.р., молекулярная к.р., металлическая к.р.. закон постоянства состава вещества. Уметь: характеризовать и объяснять свойства веществ (вода. Кислород, алмаз, хлорид натрия, алюминий) на основании вида химической связи и типа к.р. | ПСХЭ. През ентация: Типы кристаллических решеток. Д: Шаростержневые модели к.р. Л.14: ознакомление с коллекцией веществ с разным типом кристаллической решетки. Изготовление моделей к.р. | § 23 упр, 3,4,5,7 |
| 40/12 |
| Комбинированный урок | Физические явления в химии. Чистые вещества и смеси. Способы разделения смесей. | Чистые вещества и смеси. Примеры жидких, твердых и газообразных смесей. Свойства чистых веществ и смесей. Их состав. Массовая и объемная доля компонента смеси. Расчеты, связанные с использованием понятия «доля». | Устный опрос. Устная и письменная работа по учебнику § 24, №1,4, Знать: понятие чистое вещество, смесь, однородная смесь, неоднородная смесь; классификация смесей; способы разделения смесей Уметь: оперировать понятиями чистое вещество, смесь, однородная и неоднородная смесь, классифицировать смеси по определенным признакам, разделять однородные и неоднородные смеси. | Реактивы и оборудование: однородные смеси (р-ры солей, щелочей, кислот), неоднородные смеси(известковое молоко) Л.15. Ознакомление с образцом горной породы. | § 24, №2,3, презентации
|
| 41/13 |
| Урок -практическая работа | Практическая работа №3. Анализ почвы и воды. | Правила Тб и ТО. Способы разделения однородных и неоднородных смесей. Химический анализ почвенной вытяжки и воды. | Практическая работа №3, с 181-183 Знать: способы разделения однородных и неоднородных смесей. Уметь: осуществлять разделение неоднородной смеси фильтрованием и разделение однородной смеси выпариванием; проводить анализ почвенной вытяжки и воды; описывать наблюдение и делать выводы. | Наборы раздаточного материала для практической работы. Инструкции по ТБ и ТО | Оформить практическую работу |
| 42/14 |
| Комбинированный урок | Массовая и объемная доли компонента смеси. Расчеты, связанные с использованием понятия «доля». | Расчеты, связанные с использованием понятия «доля». Выполнение заданий по теме «Соединения химических соединений». | Письменная групповая и инд. работа. Знать: единицу измерения массовой доли (объемной) смеси(раствора); формулы вычисления массовой и объемной доли компонентов смеси (р-ра) Уметь: вычислять массовую и объемную долю вещества и массовую и объемную долю растворенного вещества по формулам. | ПСХЭ Справочная таблица | § 25, №3, 4 выучить формулы, разобрать образцы решения задач |
| 43/15 |
| Урок -практическая работа | Практическая работа №5. Приготовление раствора сахара и расчет его массовой доли в растворе | Правила по ТБ и ТО. Массовая доля растворенного вещества. | Знать: формулы вычисления массовой доли растворенного вещества. Уметь: решать расчетные задачи на вычисление массовой доли растворенного вещества, массы раствора и количества структурных частиц вещества; взвешивать вещества на лабораторных весах; описывать наблюдения. Делать выводы. | Инструкции. |
|
| 44-45/16-17 |
| Комбинированные уроки | Расчет массовой и объемной долей компонентов смеси веществ. | Расчеты, связанные с использованием понятия «доля».Выполнение заданий по теме «Соединения химических элементов» 1ч: Вычисление массовой доли вещества в растворе по известной массе растворенного вещества и массе растворителя. 2ч: Вычисление массы растворяемого вещества и растворителя, необходимых для приготовления определенной массы раствора с известной массовой долей растворенного вещества. | Письменная групповая и инд. работа. Знать: : единицу измерения массовой доли (объемной) смеси(раствора); формулы вычисления массовой и объемной доли компонентов смеси (р-ра) Уметь: Решать задачи с использованием формул массовую и объемную долю вещества и массовую и объемную долю растворенного вещества.
| ПСХЭ Справочная таблица | § 25 Упр1,2,4 |
| 46/18 |
| Урок контроля знаний. | Контрольная работа № 3 по теме: «Соединения химических элементов» | Выявление знаний, умений учащихся, степени усвоения материала по г.3 | Письменная инд. работа. Знать: теоретический материал (урок 28-41) Уметь: применять полученные знаний и умения
|
|
|
| Тема 4. Изменения, происходящие с веществами ( 16ч+ 2 ч практические работы ) |
| 47/1 |
|
| Физические явления. Разделение смесей. | Понятие явлений как изменений, происходящих с веществом. Явления, связанные с изменением кристаллического строения вещества при постоянном его составе, - физическое явление. Физические явления в химии: дистилляция, кристаллизация, выпаривание и возгонка веществ, центрифугирование. | Устный опрос. Устная и письменная работа с учебником. § 26. Знать: понятие чистое вещество, смесь, однородная смесь, неоднородная смесь, классификацию смесей; способы разделения однородной и неоднородной смесей. Уметь: оперировать понятиями чистое вещество, смесь, однородная и неоднородная смесь; классифицировать смеси по определенным признакам; разделять однородные и неоднородные смеси. |
| § 26. Упр. 3-6
|
| 48/2 |
|
| Химические явления. Условия и протекания химических реакций | Явления, связанные с изменением состава вещества, — химические реакции. Признаки и условия протекания химических реакций. Понятие об экзо- и эндотермических реакциях. Реакции горения как частный случай экзотермических реакций, протекающих с выделением света. | Письменная самостоятельная работа: тест. Устная и письменная работа с учебником: §27 Знать: понятия реакция горения, экзо- и эндотермические реакции; признаки химических реакций и условия их протекания. Уметь: по характерным признакам отличать химические реакции от физических явлений. | Реактивы и оборудование для хим. Эксперимента: Д: примеры химических явлений: горение магния. Фосфора; взаимодействие соляной кислоты с мрамором или мелом. | § 27, выучить определения, упр1,6 |
| 49/3 |
| Урок -практическая работа | Практическая работа №2. Наблюдение за горящей свечой. | Правила Тб и ТО. Метод познаний и наблюдений. Зависимость реакций от условий их протекания. Качественное определение продуктов реакции горения.
| Практическая работа №2. Стр. 199-200 Знать: отличия физических явлений от химических; условия протекания реакций; способы качественного определения продуктов реакции горения. Уметь: осуществлять химический эксперимент, соблюдать правила ТБ и ОТ; описывать наблюдения и делать соответствующие выводы. | Наборы раздаточного материала для пр. Работы. Инструкции по ТБ и ОТ | Оформить практическую работу. |
| 50/4 |
| Урок-практическая работа | Практическая работа №4. Признаки химических реакций. | Правила Тб и ТО. Признаки химических реакций и условия их протекания. | Практическая работа №4. Стр. 201-203 Знать: признаки химических реакций и условия их протекания. Уметь: осуществлять химический эксперимент. Соблюдать правила ТБ и ОТ; описывать наблюдения и делать выводы. | Наборы раздаточного материала для пр. Работы. Инструкции по ТБ и ОТ | Оформить практическую работу |
| 51/5 |
| Урок изучения нового материала. | Химические уравнения. Закон сохранения массы веществ. | Закон сохранения массы веществ. Уравнения химических реакций. Значение индексов и коэффициентов. | Самостоятельная работа: тест. Устная и письменная работа с учебником: § 28 Знать: формулировку закона сохранения массы вещества; алгоритм составления химических уравнений- правила подбора коэффициентов. Уметь: составлять уравнения химических реакций. |
| § 28. № 1-3. Выучить алгоритм. |
| 52/6 |
| Урок –закрепления нового материала | Составление уравнений химических реакций. | Закон сохранения массы веществ. Уравнения химических реакций. | Самостоятельная работа. Письменная работа. Знать: алгоритм составления химических уравнений- правила подбора коэффициентов. Уметь: составлять уравнения химических реакций. | Справочная таблица. | § 28. |
| 53-54 /7-8 |
| Комбинированный урок | Расчеты по химическим уравнениям. | Расчеты по химическим уравнениям. Решение задач на нахождение количества вещества, массы или объема продукта реакции по количеству вещества, массе или объему исходного вещества.
| Самостоятельная работа: решение задач. Устная и письменная работа с учебником: §29 Знать: единицы важнейших величин; алгоритм решения расчетных задач по уравнениям реакций. Уметь: решать расчетные задачи по уравнениям реакци1 и находить количество вещества, массу и объем продуктов реакции по количеству вещества, объему и массе исходных веществ.
| Справочная таблица. | § 29. Разобрать образцы решения задач. |
| 55/9 |
| Комбинированный урок | Расчеты по химическим уравнениям | Расчеты по химическим уравнениям. Расчеты с использованием понятия «доля», когда исходное вещество дано в виде раствора с заданной массовой долей растворенного вещества или содержит определенную долю примесей. | Самостоятельная работа: решение задач. Устная и письменная работа с учебником: §29 Знать: единицы важнейших величин; алгоритм решения расчетных задач по уравнениям реакций. Уметь: решать расчетные задачи по уравнениям реакций с понятием примеси, массовая доля растворенного вещества и находить количество вещества, массу и объем продуктов реакции по количеству вещества, объему и массе исходных веществ.
| Справочная таблица. | § 29. Упр1, 4 |
| 56/10 |
| Комбинированный урок | Реакции разложения | Типы химических реакций. Понятие о скорости химических реакций. Катализаторы. Ферменты. | Устный опрос. Лабораторная работа «Реакции разложения, катализаторы, ферменты, скорость химической реакции». Устная и письменная работа с учебником: §30 Знать: понятия реакции разложения, скорость химической реакции, катализаторы, ферменты. Уметь: оперировать понятиями; составлять уравнения химических реакций; осуществлять реакцию разложения, соблюдая правила ТБ и ОТ; описывать наблюдения и делать выводы.
| Реактивы и оборудование для химического эксперимента Д: Получение гидроксида меди(II); разложение перманганата калия; разложение пероксида водорода | § 30, упр 1, 3, 4 |
| 57/11 |
| Комбинированный урок | Реакции соединения | Реакции соединения. Каталитические и некаталитические реакции. Обратимые и необратимые реакции. | Устный опрос. Лабораторная работа «Реакции соединения». Устная и письменная работа с учебником: § 31 Знать: понятия реакции соединения, обратимые и необратимые реакции, каталитические и некаталитические реакции. Уметь: оперировать понятиями; составлять уравнения реакций соединения; осуществлять реакции соединения, соблюдая правила ТБ и ОТ; решать схемы превращения; описывать наблюдения и делать соответствующие выводы. | Реактивы и оборудование для химического эксперимента Л: 16 Окисление меди в пламени спиртовки. | § 31 упр 1, 2 |
| 58/12 |
| Комбинированный урок | Реакции замещения. Ряд активности металлов. | Реакции замещения. Электрохимический ряд напряжений металлов, его использование для прогнозирования возможности протекания реакций между металлами и растворами кислот. Реакции вытеснения одних металлов из растворов их солей другими металлами. | Устный опрос. Лабораторная работа «Реакции замещения». Устный опрос. Работа с учебником § 32. Знать: понятия реакций замещения, ряд напряжений металлов. Уметь: оперировать понятиями; составлять уравнения реакций замещения; пользоваться рядом напряжений металлов при составлении уравнений реакций замещения; осуществлять реакции замещения, соблюдая правила ТБ и ОТ; описывать наблюдения и делать соответствующие выводы. | Реактивы и оборудование для химического эксперимента Д: взаимодействие разбавленных кислот с металлами Л.17: Замещение меди в растворе хлорида меди (II) железом. | § 32. Упр1,2,3 |
| 59/13 |
| Комбинированный урок | Реакции обмена. Правило Бертолле. | Реакции обмена. Реакции нейтрализации. Условия протекания реакций обмена в растворах до конца. | Устный опрос. Устная и письменная работа § 33 Демонстрационный эксперимент «Реакции обмена и нейтрализации» Знать :понятия реакции обмена, реакции нейтрализации; условия протекания реакций обмена до конца. Уметь: оперировать понятиями; составлять уравнения реакций замещения; определять смысл реакций, зная условия её протекания; осуществлять реакции обмена, соблюдая правила ТБ и ОТ; описывать наблюдения и делать соответствующие выводы. | Реактивы и оборудование для химического эксперимента Д: Растворение гидроксида меди (II) в кислотах, взаимодействие с серной кислотой. | § 33 упр3, 4.6 |
| 60/14 |
| Урок совершенствования знаний, умений и навыков. | Типы химических реакций на примере свойств воды. | Типы химических реакций (по признаку «число и состав исходных веществ и продуктов реакции») на примере свойств воды. Химические свойства воды. Физические свойства воды, нахождение в природе. Значение воды в природе и жизни человека. | Письменная самостоятельная работа: тест. Устная и письменная работа с учебником § 34. Сообщения учащихся. Знать: понятие электролиз, фотолиз, фотосинтез, щелочные и щелочно-земельные металлы, гидроксиды, основания. Кислоты, гидролиз; типы химических реакций; условия взаимодействия оксидов металлов и оксидов неметаллов с водой. Уметь: Составлять уравнения реакций, характеризующие химические свойства воды.
| Реактивы и оборудование для химического эксперимента: вода, оксид кальция, сера, натрий металлический, универсальный индикатор; химическая посуда, ложечка для сжигания. | § 34, №1(б-д), 2.3.4 |
| 61-63/ 15-17 |
| Урок обобщающего повторения | Обобщение знаний по теме: «Изменения, происходящие с веществами» | Типы химических реакций: разложения, соединения, замещения, разложения. Условия протекания реакций обмена. Характеристика уравнений реакции: обратимость, скорость, выделения или поглощения энергии. | Устная и письменная самостоятельная работа по вопросам и заданиям. Письменная самостоятельная работа: тест. Знать: теоретический материал по теме. Уметь: применять полученные знания. | Справочная таблица. | Повт. § 26-34 |
| 64/18 |
| Урок контроля знаний | Контрольная работа № 4 по теме: «Изменения, происходящие с веществами» | Выявление знаний, умений учащихся, степени усвоения ими материала по главе 4. | Контрольная работа № 4 Знать: теоретический материал по теме. Уметь: применять полученные знания | Справочные таблицы | Повт. § 26-34 |
| Тема 5. Растворение. Растворы. Свойства растворов электролитов. ( 25ч +3 ч. практичекие работы) |
| 65/1 |
| Урок изучения нового материала | Растворение. Растворимость веществ в воде. | Растворы в природе и жизни человека. Растворение как физико-химический процесс. Тепловые явления при растворении и образовании гидратов и кристаллогидратов. Растворимость. Образование насыщенных и пересыщенных растворов. Растворимость кислот, оснований и солей при темп +20 гр. | Устная и письменная работа с учебником § 36, таблица 9. Знать: понятия растворы, гидраты, кристаллогидраты, растворимость, ненасыщенные растворы, насыщенные и пересыщенные растворы. Уметь: оперировать понятиями; работать с таблицей растворимости; решать простейшие задачи на растворимость | Таблица растворимости. Реактивы и оборудование для химического эксперимента: медный купорос, глауберова соль, концентрированная серная кислота. Д: приготовление раствора серной кислоты, кристаллогидрата сульфата меди(II) | § 36 упр. № 1,3.6 |
| 66/2 |
| Комбинированный урок | Электролитическая диссоциация | Виды химической связи. Электролитическая диссоциация. Электролиты и неэлектролиты. Механизм диссоциации электролитов с различным типом химической связи. Степень электролитической диссоциации. Сильные и слабые электролиты. | Устный опрос. Устная и письменная работа с учебником§ 36, 37. Сообщения учащихся. Знать: Понятия электролиты, неэлектролиты, ассоциация, электролитическая диссоциация, гидратированные ионы, ионы простые и сложные, степень электролитической диссоциации, сильные и слабые электролиты; механизм электролитической диссоциации. Уметь: Оперировать понятиями; объяснять механизм электролитической диссоциации; составлять уравнения диссоциации электролитов. | Таблица растворимости. Реактивы и оборудование для химического эксперимента: твердая поваренная моль и её раствор; уксусная и серная кислоты, раствор щелочи, прибор для работы с эл. Током. Д: электропрводность растворов солей. Кислот. Оснований. | § 36, №1-5. Доп. д/з |
| 67-68/3-4 |
| Комбинированный урок | Основные положения теории электролитической диссоциации. | Основные положения теории электролитической диссоциации. Катионы и анионы. Кислоты, основания и соли в свете ТЭД. | Устный опрос. Письменный опрос: инд. Задания. Устная и письменная работа с учебником § 37, сообщения учащихся. Знать: основные положения теории электролитической диссоциации; понятия катионы и анионы; определения кислоты, основания и соли в свете ТЭД. Уметь: объяснять свойства растворов кислот, оснований, солей в свете ТЭД; составлять уравнения диссоциации сильных и слабых электролитов. | Таблица растворимости. Реактивы и оборудование для химического эксперимента: твердая поваренная моль и её раствор; уксусная и серная кислоты, раствор щелочи, прибор для работы с эл. Током. Д: электропроводность растворов солей. Кислот. Оснований.
| § 37,№ 1-5 § 38,№ 1,2 |
| 69-/5 |
| Комбинированный урок | Ионные уравнения реакций | Ионные уравнения реакций. Условия протекания реакции обмена между электролитами до конца в свете ионных представлений. Уравнения реакции ионного обмена в молекулярном, ионном виде. | Письменная самостоятельная работа: тест. Лабораторные работы. Устная и письменная работа с учебником § 38 Знать: понятия реакции ионного обмена, реакции нейтрализации; признаки протекания реакций ионного обмена до конца. Уметь: составлять уравнения реакций ионного обмена в молекулярном виде, общем ионном виде и сокращенном ионном виде. | Реактивы и оборудования для химического эксперимента. Л18: взаимодействие раствора хлорида натрия с нитратом серебра Л19:получение нерастворимого гидроксида и взаимодействие его с кислотами. | § 38.№ 3, 5 |
| 70/6 |
| Урок -практическая работа | Практическая работа №6. Ионные реакции | Правила ТБ и ОТ. Ионные реакции | Практическая работа №6. Знать: признаки протекания реакций ионного обмена до конца. Уметь: осуществлять химический эксперимент с растворами электролитов, соблюдая правила ТБ и ОТ; описывать наблюдения и делать выводы. | Наборы раздаточного материала для практической работы. Инструкции по ТБ и ОТ | Оформить практическую работу. |
| 71/7 |
| Урок -практическая работа | Практическая работа №7 Условия протекания химических реакций между растворами электролитов до конца | Правила ТБ и ОТ. Признаки протекания реакций ионного обмена до конца | Практическая работа №7 Знать: признаки протекания реакций ионного обмена до конца. Уметь: осуществлять химический эксперимент с растворами электролитов, соблюдая правила ТБ и ОТ; описывать наблюдения и делать выводы. | Наборы раздаточного материала для практической работы. Инструкции по ТБ и ОТ | Оформить практическую работу |
| 72-74/9-11 |
| Комбинированный урок | Кислоты, их классификация и свойства. | Состав, номенклатура, классификация, диссоциация кислот. Химические свойства кислот в свете ТЭД. | Письменная самостоятельная работа. Устная и письменная работа с учебником: § 39 Лабораторная работа. Знать: классификацию кислот; химические свойства кислот; правила работы с рядом напряжения металлов. Уметь: объяснять свойства кислот в сете ТЭД, составлять уравнения химических реакций в молекулярном и ионнов виде и рассматривать их с позиции ОВР. | Реактивы и оборудование для химического эксперимента. Л.20: взаимодействие кислот с основаниями. Л.21.: взаимодействие кислот с оксидами металлов. Л.22: взаимодействие кислот с металлами. Л.23: взаимодействие кислот с солями. | § 39 упр1, 2, 3 |
| 7577/12-14 |
| Комбинированный урок | Основания, их классификация и свойства. | Состав, номенклатура, классификация, диссоциация оснований. Химические свойства оснований в свете ТЭД. | Письменная самстоятельная работа. Индивидуальные задания. Устная и письменная работа с учебником: § 40 Лабораторная работа. Знать: классификацию оснований; химические свойства оснований; разложение нерастворимых оснований. Уметь: объяснять свойства оснований в сете ТЭД, составлять уравнения химических реакций в молекулярном и ионном виде. | Реактивы и оборудование для химического эксперимента. Л.24: взаимодействие щелочей с кислотами Л.25: взаимодействие щелочей с оксидами металлов. Л.26: взаимодействие щелочей с солями. Л.27: получение и свойства нерастворимых оснований. | § 40упр. 1-6 |
| 78-79/15-16 |
| Комбинированный урок | Оксиды, их классификация и свойства.
| Состав, номенклатура, классификация, оксидов. Химические свойства оксидов в свете ТЭД. | Письменная самостоятельная работа.. Устная и письменная работа с учебником: § 41 Лабораторная работа. Знать: понятия несолеобразующие оксиды, основные оксиды, кислотные оксиды; классификацию оксидов; химические свойства оксидов. Уметь: объяснять свойства солеобразующих оксидов в свете ТЭД, составлять уравнения химических реакций в молекулярном и ионном виде .
| Реактивы и оборудование для химического эксперимента. Л.28: взаимодействие основных оксидов с кислотами. Л.29: взаимодействие основных оксидов с водой. Л.30: взаимодействие кислотных оксидов со щелочами. Л.31: Взаимодействие кислотных оскидов с водой. | § 41, №1-5 |
| 80-81/17-18 |
| Комбинированный урок | Соли, их классификация и свойства. | Состав, номенклатура, классификация, диссоциация солей. Химические свойства солей в свете ТЭД. | Устный опрос, письменный опрос. Индивидуальные задания. Устная и письменная работа с учебником: § 42 Лабораторная работа. Знать: классификацию солей; химический свойства средних солей; правила работа с рядом напряжений металлов. Уметь: объяснять свойства солей в свете ТЭД составлять уравнения химических реакций в молекулярном и ионном виде
| Реактивы и оборудование для химического эксперимента. Л.32: взаимодействие солей с кислотами. Л.33; взаимодействие солей со щелочами Л.34: взаимодействие солей с солями. Л.36.:взаимодействие растворов солей с металлами. | § 42. № 1-5 |
| 82/19 |
| Комбинированный урок | Генетическая связь между классами неорганических веществ. | Химические свойства кислот, оснований, оксидов, солей в свете ТЭД. Генетический ряд металлов и неметаллов. Генетическая связь классов неорганических соединений. | Письменная самостоятельная работа: тест. Устная и письменная работа с учебником: § 43. Знать: понятия генетический ряд, генетическая связь классов неорганических соединений. Уметь: составлять уравнения реакций по схеме превращения, составлять и решать схемы генетической связи классов соединений, составлять схемы генетических рядов металлов и неметаллов. | Справочные таблицы. | § 43. № 1,2, 4 |
| 83/20- |
| Урок-практическая работа | Практическая работа №8. Свойства кислот, оснований, оксидов и солей. | Правила ТБ и ОТ. Химические свойства кислот, оснований, оксидов и солей в свете ТЭД. Реакции ионного обмена и качественный состав вещества. Схема генетической связи классов веществ | Практическая работа №8. Знать: химические свойства кислот, оснований, оксидов и солей в свете ТЭД; схему генетической связи классов веществ. Уметь: осуществлять химический эксперимент по изучению свойств кислот, оснований, оксидов и солей. Соблюдая правила ТБ и ОТ; описывать наблюдения, делать соответствующие выводы. | Наборы раздаточного материала для химического эксперимента. | Оформить работу. |
| 84/21 |
| Урок изучения нового материала | Окислительно-восстановительные реакции(ОВР). | Степень окисления. Определения степени окисления химических элементов в соединениях. Окислительно-восстановительные реакции(ОВР). Окислитель и восстановитель, окисление и восстановление. | Устная и письменная работа с учебником. §44 Знать: понятие окислительно-восстановительные реакции, окислитель. Восстановитель, процесс окисления и восстановления, метод электронного баланса (МЭБ) Уметь: определять окислитель, восстановитель, процесс окисления и восстановления в ОВР; составлять уравнения ОВР методом электронного баланса. | Справочная таблица, Алгоритм составления уравнения ОВР МЭБ. Д:взаимодействие цинка с серой, соляной кислотой, хлоридом меди(II)горение магния. | §44, №1-3 |
| 85-86/22-23 |
| Урок обобщающего повторения | Составление уравнений окислительно-восстановительных реакций методом электронного баланса. | Составление уравнений методом ОВР. | Устная и письменная работа с учебником. §44. Письменная самостоятельная работа: тест. Знать: основные понятия учения об ОВР; метод электронного баланса. Уметь: определять ОВР; составлять уравнения ОВР методом электронного баланса. | ПСХЭ, справочные таблицы, алгоритм составления уравнения ОВР методом электронного баланса | Дополнительные задания. |
| 87/24 |
| Комбинированный урок | Свойства изученных классов веществ окислительно-восстановительных процессах. | Свойства кислот, солей, оксидов и оснований в свете учения об ОВР. | Устный опрос. Письменный опрос: индивидуальные задания. Обучающая письменная самостоятельная работа. Знать: химические свойства кислот, солей, оксидов и оснований. Уметь: составлять уравнения реакций, характеризующих химические свойства основных классов неорганических соединений в молекулярном, ионном виде и рассматривать их с позиции ОВР. | Справочная таблица | Дополнительные задания. |
| 88/25 |
| Урок -практическая работа | Практическая работа №9. Решение экспериментальных задач. | Правила ОТ и ТБ. Физические и химические свойства кислот, оснований, оксидов и солей в свете теорий электролитической диссоциации и ОВР. Подтверждение качественного состава вещества реакциями ионного обмена. Схема генетической связи классов веществ. | Практическая работа №9. Знать: физические и химические свойства кислот, оснований, оксидов и солей в свете теорий электролитической диссоциации и ОВР; схему генетической связи классов веществ. Уметь: осуществлять химический эксперимент по изученной теме, соблюдая правила ТБ и ОТ; описывать наблюдения и делать выводы. | Наборы раздаточного материала для химического эксперимента. | Оформить работу. |
| 89-90/25-26 |
| Урок обобщающего повторения. | Растворы. Реакции ионного обмена и ОВР. Решение расчетных задач по формуле и по уравнениям реакций. | Обобщение и повторение по теме «Растворение. Растворы. Реакции ионного обмена и ОВР» | Устная и письменная групповая работа по вопросам задания. Письменная самостоятельная работа: тест. Знать: теоретический материал по теме. Уметь: применять полученные знания и умения. | ПСХЭ. Справочные таблицы. | Повт. § 36-44 |
| 91/27 |
| Урок обобщающего повторения. | Решение расчетных задач по уравнениям химических реакций. | Обобщение и повторение по теме «Растворение. Растворы. Реакции ионного обмена и ОВР» | Устная и письменная групповая работа по вопросам задания. Письменная самостоятельная работа: тест. Знать: теоретический материал по теме. Уметь: применять полученные знания и умения. | ПСХЭ. Справочные таблицы. | Дополнительные задания. |
| 92/28 |
| Урок контроля знаний | Контрольная работа № 5 по теме: «Растворение. Растворы. Свойства электролитов» | Выявление знаний и умений учащихся, степени усвоения ими материала по главе 4. | Контрольная работа № 5 Знать: теоретический материал по теме. Уметь: применять полученные знания и умения. | ПСХЭ. Справочные таблицы | Повт. § 36-44 |
| Тема 6. Повторение вопросов 8 класса. (7ч.) |
| 93 |
|
| ПСХЭ и строение атома. |
| Устная и письменная работа с учебником. Сообщения учащихся. Знать строение атома Уметь составлять электронные формулы атомов химических элементов. |
| Дополнительные задания |
| 94 |
|
| Важнейшие классы неорганических соединений | Основные классы неорганических соединений: оксиды(классификация), кислоты, основании, соли. | Знать химические формулы. Уметь различать по классам . Определять С.О. химических элементов в соединениях. |
|
|
| 95 |
|
| Химические реакции. |
| Знать основные типы химических реакций Уметь различать и составлять уравнения химических реакций в свете ТЭД и ОВР. |
|
|
| 96 |
|
| Решение расчетных задач по теме Растворы. |
|
|
|
|
| 97 |
|
| Решение расчетных задач по уравнениям химических реакций. | Обобщение и повторение по теме «Растворение. Растворы. Реакции ионного обмена и ОВР» | Устная и письменная групповая работа по вопросам задания. Письменная самостоятельная работа: тест. Знать: теоретический материал по теме. Уметь: применять полученные знания и умения. | ПСХЭ. Справочные таблицы. | Дополнительные задания. |
| 98 |
|
| Обобщающий урок. Подготовка к итоговой контрольной работе. |
|
|
|
|
| 99 |
|
| Контрольная работа № 6. Годовая |
|
|
|
|
| Тема 9. Учебные экскурсии (3ч.) |
| 100-102 |
|
| Учебная экскурсия. Резервное время |
|
|
| Отчёт по плану |
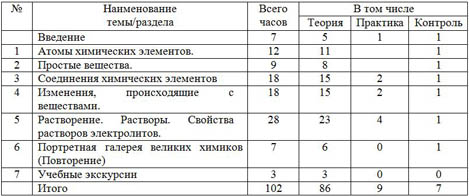

 Получите свидетельство
Получите свидетельство Вход
Вход











 Рабочая программа по химии (8 класс) (0.1 MB)
Рабочая программа по химии (8 класс) (0.1 MB)
 1
1 1023
1023 69
69 Нравится
0
Нравится
0



