Пояснительная записка
Рабочая программа по химии предназначена для учащихся 8-х классов и рассчитана на 68 часов в год, по 2 часа в неделю, резервное время -2 часа. На выполнение практической части программы отведено 7 часов. Предусмотрено 6 контрольных работ, из них одна итоговая.
Рабочая программа по химии в 8 классе составлена на основе «Программы общеобразовательных учреждений. 8-9 классы. 10-11 классы» Н.Н.Гара, Москва «Просвещение» 2010 г. и реализуется при помощи учебника «Неорганическая химия» Г.Е.Рудзитис, Ф.Г.Фельдман, 2010 г. Программа составлена в соответствии с федеральным компонентом государственного стандарта основного общего образования.
При организации учебного процесса используются следующие формы: уроки изучения новых знаний, уроки закрепления знаний, комбинированные уроки, уроки обобщения и систематизации знаний, уроки контроля, практические работы, а также сочетание указанных форм.
Преобладающими формами текущего контроля знаний, умений и навыков являются
самостоятельные и контрольные работы, различные тестовые формы контроля, практические работы.
Изучение химии в основной школе направлено на достижение следующих целей:
освоение важнейших знаний об основных понятиях и законах химии, химической символике;
овладение умениями наблюдать химические явления, проводить химический эксперимент, производить расчеты на основе химических формул веществ и уравнений химических реакций;
развитие познавательных интересов и интеллектуальных способностей в процессе проведения химического эксперимента, самостоятельного приобретения знаний в соответствии с возникающими жизненными потребностями;
воспитание отношения к химии как к одному из фундаментальных компонентов естествознания и элементу общечеловеческой культуры;
применение полученных знаний и умений для безопасного использования веществ и материалов в быту, сельском хозяйстве и на производстве, решения практических задач в повседневной жизни, предупреждения явлений, наносящих вред здоровью человека и окружающей среде.
Общая характеристика учебного предмета
Весь теоретический материал курса химии для основной школы структурирован по шести блокам: Методы познания веществ и химических явлений. Экспериментальные основы химии; Вещество; Химическая реакция; Элементарные основы неорганической химии; Первоначальные представления об органических веществах; Химия и жизнь. Содержание этих учебных блоков в программе направлено на достижение целей химического образования.
В курсе 8 класса учащиеся изучают первоначальные химические понятия, неметаллы - кислород и водород, растворы, основные классы неорганических соединений, периодический закон и периодическую систему химических элементов Д.И.Менделеева, строение атома, строение веществ, химическую связь, закон Авогадро, галогены. Приобретаются навыки в выполнении практических работ и решении качественных и расчетных задач.
Учет межпредметных связей в преподавании неорганической химии позволяет более рационально использовать изучение нового материала путем устранения дублирования между новым и уже изученным содержанием. Межпредметные связи прослеживаются как вертикальные (между ступенями образования), так и горизонтальные (на одной ступени обучения) между химией и другими курсами. Курс неорганической химии 8 класса опирается в большей степени на знание курса алгебры, физики, биологии, частично истории и географии. Перечисленные науки дают для химии следующие понятия:
Алгебра: Расчетные задачи - вычисление относительной молекулярной массы вещества по формуле; вычисление массовой доли элемента в химическом соединении. Составление формул соединений по валентности; вычисления по химическим уравнениям массы и количества одного из продуктов реакции по массе исходного вещества; определение массовой доли растворенного вещества). Изучение данных тем предполагает наличие математических знаний у учащихся.
Физика: Предмет химии. Вещества и их свойства. Закон Авогадро. Закон сохранения массы веществ. Физические свойства веществ, агрегатное состояние изучаются в темах: «Основные классы неорганических соединений»; «Кислород, его общая характеристика и нахождение в природе»; «Воздух и его состав»; «Водород, его общая характеристика и нахождение в природе»; «Вода - растворитель». Тепловой эффект химических реакций (эндо- и экзотермические реакции). Физические явления. Молекулы и атомы. Атомно-молекулярное учение. Строение атома. Кристаллические решетки.
Биология: Физические и химические явления. Химическое загрязнение окружающей среды и его последствия. Круговорот кислорода в природе. Вода. Растворы. Кислород, его общая характеристика и нахождение в природе.
География: Чистые вещества и смеси. Круговорот воды в природе. Чистые вещества и смеси.
История: Вклад ученых разных стран в становление химии как науки.
РАСПРЕДЕЛЕНИЕ ЧАСОВ РАБОЧЕЙ ПРОГРАММЫ
| Наименование тем | Количество часов авторской программы | Количество часов рабочей программы |
| Первоначальные химические понятия | 18 |
15 (3 часа использованы на тему " Основные классы неорганических соединений") |
| Кислород. Горение | 5 | 6 (Один час добавлен из темы «Периодический закон и периодическая таблица химических элементов Д.И.Менделеева. Строение атома») |
| Водород | 3 | 3 |
| Растворы. Вода | 6 | 7 (1 час добавлен из темы "Галогены" для обобщающего урока) |
| Основные классы неорганических соединений | 9 | 16 (3 часа добавлены из темы " Первоначальные химические понятия ", 3 часа из темы " Химическая связь. Строение веществ" и 1 час добавлен из темы "Резервное время") |
| Периодический закон и периодическая таблица химических элементов Д.И.Менделеева. Строение атома | 8 | 6 (1 час использован на тему «Кислород. Горение») |
| Химическая связь. Строение веществ | 9 | 6 (3 часа использованы на тему «Основные классы неорганических соединений»)
|
| Закон Авогадро. Молярный объем газов | 3 | 3 |
| Галогены | 6 | 5 |
| Резервное время | 3 |
2 |
| Итого | 70 (по федеральному плану) |
68 (по плану МБОУ «СОШ № 17») |
РАСПРЕДЕЛЕНИЕ ПРАКТИЧЕСКИХ РАБОТ
|
Наименование тем (разделов) |
Практическая работа авторской программы
|
Практическая работа рабочей программы |
|
Первоначальные химические понятия | Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием.
| Правила техники безопасности при работе в химическом кабинете. Приемы обращения с лабораторным штативом и спиртовкой, изучение строения пламени.
|
| Очистка загрязненной поваренной соли. | Очистка загрязненной поваренной соли. |
| Кислород. Горение | Получение и свойства кислорода. | Получение, собирание и распознавание кислорода.
|
| Водород |
- | Получение, собирание и распознавание водорода. |
| Растворы. Вода | Приготовление растворов солей с определенной массовой долей растворенного вещества.
|
Приготовление раствора соли с определенной массовой долей вещества.
|
| Основные классы неорганических соединений | Решение экспериментальных задач по теме «Основные классы неорганических соединений».
| Решение экспериментальных задач по теме «Основные классы неорганических соединений».
|
| Периодический закон и периодическая таблица химических элементов Д.И.Менделеева. Строение атома |
- |
- |
| Химическая связь. Строение веществ |
-
|
- |
| Закон Авогадро. Молярный объем газов |
-
|
- |
| Галогены | Получение соляной кислоты и изучение ее свойств.
| Химические свойства соляной кислоты. |
|
Итого
|
6 практических работ |
7 практических работ |
График проведения практических работ
по химии в 8-х классах на 2014-2015 учебный год
| № практической работы | Дата проведения |
Тема практической работы |
|
1 |
|
«Правила техники безопасности при работе в химическом кабинете. Приёмы обращения с лабораторным штативом и спиртовкой, изучение строения пламени»
|
|
2 |
|
«Очистка загрязненной поваренной соли»
|
|
3 |
|
«Получение, собирание и распознавание кислорода»
|
|
4 |
|
«Получение, собирание и распознавание водорода»
|
|
5 |
|
«Приготовление раствора соли с определенной массовой долей вещества»
|
|
6 |
|
Решение экспериментальных задач по теме "Основные классы неорганических соединений"
|
|
7 |
|
«Химические свойства соляной кислоты»
|
Содержание рабочей программы
Тема 1. Первоначальные химические понятия (15 ч)
Предмет химии. Химия как часть естествознания. Вещества и их свойства. Чистые вещества и смеси. Способы очистки веществ: отстаивание, фильтрование, выпаривание, кристаллизация, дистилляция, хроматография. Физические и химические явления. Химические реакции. Признаки химических реакций и условия возникновения и течения химических реакций.
Атомы и молекулы. Вещества молекулярного и немолекулярного строения. Качественный и количественный состав вещества. Простые и сложные вещества. Химический элемент. Язык химии. Знаки химических элементов, химические формулы. Закон постоянства состава веществ.
Атомная единица массы. Относительная атомная и молекулярная массы. Количество вещества, моль. Молярная масса.
Валентность химических элементов. Определение валентности элементов по формулам их соединений. Составление химических формул по валентности.
Атомно-молекулярное учение. Закон сохранения массы веществ. Химические уравнения. Классификация химических реакций по числу и составу исходных и полученных веществ.
Демонстрации. Ознакомление с образцами простых и сложных веществ. Способы очистки веществ: кристаллизация, дистилляция, хроматография. Опыты, подтверждающие закон сохранения массы веществ.
Химические соединения количеством вещества 1 моль. Модель молярного объема газов.
Лабораторные опыты. Рассмотрение веществ с различными физическими свойствами. Разделение смеси с помощью магнита. Примеры физических и химических явлений. Реакции, иллюстрирующие основные признаки характерных реакций. Разложение основного карбоната меди(II). Реакция замещения меди железом.
Практические работы.
Правила техники безопасности при работе в химическом кабинете. Приемы обращения с лабораторным штативом и спиртовкой, изучение строения пламени.
Очистка загрязненной поваренной соли.
Расчетные задачи. Вычисление относительной молекулярной массы вещества по формуле. Вычисление массовой доли элемента в химическом соединении. Установление простейшей формулы вещества по массовым долям элементов. Вычисления по химическим уравнениям массы или количества вещества по известной массе или количеству одного из вступающих или получающихся в реакции веществ
Тема 2. Кислород. Горение (6 ч)
Кислород. Нахождение в природе. Физические и химические свойства. Получение, применение. Круговорот кислорода в природе. Горение. Оксиды. Воздух и его состав. Медленное окисление. Тепловой эффект химических реакций.
Топливо и способы его сжигания. Защита атмосферного воздуха от загрязнений.
Демонстрации. Получение и собирание кислорода методом вытеснения воздуха, методом вытеснения воды. Определение состава воздуха. Коллекции нефти, каменного угля и продуктов их переработки.
Лабораторные опыты. Ознакомление с образцами оксидов.
Практическая работа. Получение, собирание и распознавание кислорода.
Расчетные задачи. Расчеты по термохимическим уравнениям.
Тема 3. Водород (3 ч)
Водород. Нахождение в природе. Физические и химические свойства. Водород — восстановитель. Получение, применение.
Демонстрации. Получение водорода в аппарате Киппа, проверка водорода на чистоту, горение водорода, собирание водорода методом вытеснения воздуха и воды.
Практическая работа. Получение, собирание и распознавание водорода.
Тема 4. Растворы. Вода. (7 ч)
Вода — растворитель. Растворимость веществ в воде. Определение массовой доли растворенного вещества. Вода. Методы определения состава воды — анализ и синтез. Физические и химические свойства воды. Вода в природе и способы ее очистки. Круговорот воды в природе.
Практическая работа. Приготовление раствора соли с определенной массовой долей вещества.
Расчетные задачи. Нахождение массовой доли растворенного вещества в растворе. Вычисление массы растворенного вещества и воды для приготовления раствора определенной концентрации
Тема 5. Основные классы неорганических соединений (16 ч)
Оксиды. Классификация. Основные и кислотные оксиды. Номенклатура. Физические и химические свойства. Получение. Применение.
Основания. Классификация. Номенклатура. Физические и химические свойства. Реакция нейтрализации. Получение. Применение.
Кислоты. Классификация. Номенклатура. Физические и химические свойства. Вытеснительный ряд металлов Н. Н. Бекетова. Применение.
Соли. Классификация. Номенклатура. Физические и химические свойства. Способы получения солей.
Генетическая связь между основными классами неорганических соединений.
Демонстрации. Знакомство с образцами оксидов, кислот, оснований и солей. Нейтрализация щелочи кислотой в присутствии индикатора.
Лабораторные опыты. Опыты, подтверждающие химические свойства кислот, оснований.
Практическая работа. Решение экспериментальных задач по теме «Основные классы неорганических соединений».
Тема 6. Периодический закон и периодическая таблица химических элементов
Д.И.Менделеева. Строение атома (6 ч)
Первые попытки классификации химических элементов. Понятие о группах сходных элементов. Периодический закон Д. И. Менделеева. Периодическая таблица химических элементов. Группы и периоды. Короткий и длинный варианты периодической таблицы. Значение периодического закона. Жизнь и деятельность Д. И. Менделеева.
Строение атома. Состав атомных ядер. Электроны. Изотопы. Строение электронных оболочек атомов первых 20 элементов периодической системы Д. И. Менделеева.
Лабораторные опыты. Взаимодействие гидроксида цинка с растворами кислот и щелочей.
Тема 7. Химическая связь. Строение веществ (6 ч)
Электроотрицательность химических элементов. Основные виды химической связи: ковалентная неполярная, ковалентная полярная, ионная. Валентность элементов в свете электронной теории. Степень окисления. Правила определения степени окисления элементов. Окислительно-восстановительные реакции.
Кристаллические решетки: ионная, атомная и молекулярная. Кристаллические и аморфные вещества. Зависимость свойств веществ от типов кристаллических решеток.
Демонстрации. Ознакомление с моделями кристаллических решеток ковалентных и ионных соединений. Сопоставление физико-химических свойств соединений с ковалентными и ионными связями.
Тема 8. Закон Авогадро. Молярный объем газов (3 ч)
Закон Авогадро. Молярный объем газов. Относительная плотность газов. Объемные отношения газов при химических реакциях.
Расчетные задачи. Объемные отношения газов при химических реакциях.
Вычисления по химическим уравнениям массы, объема и количества вещества одного из продуктов реакции по массе исходного вещества, объему или количеству вещества, содержащего определенную долю примесей.
Тема 9. Галогены (5 ч)
Положение галогенов в периодической таблице и строение их атомов. Хлор. Физические и химические свойства хлора. Применение. Хлороводород. Соляная кислота и ее соли. Сравнительная характеристика галогенов.
Демонстрации. Знакомство с образцами природных хлоридов. Знакомство с физическими свойствами галогенов. Получение хлороводорода и его растворение в воде.
Лабораторные опыты. Распознавание соляной кислоты, хлоридов, бромидов, иодидов и иода. Вытеснение галогенов друг другом из раствора их соединений.
Практическая работа. Химические свойства соляной кислоты.
Тема 10. Заключение (2 ч)
Обобщение знаний по курсу 8 класса. Итоговое повторение. Резервное время.
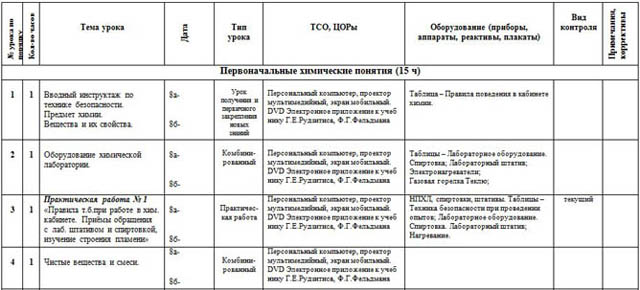
Тематическое планирование 8 класс. Учебник Г.Е.Рудзитис, Ф.Г.Фельдман
| № урока по порядку
| Кол-во часов
|
Тема урока |
Дата |
Тип урока |
ТСО, ЦОРы |
Оборудование (приборы, аппараты, реактивы, плакаты) |
Вид контроля | Примечания, коррективы
|
| Первоначальные химические понятия (15 ч) |
|
1 |
1 |
Вводный инструктаж по технике безопасности. Предмет химии. Вещества и их свойства.
|
8а-
8б- |
Урок получения и первичного закрепления новых знаний |
Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Правила поведения в кабинете химии. |
|
|
|
2 |
1 |
Оборудование химической лаборатории.
|
8а-
8б- |
Комбини-рованный |
Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Таблицы – Лабораторное оборудование. Спиртовка; Лабораторный штатив; Электронагреватели; Газовая горелка Теклю; |
|
|
|
3 |
1 | Практическая работа № 1 «Правила т.б.при работе в хим. кабинете. Приёмы обращения с лаб. штативом и спиртовкой, изучение строения пламени» |
8а-
8б- |
Практичес-кая работа | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| НПХЛ, спиртовки, штативы. Таблицы – Техника безопасности при проведении опытов; Лабораторное оборудование. Спиртовка. Лабораторный штатив; Нагревание. | текущий |
|
|
4 |
1 |
Чистые вещества и смеси.
| 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
|
|
|
|
5 |
1 |
Практическая работа № 2 «Очистка загрязненной поваренной соли»
| 8а-
8б- |
Практичес-кая работа |
| НПХЛ, спиртовки, Таблицы – Лабораторное оборудование. Нагревание; Техника экспериментальной работы. Обращение с твердыми веществами. Взвешивание. Фильтрование. | текущий |
|
|
6 |
1 |
Физические и химические явления. Хим-ие реакции. Молекулы и атомы.
|
8а-
8б- |
Комбини-рованный |
Персональный компьютер, проек-тор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Демонстрационный набор для составления объёмных моделей молекул. Таблица - физические явления и химические реакции |
|
|
|
7 |
1 |
Простые и сложные вещества. Химические элементы.
| 8а-
8б- |
Комбини-рованный |
Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Периодическая система химических элементов Д.И.Менделеева. |
|
|
|
8 |
1 |
Знаки химических элементов. Относит. атомная масса хим-их элементов.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблицы – Знаки, Периодическая система химических элементов Д.И.Менделеева. |
|
|
|
9 |
1 |
З-н постоянства состава веществ. Хим-ие формулы. Относит. молекулярная масса. | 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Периодическая система химических элементов Д.И.Менделеева. |
|
|
| 10 | 1 | Валентность химических элементов. | 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица- Валентность. |
|
|
| 11 | 1 | Определение валентности элементов по фор-м их соед-й. Составление хим-х формул по валентности. | 8а-
8б-
| Комбини-рованный |
|
|
|
|
|
12 |
1 |
Атомно-молекулярное учение. З-н сохранения массы веществ. Хим-ие уравнения. | 8а-
8б-
|
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Прибор для иллюстрации закона сохранения массы веществ. Таблица- |
|
|
|
13 |
1 |
Типы химических реакций.
| 8а-
8б-
|
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Таблица – классификация химических реакций. |
|
|
|
14 |
1 |
Количество вещества. Моль. Молярная масса.
| 8а-
8б- |
Комбини-рованный
|
|
|
|
|
|
15 |
1 |
Контрольная работа № 1 по теме «Первоначальные химические понятия» | 8а-
8б- | Урок контроля, оценки и коррекции знаний учащихся |
|
|
текущий |
|
| Кислород. Горение (6 ч) |
|
16 |
1 |
Кислород его общая хар-ка и нахождение в природе. Получение кислорода. | 8а-
8б- | Урок получения и первично го закрепле ния новых знаний | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Периодическая система химических элементов Д.И.Менделеева. |
|
|
|
17 |
1 |
Свойства, применение и круговорот кислорода в природе. | 8а-
8б- | Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
18 |
1 |
Выполнение упражнений.
| 8а-
8б-
|
|
|
|
|
|
|
19 |
1 |
Воздух и его состав. Топливо и способы его сжигания. |
8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Прибор для определения состава воздуха |
|
|
|
20 |
1 |
Практическая работа № 3 «Получение, собирание и распознавание кислорода» |
8а-
8б- |
Практичес кая работа |
| НПХЛ, реактивы, КДОХУ Таблицы – Техника безопасности при работе с газами; Техника эксперимен-тальной работы; Получение и собирание газов. | текущий |
|
|
21 |
1 |
Тепловой эффект химических реакций.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Таблица – Тепловой эффект химической реакции. |
|
|
| Водород (3 ч) |
|
22 |
1 |
Водород, его общая характеристика и нахождение в природе. Получение водорода. |
8а-
8б- | Урок получения и первично го закрепле ния новых знаний | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| Аппарат Киппа, прибор для получения газов лабораторный. Таблицы – Техника безопасности при работе с газами; Техника экспериментальной работы; Получение и собирание газов. |
|
|
|
23 |
1 |
Свойства и применение водорода. | 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
24 |
1 |
Практическая работа № 4 «Получение, собирание и распознавание водорода» | 8а-
8б- |
Практичес кая работа |
| НПХЛ, реактивы, КДОХУ.Таблицы – Техника безопасности при работе с газами; Техника экспериментальной работы; Получение и собирание газов. | текущий |
|
|
Растворы. Вода. (7 ч) |
|
25 |
1 |
Вода- растворитель. Растворы.
| 8а-
8б- | Урок получения и первично го закрепле ния новых знаний | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| Аппарат для дистилляции воды. Набор посуды для дистилляции воды. Таблица – Техника экспериментальной работы. Перегонка. |
|
|
|
26 |
1 |
Определение массовой доли растворенного вещества.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| Весы технические демонстрационные Т-1000 с набором гирь. Таблицы – Техника экспериментальной работы. Взвешивание; Приготовление растворов; Обращение с твердыми веществами. |
|
|
|
27 |
1 |
Решение расчетных задач по теме «Растворы» | 8а-
8б-
|
|
|
|
|
|
|
28 |
1 |
Практическая работа № 5 «Приготовление р-ра соли с определенной массовой долей вещества» | 8а-
8б- |
Практичес-кая работа |
| НПХЛ, весы учебные с гирями до 200 г. Таблицы – Техника экспериментальной работы. Взвешивание; Приготовление растворов; Обращение с твердыми веществами. | текущий |
|
|
29 |
1 |
Вода.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Вода - необычное вещество. |
|
|
|
30 |
1 |
Контрольная работа № 2 по темам «Кислород. Горение. Водород. Вода. Растворы»
| 8а-
8б- | Урок контроля, оценки и коррекции знаний учащихся |
|
| текущий |
|
| 31 | 1 | Обобщающий урок по темам «Кислород. Горение. Водород. Вода. Растворы» | 8а-
8б- | Урок обобщения и систематизации знаний |
|
|
|
|
| Основные классы неорганических соединений (16 ч)
|
|
32 |
1 |
Классификация и названия оксидов. | 8а-
8б- | Урок получения и первично го закрепле ния новых знаний | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблицы - Бинарные соединения. Классификация оксидов. |
|
|
|
33 |
1 |
Физические и химические свойства оксидов.
| 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
34 |
1 |
Получение и применение оксидов.
| 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
35 |
1 |
Классификация и названия оснований.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
36 |
1 |
Физические и химические свойства оснований. | 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Кислотность среды. Таблица растворимости веществ. |
|
|
|
37 |
1 |
Получение и применение оснований.
| 8а-
8б-
|
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
38 |
1 | Состав, названия и классификация кислот.
| 8а-
8б-
|
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица - Важнейшие кислоты и их соли. |
|
|
|
39 |
1 |
Физические и химические свойства кислот.
| 8а-
8б-
|
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица растворимости веществ.
|
|
|
|
40 |
1 |
Получение и применение кислот.
| 8а-
8б-
|
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
41 |
1 |
Состав, названия и классификация солей. | 8а-
8б-
|
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблицы - Номенклатура солей; Классификация солей. Важнейшие кислоты и их соли. |
|
|
|
42 |
1 |
Химические свойства солей.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Таблица растворимости веществ. |
|
|
|
43 |
1 |
Получение и применение солей.
| 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
44 |
1 |
Генетическая связь между важнейшими классами неорг-х веществ.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Генетическая связь классов неорганических веществ. |
|
|
|
45
|
1 |
Решение расчетных задач. | 8а-
8б- |
|
|
|
|
|
|
46 |
1 |
Практическая работа № 6 «Решение экспериментальных задач»
| 8а-
8б- |
Практичес кая работа |
| НПХЛ, реактивы Таблицы – Техника экспериментальной работы. Обращение с жидкими веществами; Обращение с твердыми веществами. | текущий |
|
|
47 |
1 |
Контрольная работа №3 по теме «Важнейшие классы неорганических соединений»
| 8а-
8б- | Урок контроля, оценки и коррекции знаний учащихся |
|
| текущий |
|
| Периодический закон и периодическая таблица химических элементов Д.И.Менделеева. Строение атома (6 ч)
|
|
48 |
1 |
Классификация химических элементов.
| 8а-
8б- | Урок получения и первично го закрепле ния новых знаний | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
49 |
1 |
Периодический закон Д.И.Менделеева.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| Таблицы – Форма электромагнитных облаков и последовательность заполнения подуровней электронами; Расположение электронов по орбиталям в атомах первых 20 элементов. |
|
|
|
50 |
1 |
Периодическая таблица химических элементов Д.И.Менделеева. | 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – Периодическая система химических элементов Д.И.Менделеева. |
|
|
|
51 |
1 |
Строение атома.
|
8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| Модель структуры атома. Таблицы-строение атома, Электронная орбиталь, Модели атомов некоторых элементов; Строение атома. Изотопы; Электронные конфигурации атомов. |
|
|
|
52 |
1 |
Строение атома.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана | Модель структуры атома. Таблицы-строение атома, Электронная орбиталь, Модели атомов некоторых элементов; Строение атома. Изотопы; Электронные конфигурации атомов. |
|
|
|
53 |
1 |
Значение периодического закона. Жизнь и деятельность Д.И.Менделеева. | 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
Химическая связь. Строение веществ (6 ч) |
|
54 |
1 |
Электроотрицательность химических элементов.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
|
|
|
|
55 |
1 |
Основные виды химической связи.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – химическая связь; Образование ковалентной и ионной химических связей. |
|
|
|
56 |
1 |
Основные виды химической связи.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
|
Таблица – химическая связь; Образование ковалентной и ионной химических связей. |
|
|
|
57 |
1 |
Кристаллические решетки.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана
| Таблица - Кристаллы; Типы кристаллических решеток. Кристаллическая решетка двуокиси кремния. |
|
|
|
58 |
1 |
Степень окисления.
|
8а-
8б- |
Комбини-рованный
|
Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Таблица – степень окисления. |
|
|
|
59 |
|
Контрольная работа №4 по теме «ПЗ и ПТХЭ Д.И.Менделеева. Строение атома» | 8а-
8б- | Урок контроля, оценки и коррекции знаний учащихся |
|
| текущий |
|
| Закон Авогадро. Молярный объем газов (2 ч) |
|
60 |
1 |
Закон Авогадро.
|
8а-
8б- | Урок получения и первично го закрепле ния новых знаний |
Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
|
|
|
|
61 |
1 |
Объёмные отношения газов при химических реакциях.
| 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
|
|
|
| Галогены (5 ч) |
|
62 |
1 |
Положение галогенов в пер-й таблице и строение их атомов. Хлор.
| 8а-
8б- | Урок получения и первично го закрепле ния новых знаний
|
Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана | Прибор для получения газов лабораторный. Таблица – Техника безопасности при работе с газами. Периодическая система химических элементов Д.И.Менделеева. Техника экспериментальной работы. Получение и собирание газов. |
|
|
|
63 |
1 |
Хлороводород. Соляная кислота и её соли.
| 8а-
8б- |
Комбини-рованный | Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Прибор для получения галоидоалканов и сложных эфиров |
|
|
|
64 |
1 |
Сравнительная характеристика галогенов.
| 8а-
8б- |
Комбини-рованный
| Персональный компьютер, проектор мультимедийный, экран мобильный. DVD Электронное приложение к учеб нику Г.Е.Рудзитиса, Ф.Г.Фельдмана |
Прибор для демонстрации испарения и конденсации. |
|
|
|
65 |
1 |
Практическая работа № 7 «Химические свойства соляной кислоты» | 8а-
8б-
|
Практичес кая работа |
| НПХЛ, реактивы. Таблицы – Техника экспериментальной работы. Обращение с жидкими веществами; Обращение с твердыми веществами. | текущий |
|
|
66 |
1 |
Итоговая контрольная работа
| 8а-
8б- | Урок контроля, оценки и коррекции знаний учащихся |
|
| Промежу точный |
|
|
Заключение (2 ч) |
|
67 |
1 |
Обобщение знаний по курсу химии 8 класса |
8а-
8б- | Урок обобщения и систематизации знаний |
|
|
|
|
|
68 |
1 |
Итоговое повторение | 8а-
8б- | Урок обобщения и систематизации знаний |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Проведено в 8а классе - _____ часов
Проведено в 8б классе - _____ часов
Практических работ- ______
Контрольных работ-______
Требования к уровню достижений обучающихся 8-х классов
В результате изучения химии ученик должен:
Знать:
химическую символику: знаки химических элементов, формулы химических веществ и уравнения химических реакций;
важнейшие химические понятия: химический элемент, атом, молекула, относительные атомная и молекулярная массы, ион, химическая связь, вещество, классификация веществ, моль, молярная масса, молярный объем, химическая реакция, классификация реакций, окислитель и восстановитель, окисление и восстановление;
основные законы химии: сохранения массы веществ, постоянства состава, периодический закон;
Уметь:
называть: химические элементы, соединения изученных классов;
объяснять: физический смысл атомного (порядкового) номера химического элемента, номеров группы и периода, к которым элемент принадлежит в периодической системе Д.И. Менделеева; закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп;
характеризовать: химические элементы (от водорода до кальция) на основе их положения в периодической системе Д.И.Менделеева и особенностей строения их атомов; связь между составом, строением и свойствами веществ; химические свойства основных классов неорганических веществ;
определять: состав веществ по их формулам, принадлежность веществ к определенному классу соединений, типы химических реакций, валентность и степень окисления элемента в соединениях, тип химической связи в соединениях;
составлять: формулы неорганических соединений изученных классов; схемы строения атомов первых 20 элементов периодической системы Д.И.Менделеева; уравнения химических реакций;
обращаться с химической посудой и лабораторным оборудованием;
распознавать опытным путем: кислород, водород; растворы кислот и щелочей, хлорид-ионы;
вычислять: массовую долю химического элемента по формуле соединения; массовую долю вещества в растворе; количество вещества, объем или массу по количеству вещества, объему или массе реагентов или продуктов реакции;
использовать приобретенные знания и умения в практической деятельности и повседневной жизни:
для безопасного обращения с веществами и материалами;
экологически грамотного поведения в окружающей среде;
оценки влияния химического загрязнения окружающей среды на организм человека;
критической оценки информации о веществах, используемых в быту;
приготовления растворов заданной концентрации.
Формирование у учащихся общеучебных умений и навыков
1. Учебно-организационные общеучебные умения и навыки обеспечивают планирование,
организацию, контроль, регулирование и анализ собственной учебной деятельности учащимся.
К ним относятся:
определение индивидуальных и коллективных учебных задач;
выбор наиболее рациональной последовательности действий по выполнению учебной задачи;
сравнение полученных результатов с учебной задачей;
владение различными формами самоконтроля;
оценивание своей учебной деятельности;
постановка целей самообразовательной деятельности.
2. Учебно-информационные общеучебные умения и навыки обеспечивают школьнику
нахождение, переработку и использование информации для решения учебных задач.
К ним относятся:
работа с основными компонентами учебника;
использование справочной и дополнительной литературы;
подбор и группировка материалов по определенной теме;
составление планов различных видов;
владение разными формами изложения текста;
составление на основе текста таблицы, схемы, графика, тезисов: конспектирование;
подготовка доклада, реферата;
использование различных видов наблюдения и моделирования:
качественное и количественное описание изучаемого объекта;
проведение эксперимента.
3. Учебно-логические общеучебные умения и навыки обеспечивают четкую структуру со
держания процесса постановки и решения учебных задач. К ним относятся:
определение объектов анализа и синтеза и их компонентов;
выявление существенных признаков объекта;
проведение разных видов сравнения;
установление причинно-следственных связей;
оперирование понятиями, суждениями;
владение компонентами доказательства;
формулирование проблемы и определение способов ее решения.
4. Учебно-коммуникативные общеучебные умения и навыки позволяют школьнику организовать сотрудничество со старшими и сверстниками, достигать с ними взаимопонимания, организовывать совместную деятельность с разными людьми. К таким навыкам относятся:
выслушивание мнения других;
владение различными формами устных и публичных выступлений;
оценка разных точек зрения;
владение приемами риторики.
Учебно-методическое обеспечение предмета:
учебно-программные материалы:
рабочая учебная программа по химии;
«Программы общеобразовательных учреждений. 8-9 классы. 10-11 классы» Н.Н.Гара, 2010 г.
учебно-теоретические материалы:
учебно-практические материалы:
Список литературы для учителя:
Зуева М.В., Гара Н.Н.; «Школьный практикум. Химия. 8-9 классы»;
Обучение химии. Психолого-методический подход, Санкт-Петербург, «Каро», 2002
«Тематические игры по химии» Методическое пособие для учителя, Творческий центр, Москва, 2004
Хомченко И.Г.; «Сборник задач и упражнений по химии для средней школы»;
Штремпелер Т.И., «Химия на досуге. Домашняя химическая лаборатория», книга для учащихся, Москва, «Просвещение», «Учебная литература», 1996;
CD Уроки химии КиМ (8-9 класс)
СD Химия. 8 класс
СD Открытая химия 2.6
СD Виртуальная химическая лаборатория. 8 класс
СD Электронные уроки и тесты. Химия в школе. Вещества и их превращения
СD Электронные уроки и тесты. Химия в школе. Атом и молекула
СD Электронные уроки и тесты. Химия в школе. Минеральные вещества
СD Электронные уроки и тесты. Химия в школе. Соли
СD Электронные уроки и тесты. Химия в школе. Сложные химические соединения в повседневной жизни
СD Электронные уроки и тесты. Химия в школе. Кислоты и основания
СD Электронные уроки и тесты. Химия в школе. Водные растворы
СD Интерактивные творческие задания. Химия 8-9 кл. Сетевая версия
Список литературы для учащихся:
Аликберова Л.Ю., «Занимательная химия» Москва, «АСТ-ПРЕСС, 2002
Галичкина О.В., «Занимательная химия. Тематические кроссворды» 8-11 класс, Волгоград
Дьячков П. «Тесты по химии 8-11 классы»
«Понятия и определения», химия, словарик школьника, издательский дом «Литера», Санкт-Петербург, 2005
Савина Л.А., «Я познаю мир», детская энциклопедия, химия, Москва, «Астрель», 2002
Хомченко И.Г., «Сборник задач и упражнений по химии для средней школы»;
«Химия: кислоты и основания», пособие для учащихся8-11 классов общеобразовательных учреждений, Москва, «Просвещение», 2000
Штремпелер Т.И., «Химия на досуге. Домашняя химическая лаборатория», книга для учащихся, Москва, «Просвещение», «Учебная литература», 1996
ИНТЕРНЕТ РЕСУРСЫ
http://him.1september.ru - Газета «Химия» и сайт для учителя «Я иду на урок химии»
http://www.chemnet.ru - портал фундаментального химического образования
http://www.alhimik.ru - АЛХИМИК: сайт Л.Ю. Аликберовой
http://www.hemi.nsu.ru - Основы химии: образовательный сайт для школьников и студентов
http://www.chemistry.ru - Химия в Открытом колледже
http://webelements.narod.ru - онлайн-справочник химических элементов
http://belok-s.narod.ru - Белок и все о нем в биологии и химии
http://maratakm.narod.ru - Виртуальная химическая школа
http://all-met.narod.ru - Занимательная химия: все о металлах
http://chem.km.ru - Мир химии
http://www.104.webstolica.ru - Кабинет химии: сайт Л.В. Рахмановой
http://experiment.edu.ru - Коллекция «Естественнонаучные эксперименты»: химия
http://www.chemistry.ssu.samara.ru - Органическая химия: электронный учебник для средней школы
http://school-sector.relarn.ru/nsm/ - Химия для всех: иллюстрированные материалы по общей, органической и неорганической химии
http://chemistry.r2.ru - Химия для школьников: сайт Дмитрия Болотова
http://schoolchemistry.by.ru - Школьная химия
http://rushim.ru/books/books.htm - Электронная библиотека по химии и технике
http://him.1september.ru Газета «Химия»
http://www.elementy.ru/trefil/ - Энциклопедия «Природа науки. 200 законов мироздания»
http://vschool.km.ru - Виртуальная школа Кирилла и Мефодия
http://www.ege.ru - Сайт информационной поддержки Единого государственного экзамена в компьютерной форме
http://www.mon.gov.ru - Министерство образования и науки Российской Федерации
http://www.en.edu.ru - Естественнонаучный образовательный портал
http://www.rusolymp.ru - Всероссийская олимпиада школьников
http://www.eidos.ru/olymp/ - Всероссийские дистанционные эвристические олимпиады
http://www.childfest.ru - Умник: Всероссийский детский интернет-фестиваль
http://unk.future4you.ru - Юность, наука, культура: Всероссийский открытый конкурс исследовательских и творческих работ учащихся
http://www.megabook.ru - Мегаэнциклопедия портала «Кирилл и Мефодий»
http://school-collection.edu.ru/collection/?interface=themcol#45007 - Единая коллекция цифровых образовательных ресурсов
Средства обучения
1.Печатные пособия.
Таблицы:
Периодическая таблица химических элементов Д. И. Менделеева. Портреты ученых.
Учебно-методическое пособие с комплектом таблиц «Номенклатура» (Бинарные соединения; Номенклатура солей; Номенклатура органических соединений; Предельные углеводороды; Непредельные углеводороды; Функциональные производные углеводородов)
Учебно-методическое пособие с комплектом таблиц «Химические реакции» (Брошюра с методическими рекомендациями для педагога; Физические явления и химические реакции; Закон сохранения массы вещества; Классификация химических реакций; Тепловой эффект химической реакции; Окислительно-восстановительные реакции; Электролиз; Генетическая связь классов неорганических веществ; Генетическая связь классов органических веществ)
Учебно-методическое пособие с комплектом таблиц «Химия. 8-9 класс» (Брошюра с методическими рекомендациями для педагога; Валентность; Строение атома, Изотопы; Электронные конфигурации атомов; Образование ковалентной и ионной химических связей; Типы кристаллических решеток; Окислительно-восстановительные реакции; Реакции обмена в водных растворах; Важнейшие кислоты и их соли; Классификация оксидов ; Классификация солей; Генетическая связь важнейших классов неорганических веществ; Кислотность среды; Электролитическая диссоциация; Скорость химических реакций; Химическое равновесие; Классификация органических соединений; Изометрия; Гомология; Нефть-источник углеводородов; Белки)
Учебно-методиическое пособие с комплектом таблиц «Основы химических знаний» (Брошюра с методическими рекомендациями для педагога; Форма электромагнитных облаков и последовательность заполнения подуровней электронами; Расположение электронов по орбиталям в атомах первых двадцати элементов; Вода - необычное вещество; Кривые растворимости некоторых солей в воде; Классификация и свойства оксидов; Окраска пламени; Аллотропия углерода; Электрохимические производства; Производство серной кислоты; Производство аммиака; Гибридизация атомных орбиталей; Химическая связь в органических соединения; Взаимное влияние атомов и групп в молекуле; Пространственная изомерия; Применение алкенов; Бензол; Генетическая связь различных классов углеводородов; Жиры; Моносахариды)
Учебно-методиическое пособие с комплектом таблиц «Инструктивные таблицы» (Брошюра с методическими рекомендациями для педагога; Лабораторное оборудование. Спиртовка; Лабораторное оборудование. Газовая горелка Теклю; Лабораторное оборудование. Электронагреватели; Лабораторное оборудование. Нагревание; Лабораторное оборудование. Лабораторный штатив; Техника экспериментальной работы. Получение и собирание газов; Техника экспериментальной работы. Обращение с твердыми веществами; Техника экспериментальной работы. Обращение с жидкими веществами; Техника экспериментальной работы. Взвешивание; Техника экспериментальной работы. Приготовление растворов; Техника экспериментальной работы. Фильтрование; Техника экспериментальной работы. Перегонка; Техника экспериментальной работы. Титрование)
Дидактические раздаточные карточки «Химия 8-9 класс» (Валентность; Строение атома, Изотопы; Электронные конфигурации атомов; Образование ковалентной и ионной
химических связей; Типы кристаллических решеток; Окислительно-восстановительные реакции; Реакции обмена в водных растворах; Важнейшие кислоты и их соли; Классификация оксидов; Классификация солей; Генетическая связь важнейших классов неорганических веществ; Кислотность среды; Электролитическая диссоциация; Скорость химических реакций; Химическое равновесие; Классификация органических соединений; Изометрия; Гомология; Нефть-источник углеводородов; Белки)
2. Информационно-коммуникационные средства:
DVD Электронное приложение к учебнику;
Мультимедийное учебное пособие нового образца «Химия 9 класс», ЗАО «Просвещение-МЕДИА», 2004;
Мультимедийное учебное пособие «Открытая химия 2.6», ООО «Физикон», 2005;
Электронное издание «Виртуальная химическая лаборатория (9 класс)», МарГТУ,2005;
Электронные уроки и тесты «Водные растворы», ЗАО «Просвещение-МЕДИА», 2005;
Электронные уроки и тесты «Кислоты и основания», ЗАО «Просвещение-МЕДИА», 2005;
Электронные уроки и тесты «Соли», ЗАО «Просвещение-МЕДИА», 2005;
Электронные уроки и тесты «Минеральные вещества», ЗАО «Просвещение-МЕДИА», 2005;
Электронные уроки и тесты «Углерод и его соединения. Углеводороды», ЗАО «Просвещение-МЕДИА», 2005;
Электронные уроки и тесты «Производные углеводородов», ЗАО «Просвещение-МЕДИА», 2005;
Электронные уроки и тесты «Сложные химические соединения в повседневной жизни», ЗАО «Просвещение-МЕДИА», 2005;
СD Уроки химии КиМ (8-9 класс)
3. Технические средства обучения:
компьютер мультимедийный;
мультимедийный проектор;
экран мобильный.
4. Учебно-практическое и учебно-лабораторное оборудование:
1) Приборы, приспособления: комплект посуды для демонстрации опытов по химии (КДОХУ), набор ареометров, аппарат для проведения химических реакций (АПХР), программно-аппаратный комплекс, прибор для опытов по химии с электрическим током (ПХЭ), штатив металлический, термометр спиртовой демонстрационный от 0 до 200° С, спиртовки, аппарат для получения газов Киппа, набор химической посуды и принадлежностей для лабораторных работ, демонстрационный набор для составления объемных моделей молекул, прибор для иллюстрации зависимости скорости химической реакции от условий, прибор для получения растворимых твёрдых веществ (ПРВ), приборы для получения газов (ППГ), кристаллическая решетка двуокиси кремния;
2) Реактивы и материалы: комплект реактивов для базового уровня - наборы - 1C "Кислоты", 3BC "Щелочи", 6C "Органические вещества", 7C "Минеральные удобрения", 9BC "Образцы неорганических веществ", 11C "Соли для демонстрационных опытов", 12BC "Неорганические вещества", 13BC "Галогениды", 14BC "Сульфаты, сульфиты, сульфиды", 16BC "Металлы, оксиды", 17BC "Нитраты" с серебром, 19BC "Соединение марганца", 20BC "Кислоты", 20BC "Кислоты", 22BC "Индикаторы"
5. Натуральные объекты.
Коллекции нефти, каменного угля и продуктов переработки.
КРИТЕРИИ И НОРМЫ ОЦЕНКИ ЗНАНИЙ ОБУЧАЮЩИХСЯ
1. Оценка устного ответа.
Отметка «5»:
ответ полный и правильный на основании изученных теорий;
материал изложен в определенной логической последовательности, литературным языком;
ответ самостоятельный.
Отметка «4»:
ответ полный и правильный на сновании изученных теорий;
материал изложен в определенной логической последовательности, при этом допущены две-три несущественные ошибки, исправленные по требованию учителя.
Отметка «З»:
Отметка «2»:
при ответе обнаружено непонимание учащимся основного содержания учебного материала или допущены существенные ошибки, которые учащийся не может исправить при наводящих вопросах учителя, отсутствие ответа.
2. Оценка экспериментальных умений.
Оценка ставится на основании наблюдения за учащимися и письменного отчета за работу. Отметка «5»:
работа выполнена полностью и правильно, сделаны правильные наблюдения и выводы;
эксперимент осуществлен по плану с учетом техники безопасности и правил работы с веществами и оборудованием;
проявлены организационно - трудовые умения, поддерживаются чистота рабочего места и порядок (на столе, экономно используются реактивы).
Отметка «4»:
Отметка «3»:
работа выполнена правильно не менее чем наполовину или допущена существенная ошибка в ходе эксперимента в объяснении, в оформлении работы, в соблюдении правил техники безопасности на работе с веществами и оборудованием, которая исправляется по требованию учителя.
Отметка «2»:
допущены две (и более) существенные ошибки в ходе: эксперимента, в объяснении, в оформлении работы, в соблюдении правил техники безопасности при работе с веществами и оборудованием, которые учащийся не может исправить даже по требованию учителя;
работа не выполнена, у учащегося отсутствует экспериментальные умения.
3. Оценка умений решать расчетные задачи.
Отметка «5»:
Отметка «4»:
Отметка «3»:
Отметка «2»:
4. Оценка письменных контрольных работ.
Отметка «5»:
Отметка «4»:
Отметка «3»:
Отметка «2»:
При оценке выполнения письменной контрольной работы необходимо учитывать требования единого орфографического режима.
5. Оценка тестовых работ.
оценка «5» - выполнено 100 % тестовых заданий;
оценка «4» - выполнено 75-99 % тестовых заданий;
оценка «З» - выполнено 50-74 % тестовых заданий;
оценка «2» - выполнено менее 49 % тестовых заданий;
6. Оценка реферата.
Реферат оценивается по следующим критериям:
соблюдение требований к его оформлению;
необходимость и достаточность для раскрытия темы приведенной в тексте реферата информации;
умение обучающегося свободно излагать основные идеи, отраженные в реферате;

 Получите свидетельство
Получите свидетельство Вход
Вход











 Программа по химии (8 класс к учебнику Рудзитиса Г.Е.) (0.3 MB)
Программа по химии (8 класс к учебнику Рудзитиса Г.Е.) (0.3 MB)
 0
0 2564
2564 330
330 Нравится
0
Нравится
0



