Программа элективного курса
« Составление химических уравнений»
в рамках предпрофильной подготовки
Пояснительная записка
Программа элективного курса «Составление химических уравнений» предназначена для предпрофильной подготовки учащихся 9-го класса основной школы и рассчитан на 17 часов (1 час в неделю). Курс ориентирован на углубление и расширение знаний, развитие интереса к химии.
В программу включены базовые теоретические вопросы, изучающиеся в курсе основной школы, а также химический эксперимент.
Цель. Развитие навыков и умений составлять уравнения химических реакций.
Задачи. Получение новых знаний в рамках расширения программного материала по химии в 9 классе; отработка навыков составления уравнений химических реакций; отработка практических навыков в процессе выполнения лабораторных работ; развитие познавательного интереса к предмету; формирование умений применять полученные знания в повседневной жизни.
Формы обучения: беседа, лекция, лабораторный опыт, практическая работа.
Формы работы:
1.Индивидуальная (выполнение индивидуальных заданий, лабораторных опытов).
2.Парная (выполнение практических заданий).
3.Коллективная (обсуждение проблем, возникающих по ходу занятий).
В результате изучения элективного курса учащиеся должны знать:
1.Понятие о химической реакции; сущность и механизм протекания; возможность протекания, условия и признаки химических реакций;
2.Классификацию химических реакций по различным признакам: числу и составу исходных и полученных веществ; изменению степеней окисления химических элементов; поглощению или выделению энергии; обратимости;
3.Понятие о скорости химической реакции и факторах, влияющих на скорость реакции;
4.Понятие о химическом равновесии и условиях смещения химического равновесия;
5.Понятие о реакциях ионного обмена и условиях их протекания;
6.Понятие об окислительно- восстановительной реакции; процессы окисления и восстановления; важнейшие окислители и восстановители;
7.Понятие об электролизе; электролиз раствора и расплава;
8.Правила техники безопасности при выполнении химического эксперимента;
учащиеся должны уметь:
1.Составлять уравнения химических реакций различной степени сложности;
2.Проводить расчеты энтальпии, энтропии и энергии Гиббса, скорости химической реакции;
3.Проводить химический эксперимент;
4.Работать в паре, группе;
5.Применять полученные знания и умения в повседневной жизни.
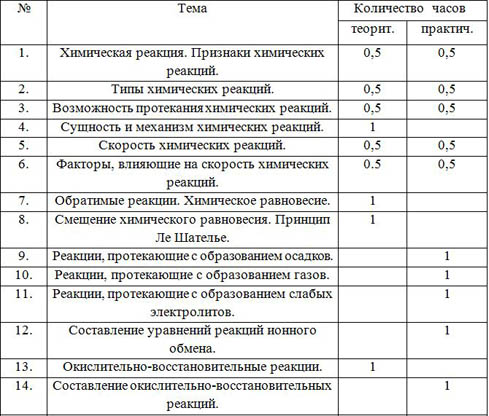
Тематическое планирование
| № | Тема | Количество часов |
| теорит. | практич. |
| 1. | Химическая реакция. Признаки химических реакций. | 0,5 | 0,5 |
| 2. | Типы химических реакций. | 0,5 | 0,5 |
| 3. | Возможность протекания химических реакций. | 0,5 | 0,5 |
| 4. | Сущность и механизм химических реакций. | 1 |
|
| 5. | Скорость химических реакций. | 0,5 | 0,5 |
| 6. | Факторы, влияющие на скорость химических реакций. | 0.5 | 0,5 |
| 7. | Обратимые реакции. Химическое равновесие. | 1 |
|
| 8. | Смещение химического равновесия. Принцип Ле Шателье. | 1 |
|
| 9. | Реакции, протекающие с образованием осадков. |
| 1 |
| 10. | Реакции, протекающие с образованием газов. |
| 1 |
| 11. | Реакции, протекающие с образованием слабых электролитов. |
| 1 |
| 12. | Составление уравнений реакций ионного обмена. |
| 1 |
| 13. | Окислительно-восстановительные реакции. | 1 |
|
| 14. | Составление окислительно-восстановительных реакций. |
| 1 |
| 15. | Электролиз как окислительно-восстановительная реакция. | 1 |
|
| 16. | Составление схем электролиза. |
| 1 |
| 17. | Итоговое занятие. Зачет. |
| 1 |
|
|
Итого | 7,5 9,5 17 часов |
Содержание занятий по программе элективного курса
«Составление химических уравнений».
Тема 1.Химическая реакция. Признаки химических реакций. Лабораторная работа №1 «Признаки химических реакций».
Тема 2. Типы химических реакций. Лабораторная работа №2 «Типы химических реакций».
Тема 3. Возможность протекания химических реакций. Понятие об энтальпии и энтропии реакции. Расчет изменения энергии Гиббса реакции.
Тема 4. Сущность и механизм химических реакций. Понятие об активированном комплексе и энергии активации.
Тема 5. Скорость химических реакций. Гомогенные и гетерогенные реакции. Расчет скорости химической реакции.
Тема 6. Факторы, влияющие на скорость химических реакций. Влияние природы, площади соприкосновения реагирующих веществ, концентрации, температуры на скорость реакции. Понятие о катализаторах и ингибиторах. Лабораторная работа №3 «Факторы, влияющие на скорость химических реакций».
Тема 7. Обратимые реакции. Химическое равновесие. Понятие об обратимых реакциях. Химическое равновесие как динамический процесс.
Тема 8. Смещение химического равновесия. Принцип Ле Шателье. Влияние концентрации реагирующих веществ, температуры и давления на смещение химического равновесия. Решение упражнений на смещение химического равновесия.
Тема 9.Неборатимые реакции. Реакции, протекающие с образованием осадков. Лабораторная работа №4.
Тема 10. Реакции, протекающие с образованием газов. Лабораторная работа №5.
Тема 11. Реакции, протекающие с образованием слабых электролитов. Лабораторная работа №6.
Тема 12. Составление уравнений реакций ионного обмена. Практическое занятие.
Тема 13. Окислительно-восстановительные реакции. Понятие об окислительно-восстановительной реакции. Окисление. Восстановление. Важнейшие окислители и восстановители.
Тема 14. Составление окислительно-восстановительных реакций. Составление окислительно-восстановительных реакций методом электронного баланса. Практическое занятие.
Тема 15. Электролиз как окислительно-восстановительная реакция. Понятие об электролизе растворов и расплавов. Практическое применение электролиза.
Тема 16. Составление схем электролиза. Практическое занятие.
Тема 17. Итоговое занятие. Зачет

 Получите свидетельство
Получите свидетельство Вход
Вход












 Программа элективного курса по химии "Составление химических уравнений" (17.07 КB)
Программа элективного курса по химии "Составление химических уравнений" (17.07 КB)
 0
0 441
441 52
52 Нравится
0
Нравится
0


