
Кислоты
Основные классы неорганических соединеНИЙ

Разделите и запишите вещества в три колонки:
- H 2 S, Al(OH) 3, H 2 SO 4 , P 2 O 5 , HCL, NaOH, Al 2 O 3 , HNO 3 , BaO, H 3 PO 4 , CO 2 .
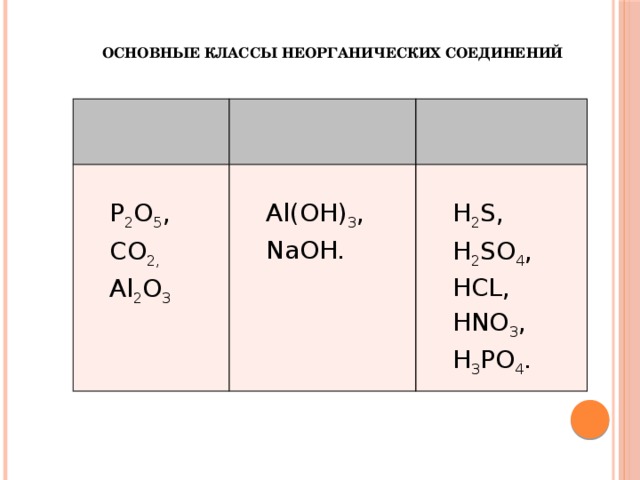
Основные классы неорганических соединеНИЙ
P 2 O 5 ,
CO 2,
Al(OH) 3 ,
Al 2 O 3
NaOH.
H 2 S, H 2 SO 4 , HCL, HNO 3 , H 3 PO 4 .

КИСЛОТЫ

-
КИСЛОТЫ: МУРАВЬИНАЯ - ЛИМОННАЯ - ЯБЛОЧНАЯ -МОЛОЧНАЯ -УГОЛЬНАЯ - СОЛЯНАЯ

Кислоты в дождевой воде
Азотная кислота может находиться
в дождевой воде после грозы.
В Астраханской области происходят постоянные выбросы в атмосферу окислов серы и азота, но в первую очередь сернистого газа, так как именно серная кислота и ее соли на 70—80% обусловливают кислотность дождей, выпадающих на больших расстояниях от места промышленного выброса.

Кислоты в растительном мире
Лишайники выделяют кислоты,
которые разрушают
горные породы
Мухоморы в качестве ядовитых токсинов «используют» иботеновую кислоту. Это вещество так ядовито, что мухомору незачем прятаться.
Очень популярен в народе щавель,
который содержит щавелевую кислоту

Кислоты в животном мире
Голожаберные моллюски в порядке самообороны выстреливают парами серной кислоты
Тропический паук педипальпида
стреляет во врагов струйкой жидкости,
содержащей 84% уксусной кислоты .
Кислоты в организме человека
Соляная кислота в желудке помогает переваривать пищу.
Аминокислоты в организме, соединяясь, образуют белки. А без белков нет ни мышц и ни кожи,

Правила техники безопасности
- 1) Выполнять все указания учителя,
- 2) Не пробовать вещества на вкус
- 3) Пробирку в руки не брать
- 4) Не приступать к выполнению опыта, не зная, что и как нужно делать
- 5)Обращаться с лабораторной посудой бережно и закончив работу, привести рабочее место в порядок.

Обсуждение результатов и формулирование выводов:
- Как можно определить раствор кислоты среди других веществ?
- Какие индикаторы изменили свой цвет в кислотах?
- Одинаковые ли изменения цвета этих индикаторов вы наблюдали в обеих кислотах?
- Какую окраску приобрели лакмус и метилоранж и в соляной, и в лимонной кислотах?
- На основании проведенных опытов сделаем выводы:

Выводы:
- Независимо от вида кислот индикаторы изменяют свой цвет одинаково;
- А это означает, что все кислоты обладают сходными свойствами.
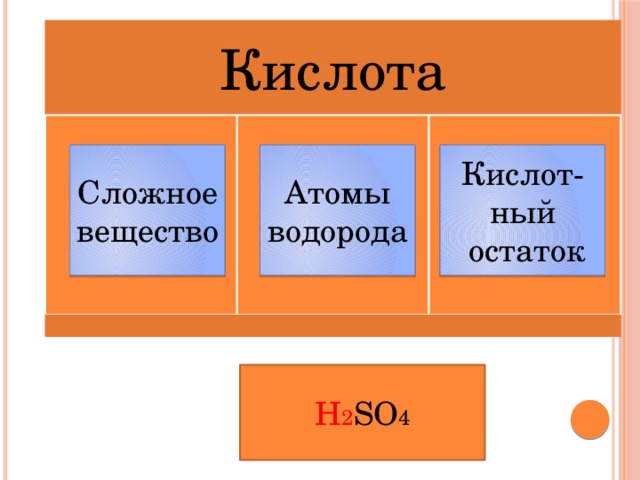
Кислота
Сложное
Атомы
Кислот-ный
вещество
водорода
остаток
H 2 SO 4
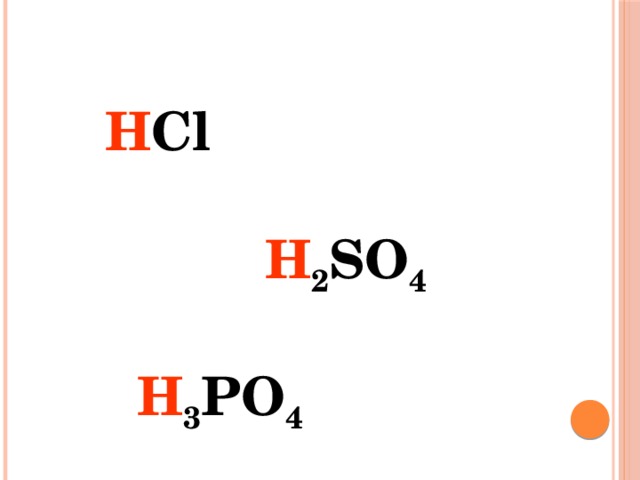
H Cl
H 2 SO 4
H 3 PO 4
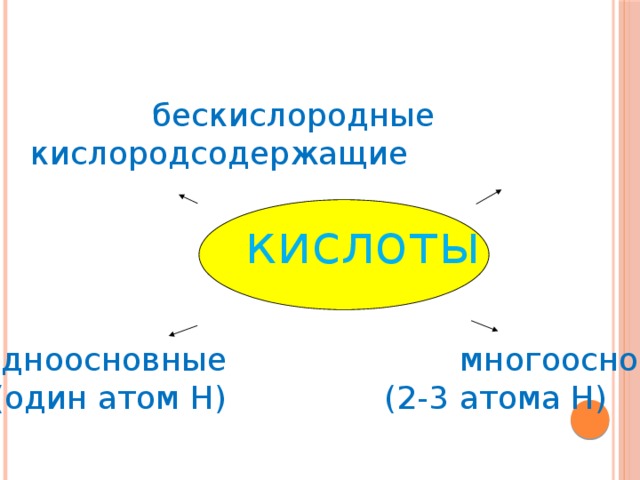
бескислородные кислородсодержащие
кислоты
одноосновные многоосновные
(один атом Н) (2-3 атома Н)

Дан «текст», в котором «спрятаны» формулы кислот. Подчеркните их.
Na 2 OH 2 CO 3 Mg(OH) 2 BaSO 4 SO 2 HСIАI(OH) 3 KNO 3 MgOH 3 PO 4 HNO 3 Na 2 SLi 2 SO 4 AI 2 O 3 Ca(OH) 2

Правильный ответ - 4 кислоты
Na 2 O H 2 CO 3 Mg(OH) 2 BaSO 4 SO 2 HСI АI(OH) 3 KNO 3 MgO H 3 PO 4 HNO 3 Na 2 SLi 2 SO 4 AI 2 O 3 Ca(OH) 2


 Получите свидетельство
Получите свидетельство Вход
Вход





























 Презентация к уроку химии на тему "Кислоты" (3.33 MB)
Презентация к уроку химии на тему "Кислоты" (3.33 MB)
 0
0 581
581 56
56 Нравится
0
Нравится
0


