
Итоговое тестирование

1. Углеводород С 9 Н 12 относится к классу:
а) алканы б) алкены в) арены г) алкины
2. Тип гибридизации атомов С в ацетилене:
а) sp 3 б) sp 2 в) sp г) sp 3 d 2
3. Длина связи С - С в молекуле этана, нм:
а) 0,154 б) 0,140 в) 0,120 г) 0,134
4. Углеводород 2,2-диметилпентан имеет молярную массу, г/моль:
а) 98 б) 100 в)102 г) 104
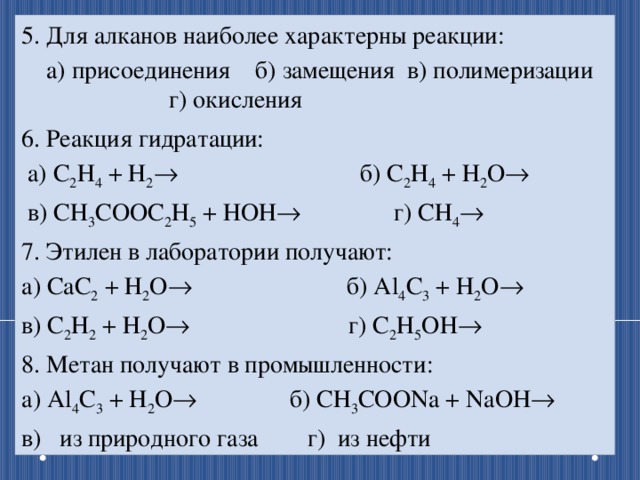
5. Для алканов наиболее характерны реакции:
а) присоединения б) замещения в) полимеризации г) окисления
6. Реакция гидратации:
а) С 2 Н 4 + Н 2 б) С 2 Н 4 + Н 2 О
в) СН 3 СООС 2 Н 5 + НОН г) СН 4
7. Этилен в лаборатории получают:
а) СаС 2 + Н 2 О б) Al 4 C 3 + H 2 O
в) С 2 Н 2 + Н 2 О г) С 2 Н 5 ОН
8. Метан получают в промышленности:
а) Al 4 C 3 + H 2 O б) СН 3 СООNa + NaOH
в) из природного газа г) из нефти

9. Наибольшая массовая доля углерода в соединении:
а) С 2 Н 2 б) С 2 Н 6 в) С 2 Н 4 г) С 2 Н 5 ОН
10. Объём воздуха, необходимый для сжигания 2 литров пропана, л:
а) 10 б) 20 в) 50 г) 100
11. Углеводород, содержащий тройную связь:
а) С 4 Н 6 б) С 4 Н 8 в) С 4 Н 10 г) СН 4
12. Толуол является представителем гомологического ряда:
а) фенола б) метанола в) бензола г) стирола
13. Гомологами являются:
а) этан и этилбензол б) циклобензол и толуол
в) бензол и толуол г) метилбензол и метанол

14. Электронная конфигурация наружного электронного слоя атома углерода в возбужденном состоянии:
а) 3s 2 3p 2 б) 2s 2 2p 2 в) 3s 1 3p 3 г) 2s 1 2p 3
15. Следующие признаки: sp 2 -гибридизация, длина углерод-углеродной связи 0,134нм, угол связи 120° характерны для молекулы:
а) бензола б) этана в) этина г) этена
16. Название вещества, формула которого
СН 3 – СН – С ≡ С – СН 3
а) 2-метилпентин-3 б) 2-метилпентин-4
в) 2-метилпентин-2 г) 4-метилпентин-2

17. Объём углекислого газа (н. у.), полученный при спиртовом брожении 5 моль глюкозы, л:
а) 2,24 б) 22,4 в) 224 г) 2240
18. Для получения этилового эфира муравьиной кислоты необходимо взять:
а) СН 3 СООН и С 2 Н 5 ОН б) НСООН и СН 3 ОН
в) СН 3 СООН и СН 3 ОН г) НСООН и С 2 Н 5 ОН
19. Углеводород, содержащий тройную связь:
а) С 4 Н 6 б) С 4 Н 8 в) С 4 Н 10 г) СН 4
20. Вещество, которое можно обнаружить по запаху: а) С 2 Н 4 О 2 б) С 3 Н 8 О 3 в) СН 3 СООН г) С 6 Н 12 О 6


 Получите свидетельство
Получите свидетельство Вход
Вход


















 Подготовка итоговому тестированию по химии (74.08 КB)
Подготовка итоговому тестированию по химии (74.08 КB)
 0
0 1273
1273 97
97 Нравится
0
Нравится
0


