Задачи:
- формировать знания учащихся о положении кремния в периодической таблице, его строении и свойствах, распространении в природе и применении, распространении в природе диоксида кремния, его свойствах и применении;
- развивать логическое мышление, умение делать выводы, правильно записывать уравнения химических реакций;
- воспитывать аккуратность, целеустремленность и необходимость в приобретении знаний;
Оборудование: таблица «характеристика кремния и диоксида кремния»,
Ход урока
Орг. момент /сообщение темы и задач урока/
Объяснение новой темы /рассказ учителя с элементами беседы и составление таблицы/
Таблица «Свойства кремния и диоксида кремния» - смотри документ
Кремний занимает 2 место после кислорода. Встречается только в виде соединений в виде оксидов и силикатов, образует множество горных пород и минералов / полевые шпаты, глина, слюда, тальк, песок.
Кристаллический SiO2, окрашенный различными примесями, образует драгоценные камни – агат, аметист, яшма.
Диоксид кремния входит в состав некоторых организмов /морские растения диатомовые водоросли и инфузории/.
Кремнезем – природный полимер.
Кремний применяют в солнечных батареях, приборостроении, для получения чистых Ме в металлургии, для изготовления фотоэлементов, получают жаро- и кислотостойкие стали.
Диоксид кремния применяют, как основное сырье для получения соединений кремния, в строительстве, в производстве стекла, цемента, керамики.
Na2SiO3 + H2SO4 = H2 SiO3 + Na2 SO4
Кремниевая кислота очень слабая и малоустойчивая, при нагревании легко разлагается на воду и оксид кремния.
H2 SiO3 = H2O + SiO2
Двухосновная, поэтому диссоциирует ступенчато:
H2 SiO3 = H+ + НSiO3-
НSiO3- = H+ + SiO32-
Стеклами называют прозрачные аморфные сплавы силикатов натрия и калия с кремнеземом.
а) Оконные стекла: в качестве сырья используют известняк - CaCO3, сода - Na2CO3, песок - SiO2.
Все эти вещества плавят в особых печах при темп. 1400 0С, называется варкой стекла.
б) тугоплавкое стекло - используется для изготовления химической посуды, приборов, оно выдерживает сильное нагревание. При его получении соду заменяют поташом К2СО3.
в) боросиликатное стекло – особо стойкое - для особо стойкой химической посуды / для его получения часть белого песка заменяют оксидом бора ( III) В2О3.
г) хрустальное стекло - обладает лучепреломляющей способностью и при шлифовке приобретает сильный блеск.
д) цветное стекло :
СоО и СuO - стекло синего цвета;
Cr2O3 - зеленого;
FeO – бледно-желтого;
TiO2 – белого;
Fe2O3 – желто-зеленого;
Se – красноватое
Недостаток стекла – хрупкость
По новой технологии изготавливают стекла, близкие по прочности к чугуну – ситаллы, которые получают быстрой кристаллизацией стекла в процессе варки.
Цемент - связывающий материал.
Силикатоцемент – обычный цемент, получаемый путем обжига смеси глины с известняком.
CaO x Al2O3 x SiO2
Обычный цемент получают, смешивая 25% известняка и 75 % глины. При смешивании цемента с песком получают цементный раствор, который на воздухе -затвердевает.
Бетон - получают, смешивая цементного раствора и гравия или щебня.
Железобетон- цемент плюс стальная арматура.
Закрепление
- Написать формулы соединений кремния, соответствующие степеням его окисления: -4, +2, +4. Назвать вещества.
- Что является сырьем силикатной промышленности?
- Как получают цветные стекла?
- Для чего применяют цемент, бетон, железобетон?
Домашнее заданий § 6.5,6.6
Итог урока, выставление оценок.

 Получите свидетельство
Получите свидетельство Вход
Вход



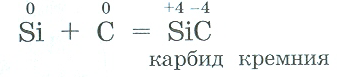
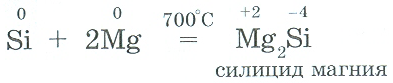
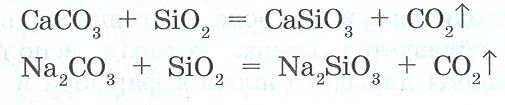










 Кремний и его соединения (0.67 MB)
Кремний и его соединения (0.67 MB)
 0
0 1171
1171 67
67 Нравится
0
Нравится
0





