Цели урока: обобщить знания по разделу «углеводороды» и ознакомить учащихся с новым разделом - кислородсодержащие органические вещества на примере производных углеводородов – одноатомных спиртов, в молекулах которых содержится –ОН группа. Объяснить влияние функциональной группы на свойства спиртов, рассмотреть строение, влияние имеющихся между молекулами спиртов водородных связей на физические свойства спиртов, изомерию и номенклатуру спиртов, провести анализ взаимного влияния атомов в молекулах спиртов.
Оборудование и реактивы: Этанол, бутанол, Na, шаростержневые модели молекул метанола и этанола, интерактивная доска, презентация PowerPoint
Тип урока: комбинированный с элементами игры
Формы учебной работы: фронтальная, индивидуальная
Методы обучения: словесные, наглядные, практические, информационно-развивающие, репродуктивные
Ход урока
- Организационный момент
- Обобщение по разделу «Углеводороды»
- «Углеводородный марафон» – проводится по типу телевизионной игры «Своя игра». Учащийся выбирает вопрос из любого раздела и любой стоимости, за правильный ответ получает фишку со стоимостью вопроса. В конце опроса подсчитывается набранная сумма и выставляются оценки за фронтальный опрос.
Алканы
10 - Назовите общую формулу алканов (Сn H2n+2)
20 - Под каким углом соединятся атомы в молекулах предельных углеводородов? (109 °28')
30 - Как еще называют алканы и почему? (предельные, насыщенные, парафины)
40 – Почему метан часто называют природным и «болотным» газом? (Его содержание в природном газе достигает до 90-98%, образуется в природе в результате разложения остатков растительных и животных организмов без доступа воздуха. Этим объясняется появление пузырьков газа в заболоченных водоемах)
50- Напишите реакцию горения метана( СН4+2О2→ СО2+2Н2О)
Циклоалканы
10- Как еще можно назвать циклоалканы? ( Циклопарафины или нафтены, они главным образом находятся в составе некоторых нефтей, поэтому нафтены)
20- Назовите общую формулу циклоалканов. (Сn H2n)
30 – Назовите формулу циклопропана (С3Н6)
40 – этот циклоалкан - легкокипящая жидкость, применяется в медицине для наркоза (циклопропан)
50 – Как образуются названия циклоалканов? Приведите пример (Названия циклоалканов образуются путем добавления приставки цикло - к названию соответствующего алкана, например: пропан – циклопропан, бутан - циклобутан)
Алкены
10 – Какие углеводороды называют алкенами? (Углеводороды, в молекулах которых имеется одна двойная связь)
20 - Связь, образующаяся вне плоскости атомных ядер, называют… (пи связью)
30 – Назовите три гомолога этилена (пропилен, бутилен, амилен)
40 - Алкен имеет следующее строение. Дайте ему название
СН3 – СН - С = СН2
½ ½
СН3 СН3 (2,3 – диметилбутилен-1)
50- Что получается при реакции полимеризации этилена? (Полиэтилен)
Алкадиены
10 –Общая формула алкадиенов (Сn H2n-2)
20 -Как еще называют алкадиены? (Диеновыми углеводородами, что говорит о двух двойных связях в молекуле)
30 – В алкадиенах взаимное расположение двойных связей может быть различным. Если две двойные связи расположены рядом, как называется такая связь? (Кумулированная – две двойные связи расположены рядом)
40 – диены легко вступают в реакции полимеризации. В результате реакции полимеризации бутадиена-1,3 (дивинила) что образуется? (Это мономер для получения синтетического каучука)
50 – Назовите фамилию ученого, который получил впервые синтетический каучук полимеризацией бутадиена -1,3 в 1928 году. (Лебедев Сергей Васильевич)
Алкины
10- Чему равен валентный угол в молекулах алкинов? (180°)
20- Назовите общую формулу алкинов (Сn H2n-2)
30-Ацетилен можно получить карбидным способом. Запишите реакцию (СаС2 + 2Н2О → С2Н2 + Са (ОН)2)
40 - Гомолог ацетилена, имеющий 8 атомов водорода имеет формулу… (С5Н8)
50 - При горении ацетилена выделяется большое количество тепла. Для чего используют это свойство? (Для резки и сварки металлов)
Арены
10 – Напишите молекулярную и структурную формулы бензола (С6Н6)
20 - Какие углеводороды называют аренами? (Углеводороды, в молекулах которых имеется бензольное кольцо)
40 – Назовите гомолог бензола, который идет на получение тротила? (толуол)
50 - Какие типы химических реакций характерны для бензола? (присоединения, замещения)
- Объяснение новой темы.
Вступительное слово учителя:
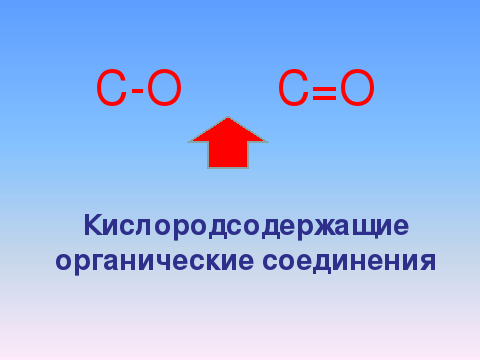
До сих пор мы изучали органические соединения, состоящие только из двух элементов – углерода и водорода. Теперь рассмотрим кислородсодержащие органические вещества, молекулы которых состоят из трех элементов – углерода, водорода, кислорода. Соединения, в составе которых имеются С-О- и С=О –связи, являются важными производными углеводородов. Они образуются в результате окисления углеводородов.
Определение в тетрадь:
Соединения, функциональные группы которых содержат кислород, называют кислородсодержащими органическими соединениями.
К кислородсодержащим органическим соединениям относятся спирты, фенолы, альдегиды и кетоны, карбоновые кислоты, простые и сложные эфиры, углеводы, жиры.
Схема № 1 (проецируется на доске) слайд №2
Сегодня мы начнем знакомство с первым классом кислородсодержащих веществ, с которыми люди знакомы с глубокой древности. Эти вещества образуются при ферментативном окислении винограда, сахара, крахмала. Название этого класса – спирты происходит от латинского слова «дух вина». А с XVIII века наряду со словом «спирт» употребляется и другое их название – «алкоголь» (по- арабски – «ал-кугул»), что означает «одурманивающий».
Это и есть тема сегодняшнего урока: Насыщенные одноатомные спирты, их состав, строение, изомеры.
После объявления темы урока и записи ее в тетради, учитель объявляет этап урока «Ожидание» (высвечивается на интерактивной доске) (слайд№3)
«Ожидание»- учитель предлагает учащимся сформулировать свои ожидания от заявленной темы, тем самым определятся цели урока. Учащиеся должны высказать свои предложения по поводу того, что они хотят узнать по данной теме. Высказывания записываются на доске. После чего вся информация обобщается и озвучиваются цели урока (выводятся на интерактивную доску)
Чтобы вывести формулу спирта, давайте решим задачу на вывод молекулярной формулы
Решение задачи у доски (1 учащийся)
Задача слайд №4
Вывести молекулярную формулу кислородсодержащего органического соединения по следующим данным: массовая доля углерода-52,17%, массовая доля водорода -13,05%, массовая доля кислорода – 34,78%
Зная валентность химических элементов и пользуясь положением теории А.М. Бутлерова, что атомы в молекулах соединяются не беспорядочно, а в строгой последовательности, согласно их валентности, составим структурную формулу выведенного вещества. слайд №7
1) Н Н 2) Н Н
| | | |
Н – С – С – О – Н Н – С – О – С - Н
| | | |
Н Н Н Н
Сопоставляя эти две формулы, задаемся вопросом, какая же из этих двух формул отвечает строению этилового спирта?
В 1 –ой формуле один атом водорода соединен с углеродом через атом кислорода, т.е. он находится в особом положении, он менее прочно связан с атомом углерода, следовательно, может легко отщепляться и замещаться другими атомами. Доказательством служит взаимодействие этилового спирта с натрием. Идет бурное выделение водорода. (Демонстрация реакции). Экспериментально доказано, что из 1 Моль спирта натрий может вытеснить 0,5 Моль водорода, или же из молекулы спирта металл вытесняет один атом водорода. Какой?
Во второй формуле все 6 атомов водорода равноценны, они непосредственно не соединены с кислородом.
А вот в первой формуле один из 6 атомов водорода вместе с кислородом образует гидроксильную –ОН группу. Такой атом весьма активен, следовательно, его может вытеснять атом металла. Поэтому истинной формулой для этилового спирта является первая формула. Эту формулу можно записывать следующим образом:
СН3-СН2-ОН или С2Н5ОН
То есть мы вывели формулу кислородсодержащего органического вещества. Известно много веществ, в состав которых наряду с С и Н входит и О. Рассмотрим прежде всего класс спиртов.
Что же значит спирт с точки зрения химии? Какие органические вещества мы будем называть спиртами?
Определение в тетрадь
слайд № 8
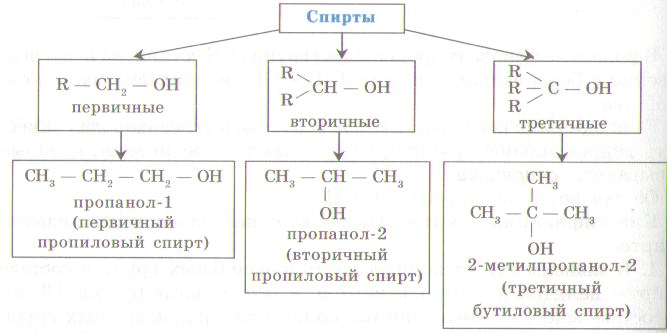
- Классификация спиртов слайды 9,10,11
Существует несколько видов делений спиртов:
1. В зависимости от количества гидроксильных групп спирты бывают одноатомные и многоатомные;
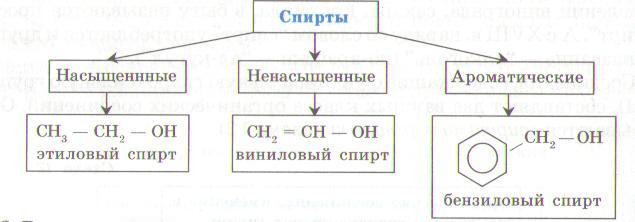
2. В зависимости от углеводородного радикала, связанного с гидроксильной группой, спирты делятся на насыщенные, ненасыщенные, ароматические.
3. В зависимости от природы атома углерода, связанного с гидроксильной группой, спирты делятся на первичные, вторичные, третичные.
2. Изомерия, номенклатура.
По систематической номенклатуре названия спиртов образуют от названий соответствующих предельных углеводородов с добавлением суффикса – ол. Составим гомологический ряд предельных одноатомных спиртов
слайд №12
Общая формула спиртов R- ОН или CxHy(OH)n.
Цифрой обозначают номер углеродного атома, который удерживает гидроксильную группу. Нумерацию углеродного скелета начинают с того конца, к которому ближе гидроксильная группа. Слайд №13
4 3 2 1
СН3-СН2-СН2 – СН2 – ОН бутанол – 1
4 3 2 1
СН3-СН2-СН – СН2 – ОН 2-метилбутанол-1
|
СН3
СН3
|
СН3-СН2-С – СН2 – ОН 2,2 – диметилбутанол -1
|
СН3
ОН
|
СН3-СН-СН – СН2 –СН3 3-метилпентанол-2
|
СН3
СН3
СН3-С - СН – СН2 –СН3 2,2-диметилпентанол - 3
| |
СН3 ОН
Изомерия спиртов обусловлена как углеродным скелетом, так и положением гидроксильной группы в углеродной цепи. Кроме того, для алканолов характерна межклассовая изомерия.
Пример межклассовой изомерии: слайд № 16
С4Н10О
СН3-СН2-СН2 – СН2 – ОН СН3-СН2 – О - СН2 - СН3
бутанол – 1 диэтиловый эфир (простой эфир)
Задание группе – Дайте названия следующим веществам слайд № 17
А) СН3-СН2-СН2 – ОН
Б) СН3-СН2-СН – СН3
|
ОН
В) СН3-СН-СН2 – ОН
|
СН2 – СН3
СН3
|
Г) СН3 – СН - С – СН2 - СН3
| |
С2Н5 ОН
СН3
|
Д) СН3-СН2 - С – ОН
| |
СН3 СН3
Задание группе – Напишите структурные формулы спиртов: слайд №18
А) 2,3 – диметилбутанол – 2
Б) 3,3- диметилбутанол – 2
В) 2,3,4 – триметилпентанол – 2
3. Физические свойства спиртов
Низшие и средние члены гомологического ряда (С1-С11) – жидкости. Высшие спирты от С12 – мазеобразные вещества, С21 - твердые вещества. Метанол, этанол, пропанол смешиваются с водой в любых соотношениях. Низшие спирты имеют характерный алкогольный запах и жгучий вкус. Все спирты легче воды. Средние спирты (С4-С6) имеют неприятный (удушливый) запах, высшие спирты лишены запаха. С возрастанием относительной молекулярной массы уменьшается растворимость жидких спиртов в воде, высшие спирты в воде практически не растворимы. Спирты линейной структуры кипят при более высокой температуре, чем спирты с разветвленным углеродным скелетом. То есть с увеличением числа атомов в углеводородном радикале и соответственно молекулярной массы изменяется и плотность, растворимость в воде, температура кипения и агрегатное состояние.
Например, жидкое состояние спиртов, высокие температуры кипения объясняются способностью молекул к ассоциации – объединению за счет возникновения между ними дополнительной ВОДОРОДНОЙ связи. Слайд № 22. Появление водородной связи обусловлено наличием полярной группы – ОН. Атом Н+ одной молекулы притягивает О- другой молекулы. Водородная связь менее прочная в 10-15 раз. (по сравнению с сигма-свяью). Однако чтобы разорвать такую связь между молекулами, необходимо затратить дополнительную энергию. Это и обусловливает высокую температуру кипения спиртов.
Еще с увеличением молекулярной массы в гомологическом ряду спиртов усиливается токсичность одноатомных спиртов. Если сравнить этиловый и амиловый спирты, то молекулярная масса последнего возрастает в 2 раза. А токсичность – в 20 раз. Спирты, содержащие 3-5 атомов углерода, образуют сивушные масла, наличие которых в спиртных напитках увеличивает их ядовитые свойства. В этом ряду исключением является метанол – сильный яд, поражающий нервную систему. При попадании в организм 1-2 чайные ложки метилового спирта поражается зрительный нерв, что приводит к полной слепоте, 30-100 мл влечет за собой смертельный исход.
Растворимость спиртов зависит от углеводородного радикала: с увеличением его длины растворимость уменьшается, т.к. увеличивается неполярная часть молекулы.
Историческая справка! Историческое название метанола - древесный спирт. Получают перегонкой твердых пород дерева. При попадании в организм превращается в формальдегид и муравьиную кислоту. Повреждает сетчатку глаза, вызывает гибель зрительного нерва, что приводит к полной потере зрения. 50 мл метанола – вызывает смерть
III.Закрепление
- Какие органические вещества называют спиртами?
- Объясните, чем обусловлена высокая химическая активность атома водорода в гидроксильной группе?
- В чем отличие водородной связи от δ – связи?
- Какие виды изомерии характерны для спиртов?
- Рефлексия. Заполните листы рефлексии – смотри документ.
- Задание на дом:
§ 8.1, 8.2 стр.161- 163 по учебнику «Химия 11» А. Темирбулатова, Н. Нурахметов и др. Используя дополнительную литературу, подготовить материал об отдельных представителях спиртов и их применение.

 Получите свидетельство
Получите свидетельство Вход
Вход


 слайд №1
слайд №1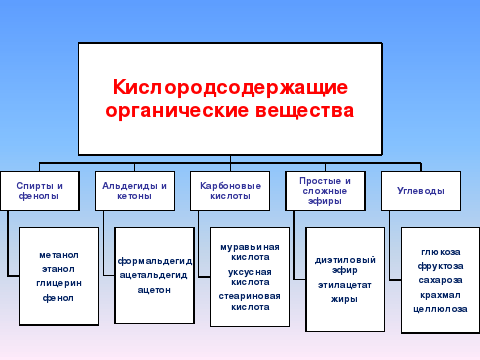

 слайд № 8
слайд № 8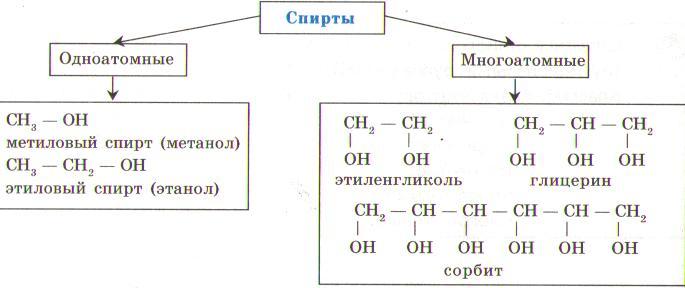
 слайд №12
слайд №12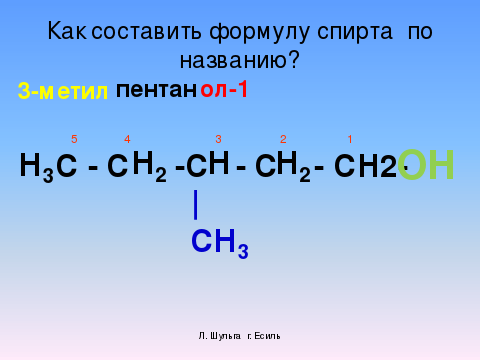 слайд №14
слайд №14 слайд №15
слайд №15








 Кислородсодержащие органические соединения. Спирты (0.63 MB)
Кислородсодержащие органические соединения. Спирты (0.63 MB)
 0
0 3567
3567 205
205 Нравится
0
Нравится
0




