Многие вещества, которые нас окружают, мы можем определить по их специфическим признакам и свойствам. Например, алюминий несложно отличить от других металлов. Он легче, также легко изменяет свою форму, при трении о бумагу или белую ткань оставляет серую полосу. Медь – металл красного цвета, имеет металлический блеск, хорошо проводит электрический ток, поэтому медь применяют при изготовлении проводов.
Такие жидкости, как уксусная кислота и этиловый спирт, также легко отличить. У каждого из вас дома наверняка есть уксусная кислота. Определить её вы можете по специфическому резкому запаху. Уксусная кислота очень хорошо растворима в воде. Этиловый спирт имеет характерный запах и хорошо смешивается с водой.
Кристаллы медного купороса имеют синий цвет, легко растворяются в воде, образуя голубой раствор. У всех у вас в аптечке есть марганцовка, её также несложно отличить. Марганцовка представляет собой тёмно-фиолетовые кристаллы, которые хорошо растворяются в воде и образуют раствор ярко-розового цвета.
Однако многие вещества распознать достаточно сложно. Как распознать кислород и углекислый газ, ведь эти газы бесцветны и не имеют запаха? Или как узнать, какое вещество находится в пробирке: раствор кислоты или соли? Какой газ находится в сосуде? Для этого проводят химические реакции, в результате которых происходят изменения с веществами. Эти специфические признаки мы можем определить с помощью наших органов чувств: зрения, обоняния, слуха. Такие химические реакции называются качественными.

То есть качественные реакции – это химические превращения, сопровождающиеся характерными признаками, с помощью которых проводят распознавание веществ.
Основными признаками химических реакций являются: изменение окраски, выпадение осадка, выделение газа, появление запаха, выделение тепла и света.
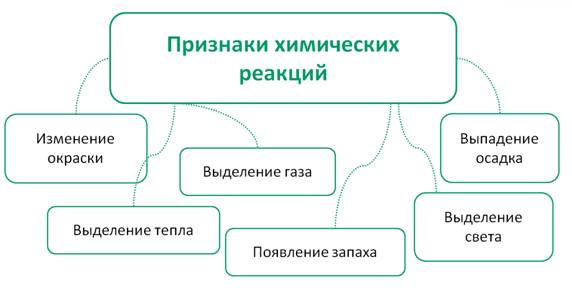
Такие явления при проведении качественных реакций называются аналитическими сигналами.
Если опустить тлеющую лучинку в пробирку с кислородом и углекислым газом, то в одной пробирке лучинка гаснет, а в другой – ярко вспыхивает. Этот опыт позволяет определить, в какой пробирке кислород, а в какой – углекислый газ. В той пробирке, где лучинка гаснет, находится углекислый газ, так как углекислый газ не поддерживает горение. В той пробирке, где лучинка вспыхнула, находится кислород, потому что кислород поддерживает горение.

А как отличить, например, углекислый газ от азота, ведь азот, как и углекислый газ, не поддерживает горение? Для этого существует качественная реакция на углекислый газ.
Если в стакан с углекислым газом добавить небольшое количество известковой воды и встряхнуть жидкость в стакане, то жидкость мутнеет. Таким образом, с помощью известковой воды, или раствора гашёной извести, можно обнаружить углекислый газ.
Если в пробирку с прозрачной известковой водой опустить стеклянную трубку и продуть через неё выдыхаемый воздух, то раствор мутнеет. Значит, и в выдыхаемом воздухе есть углекислый газ.

То есть вещество, с помощью которого проводят качественную реакцию, называется реактивом на определяемое вещество.
В нашем случае известковая вода является реактивом на углекислый газ и углекислый газ является реактивом на известковую воду.
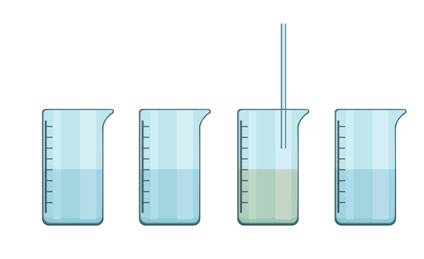
Проведём небольшой эксперимент. В четырёх стаканах у нас находятся: вода, раствор поваренной соли, раствор сахара и известковая вода. Определим, в каком стакане известковая вода. Для этого нужно пропустить через жидкость в каждом стакане выдыхаемый воздух, который обогащён углекислым газом. В третьем стакане появилось помутнение, значит, здесь находится известковая вода.
Чтобы реакцию можно было считать качественной, аналитический сигнал на определённый реактив должен появляться только при взаимодействии с одним или немногими веществами. В противном случае трудно будет сделать вывод о том, какое вещество мы обнаружили с помощью реактива.
Например, крахмал можно обнаружить с помощью раствора йода и наоборот. Если капнуть несколько капель йодной настойки на кусочек картофеля, то наблюдается появление сине-фиолетовой окраски. Данная реакция является качественной на крахмал и подтверждает наличие крахмала в картофеле.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 6848
6848