Урок
Тема: Основания: состав, названия, классификация, физические свойства. Щелочи. Химические свойства оснований. Получение оснований.
Цель: Тип урока: Урок открытия нового знания.
Содержательная цель учителя:
Способствовать усвоению материала, сформировать представление об основаниях, их составе, классификации, физических и химических свойствах, получении и применении.
Деятельностная цель: формирование у учащихся умения реализации новых способов действия, связанных с поиском и выделением информации, а также с прогнозированием результатов своей деятельности, формирование ключевых компетенций учащихся информационной (умение анализировать информацию и переводить её из одной формы в другую), проблемной и коммуникативной.
Планируемые результаты:
Предметные: Сформировать представление об основаниях, способствовать усвоению материала о их строении, роли оснований в жизни человека. Сформировать умение составлять формулы оснований, давать им названия; продолжить формирование навыков составления уравнений химических реакций; рассмотреть химические свойства оснований; сравнить химические свойства оснований, сравнить химические свойства растворимых и нерастворимых оснований; рассмотреть правила техники безопасности при работе с кислотами
Метапредметные:
Регулятивные: самостоятельно находить выход из нестандартных ситуаций, составлять план и последовательность действий, вносить коррективы и дополнения в способы своих действий в случае расхождения с эталоном реального действия и его продукта; организовывать свою деятельность, определять её цели и задачи, выбирать средства реализации цели и применять их на практике, оценивать достигнутые результаты.
Познавательные: осуществлять поиск и выделение необходимой информации, проводить анализ способов решения задачи с точки зрения их рациональности и экономичности; формировать и развивать посредством химических знаний познавательные интересы, интеллектуальные и творческие способности; вести самостоятельный поиск, анализ, отбор информации, её преобразование, сохранение, передачу и презентацию.
Коммуникативные: самостоятельно организовывать учебное взаимодействие в группе (определять общие цели, распределять роли, договариваться друг с другом; учиться управлять поведением партнера: убеждать его, контролировать, корректировать и оценивать действия. Воспитывать стремление понимать других людей, стремление к самообразованию, готовность прийти на помощь товарищам, толерантное отношение к мнению других людей.
Личностные:
Формировать: ответственное отношение к учению, готовность и способность к саморазвитию и самообразованию на основе мотивации к обучению, коммуникативную компетентность в образовательной деятельности.
Методы обучения:
- словесные (беседа, рассказ);
- практические (выполнение лабораторной);
- наглядные (презентация, демонстрационный опыт);
- частично-поисковые (проектная деятельность, инструктивные карточки, лабораторные опыты).
Методические приемы – работа с текстом, лабораторная работа, самостоятельная работа с текстом учебника и со слайдами презентации, взаимопроверка результатов работы в паре.
Образовательные ресурсы:
Презентация в PowеrPoint (интерактивная доска);
Периодическая система химических элементов Д.И. Менделеева;
Таблица растворимости
Учебник: О.С. Габриелян, И.Г. Остроумов Химия, 8 класс;
Инструктивная карточка для проведения урока;
Наборы реактивов: растворы гидроксида натрия, соляной кислоты, серной кислоты, сульфата меди (II), фенолфталеина; индикаторная бумага, гидроксид меди(II), гидроксид железа (III), углекислый газ, газоотводная трубка, нагревательное оборудование, пробирки, держатели для пробирок, штативы
Инструктивная карта для проведения лабораторной работы;
Интернет – ресурсы.
Базовые понятия и термины:
Основания, щелочи, кислоты, соли, реакция нейтрализации, реакции обмена, индикаторы, растворимость.
Этапы урока:
Организационный этап.
Постановка цели и задач урока. Мотивация учебной деятельности учащихся.
Актуализация знаний.
Первичное усвоение новых знаний.
Первичная проверка понимания
Первичное закрепление.
Домашнем задании, инструктаж по его выполнению
Рефлексия
Подведение итогов занятия
ХОД УРОКА
1)ОРГАНИЗАЦИОННЫЙ ЭТАП.
2) ПОСТАНОВКА ЦЕЛИ И ЗАДАЧ УРОКА. МОТИВАЦИЯ УЧЕБНОЙ ДЕЯТЕЛЬНОСТИ УЧАЩИХСЯ.
3) АКТУАЛИЗАЦИЯ ЗНАНИЙ.
- Приведите примеры простых и сложных веществ. Дайте им названия.
-Какие вещества называются кислотами, оксидами, основаниями?
-Атомы каких элементов входят в состав всех кислот, оксидов, оснований?
- Какие классификации кислот, оксидов, оснований вы знаете? На каких признаках они основаны?
-Какие правила техники безопасности необходимо соблюдать при работе с кислотами, щелочами? -С какими химическими веществами мы встречаемся в быту? Где они применяются?
Задание «Третий лишний»
А) CaO FeO NaOH
Б) O2 H2 CO2
B) HCl H2SO4 SO3
Задание «Крестики – нолики»
| KOH | KCl | HCl |
| K2O | Ca(OH)2 | CaCl2 |
| CaO | H2O | Ba(OH)2 |
Задание «Добавь недостающее слово»
Вещества, которые образованы атомами одного химического элемента, называют …….. веществами.
Химический диктант (по вариантам)
Учитель диктует формулу, ученики записывают название вещества, если название — формулу.
1 вариант
Азотная кислота
Соляная кислота.
Оксид натрия.
Ортофосфорная кислота
СО2.
Серная кислота.
СаО.
Оксид бария.
Оксид серы(IV).
Оксид железа (III).
Н3РО4.
Рассказ учителя
В своей жизни человек встречается с основаниями: в природе с минералами, в быту - это моющие средства, зубные пасты, представители этого класса веществ используются в производстве сахара, строительной индустрии. Поэтому очень важно знать свойства этих веществ и правила безопасного поведения с ними.
Задание (устно)
«Продолжи предложение»
Основания-это сложные вещества...
Основания еще называют...
По кислотности основания классифицируют...
Работа в парах: из предложенного списка выпишите отдельно щелочи и нерастворимые основания, дайте им названия.
ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА
4)ПЕРВИЧНОЕ УСВОЕНИЕНОВЫХ ЗНАНИЙ.
СОСТАВ, НАЗВАНИЯ И КЛАССИФИКАЦИЯ ОСНОВАНИЙ.
Рассказ учителя.
Основания — сложные неорганические вещества, состоящие из атомов металлов и одной или нескольких гидроксильных групп (ОН). Гидроксогруппа одновалентна. Такое название она имеет потому, что в ее состав входят атомы водорода и кислорода (гидроген и оксиген). Общая формула оснований —
П I

![]()





Na-0-Н
О-Н
о-н
о-н
А1 О-Н
О-Н
Ме(ОН)п , где Me —- обозначение металла, п — его валентность. Записываем на доске несколько структурных формул оснований:NaOH Са(ОН)2 А1(ОН)3
Названия оснований составляют путем соединения слова «гидроксид» и наименования металла, например, NaOH — гидроксид натрия. Первым словом является слово гидроксид, а вторым название элемента. Если элемент имеет переменную валентность, то в названии указывают ее значение после названия элемента, римской цифрой в скобках. Например, Fе(ОН)2 – гидроксид железа (II), Fе(ОН)3 – гидроксид железа (ПІ).
Для некоторых оснований применяются традиционные названия. Например, натрий гидроксид называется «едкий натр» или «каустическая сода», калий гидроксид — «едкий кали», кальций гидроксид — «гашеная известь», барий гидроксид — «едкий барит».
Работа с учебником.
Учащиеся самостоятельно знакомятся с текстом учебника § 24 стр 105-107.
ПЕРВИЧНАЯ ПРОВЕРКА ПОНИМАНИЯ НОВЫХ ЗНАНИЙ.
Индивидуальное задание (по карточкам).
Напишите формулы гидроксидов лития, бария, стронция, цезия, никеля (II), олова (II), хрома (ПІ).
ФИЗИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ.
Опережающее задание, физические свойства оснований, (сообщение ученика)
Рассказ учителя.
Основания делятся на растворимые и нерастворимые в воде.
Демонстрация.
Учитель демонстрирует образцы оснований.
Си(ОН)2 — голубого цвета; Fe(0H)3 —бурого, Ni(OH)2 —бледно-зеленого, Сг(ОН)3 — серо-зелёного цвета.
Задание.
Пользуясь таблицей растворимости, приведите формулы и названия растворимых и нерастворимых гидроксидов.
ПОЛУЧЕНИЕ ОСНОВАНИЙ.
Учащиеся обсуждают возможные способы получения растворимых оснований
Опираясь на ранее полученные знания при помощи учителя составляют уравнения химических реакций
Натрий+ вода =
Оксид натрия+вода =
Демонстрация.
Получение гидроксида меди(II).
В пробирку с 0,5 мл гидроксида натрия добавляется приблизительно такое же количество растворимой соли меди (II), например, сульфата меди(II). Наблюдается выпадение голубого осадка гидроксида меди(II).
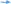
 CuS04 + 2NaOH Cu(OH)2 +Na2S04.
CuS04 + 2NaOH Cu(OH)2 +Na2S04.
ПРАВИЛА ТЕХНИКИ БЕЗОПАСТНОСТИ ПРИ РАБОТЕ СО ЩЕЛОЧАМИ.
Рассказ учителя.
Щелочи — очень агрессивные вещества, они разъедают кожу, ткани, бумагу и другие предметы. При попадании раствора щелочи на кожу или одежду необходимо смыть ее большим количеством проточной воды до исчезновения чувства мылкости, а затем нейтрализовать слабой кислотой — борной или уксусной. Твердые щелочи следует брать только пинцетом, так как при попадании на кожу они могут вызвать ожог.
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ.
Лабораторная работа.
Выполняется лабораторная работа В процессе работы заполняется таблица «Химические свойства оснований»
| ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ | |
| ЩЕЛОЧИ | НЕРАСТВОРИМЫЕ ОСНОВАНИЯ |
| ДЕЙСТВИЕ НА ИНДИКАТОРЫ | |
|
| |
| ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ | |
|
|
|
| ВЗАИМОДЕЙСТВИЕ С КИ | СЛОТНЫМИ ОКСИДАМИ |
|
|
|
| ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ | |
|
|
|
| РАЗЛОЖЕНИЕ ПРИ НАГРЕВАНИИ | |
|
| |
а) Изменение окраски индикаторов в растворах щелочей.
В пробирку поместить по 0,5 мл растворов гидроксида натрия и гидроксида меди (II) . Учащиеся добавляют несколько капель фенолфталеина в обе пробирки. Убеждаются, что только щелочи изменяют окраску индикатора: фенолфталеин становится малиновым в растворе гидроксида натрия.
б) Взаимодействие щелочей с кислотами.
Выполняется лабораторная работа.
В пробирку налить 1 мл раствора гидроксида натрия и добавить несколько капель раствора фенолфталеина. В какой цвет окрасился раствор? Объясните наблюдаемые изменения. К раствору малинового цвета из пипетки по каплям добавлять раствор соляной кислоты. После каждой капли пробирку встряхивать. Что происходит? Объясните наблюдаемые изменения. Напишите уравнение реакции
в) Взаимодействие нерастворимых оснований с кислотами.
Выполняется лабораторная работа.
В пробирку с 1мл раствора сульфата меди (II) прилить по каплям раствор гидроксида натрия. Что при этом наблюдаем? Почему происходят эти изменения? Напишите уравнение реакции.
К полученному осадку гидроксида меди (II) прилить по каплям раствор серной кислоты. Объясните происходящие изменения. Напишите уравнение реакции.
г) Разложение нерастворимых оснований при нагревании (просмотр видео опыта)
6)ПЕРВИЧНОЕ ЗАКРЕПЛЕНИЕ.
Задание.
Закончить уравнение химических реакций, отражающих свойства оснований. Укажите к какому типу относятся данные реакции (соединения, разложения, замещения, обмена)
Mg (OH)2 + HCl =
Fe (OH)2 =
Ba (OH)2 + H2SO4 =
NaOH + Zn (NO3)2=
Ca (OH)2 + CO2 =
Al(OH)3 =
Ba(OH)2 +SO3=
Это интересно знать!
В следствие загрязнения атмосферы сероводородом картины, написанные до середины 19 века со временем темнеют. Это происходит из-за взаимодействия свинцовых белил с сероводородом. Выпадает черный осадок сульфида свинца (II). В1850 году эта проблема была решена потому, что начали выпускать цинковые белила, которые при реакции с сероводородом образуют белый осадок.
По предложенной схеме составьте уравнения химических реакций, которые ведут к образованию
Цинковых белил.
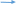

 Zn ZnCI 2 Zn(OH) 2 ZnO
Zn ZnCI 2 Zn(OH) 2 ZnO
Задание. Вставьте недостающие формулы.
Fe(OH)2 + ? = FeSO4 + ?
7)ДОМАШНЕЕ ЗАДАНИЕ (инструктаж по его выполнению)
Изучить § 24, ответить на вопросы №1,2 на стр 107
Выполнить задание №4 на стр 108
8)РЕФЛЕКСИЯ
9)ПОДВЕДЕНИЕ ИТОГОВ УРОКА

 Получите свидетельство
Получите свидетельство Вход
Вход










 Урок химии 8 класс по теме "Основания" (51.36 KB)
Урок химии 8 класс по теме "Основания" (51.36 KB)
 0
0 407
407 2
2 Нравится
0
Нравится
0



