
Алкены

Содержание
- Строение алкенов
- Изомерия и номенклатура алкенов
- Физические свойства
- Получение
- Химические свойства
- Применение алкенов
- Контрольные вопросы
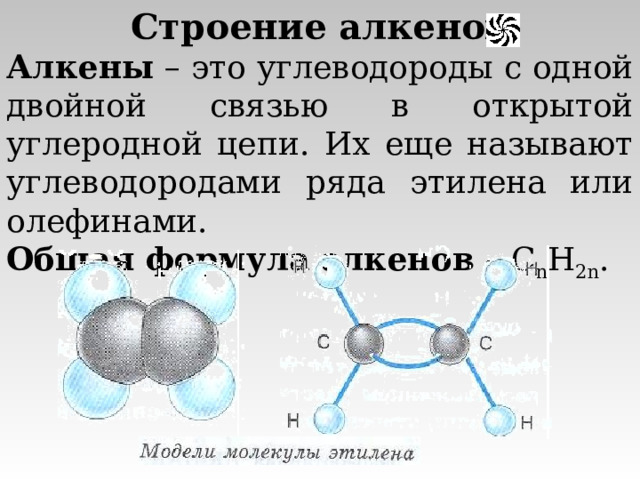
Строение алкенов
Алкены – это углеводороды с одной двойной связью в открытой углеродной цепи. Их еще называют углеводородами ряда этилена или олефинами.
Общая формула алкенов – C n H 2n .
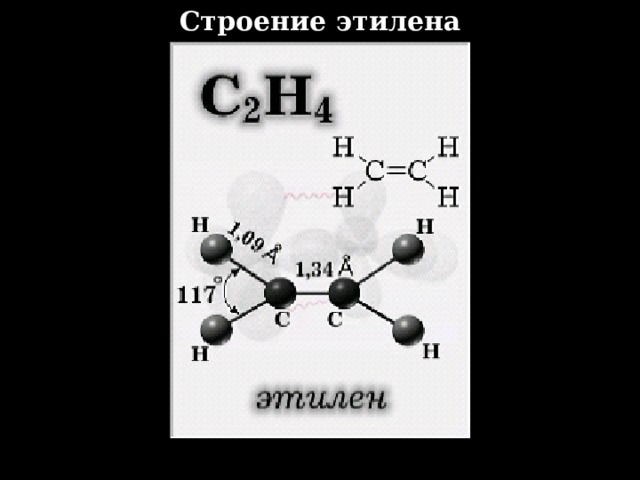
Строение этилена
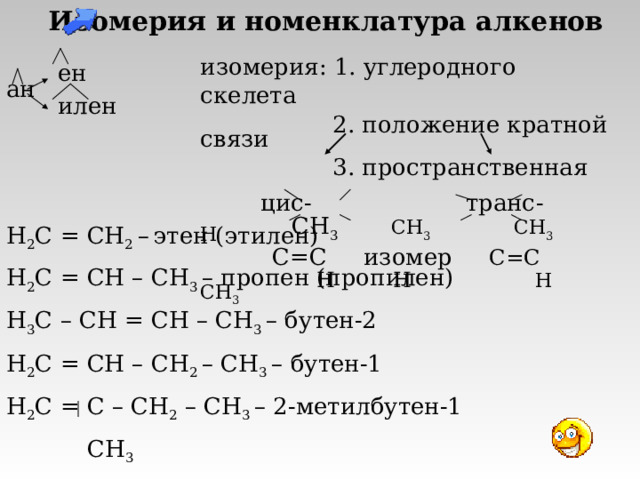
Изомерия и номенклатура алкенов
ен
ан
илен
изомерия: 1. углеродного скелета
2. положение кратной связи
3. пространственная
цис - транс -
СН 3 СН 3 СН 3 Н
С=С изомер С=С
Н Н Н СН 3
H 2 C = CH 2 – этен (этилен)
H 2 C = CH – CH 3 – пропен (пропилен)
H 3 C – CH = CH – CH 3 – бутен-2
H 2 C = CH – CH 2 – CH 3 – бутен-1
H 2 C = C – CH 2 – CH 3 – 2-метилбутен-1
CH 3
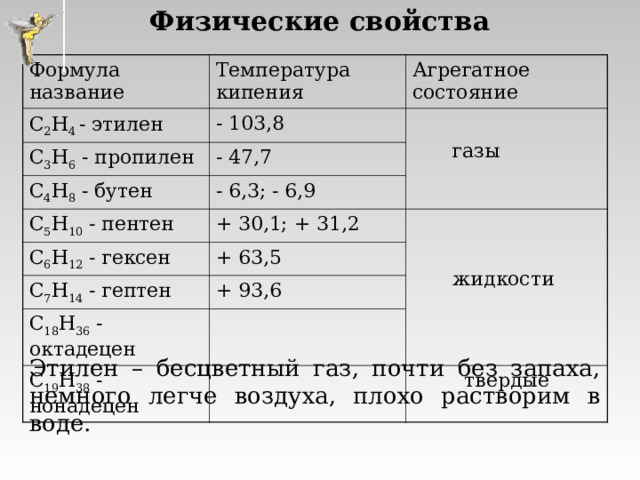
Физические свойства
Формула название
Температура кипения
C 2 H 4 - этилен
- 103,8
C 3 H 6 - пропилен
Агрегатное состояние
газы
- 47,7
C 4 H 8 - бутен
C 5 H 10 - пентен
- 6,3; - 6,9
C 6 H 12 - гексен
+ 30,1; + 31,2
жидкости
+ 63,5
C 7 H 14 - гептен
+ 93,6
C 18 H 36 - октадецен
C 19 H 38 - нонадецен
твердые
Этилен – бесцветный газ, почти без запаха, немного легче воздуха, плохо растворим в воде.
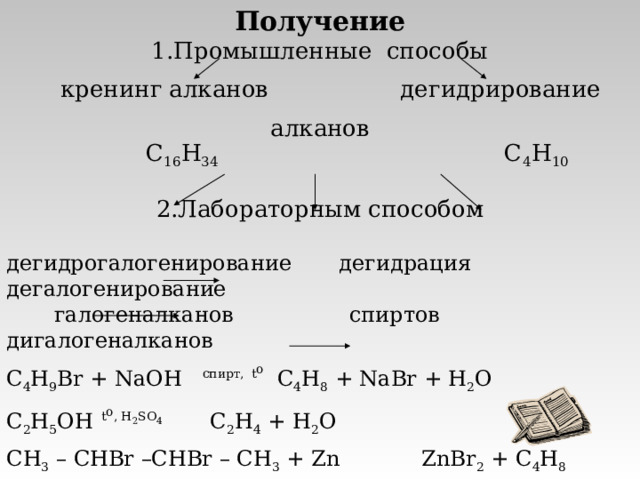
Получение
- Промышленные способы
кренинг алканов дегидрирование алканов
C 16 H 34 C 4 H 10
- Лабораторным способом
дегидрогалогенирование дегидрация дегалогенирование
галогеналканов спиртов дигалогеналканов
C 4 H 9 Br + NaOH спирт, t o C 4 H 8 + NaBr + H 2 O
C 2 H 5 OH t o , H 2 SO 4 C 2 H 4 + H 2 O
С H 3 – CHBr –CHBr – CH 3 + Zn ZnBr 2 + C 4 H 8

ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕ ГИДРАТАЦИЯ СПИРТОВ
СПИРТ → АЛК ЕН + ВОДА
ПРИМЕР: t≥ 14 0C ,
Н Н Н 2 SO 4 (конц.)
Н-С – С-Н → Н 2 С = СН 2 + Н 2 О
Н ОН эт ен
(эт илен )

Получение алкенов
КРЕКИНГ АЛКАНОВ
АЛК АН → АЛК АН + АЛК ЕН
С БОЛЕЕ ДЛИННОЙ С МЕНЕЕ ДЛИННОЙ
УГЛЕРОДНОЙ УГЛЕРОДНОЙ
ЦЕПЬЮ ЦЕПЬЮ
ПРИМЕР:
t=400-700C
С 10 Н 22 → С 5 Н 12 + С 5 Н 10
дек ан пент ан пент ен

ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕ ГИДРИРОВАНИЕ АЛКАНОВ
АЛК АН → АЛК ЕН + ВОДОРОД
ПРИМЕР:
Ni, t= 5 00C
Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2
эт ан эт ен
(эт илен )

ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕ ГИДРО ГАЛОГЕН ИРОВАНИЕ
УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ
ПРИМЕР:
спиртовой
H H раствор
Н-С–С-Н +KOH →Н 2 С = СН 2 +K Cl + H 2 O
Н Cl эт ен
хлорэт ан (эт илен )
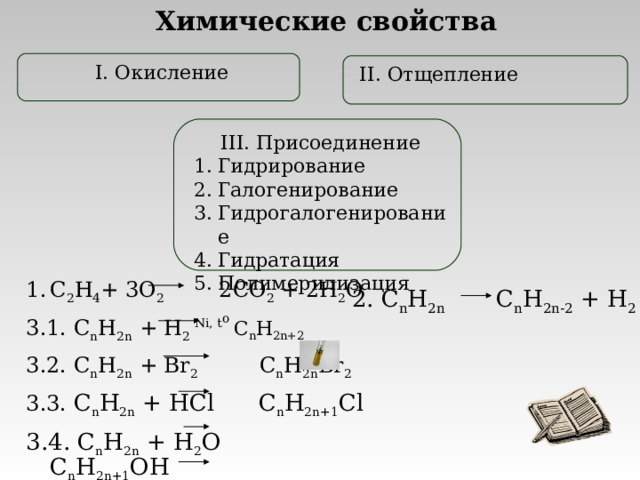
Химические свойства
I. Окисление
II. Отщепление
III. Присоединение
- Гидрирование
- Галогенирование
- Гидрогалогенирование
- Гидратация
- Полимерилизация
- C 2 H 4 + 3 O 2 2 CO 2 + 2 H 2 O
3.1. C n H 2n + H 2 Ni, t o C n H 2n + 2
3.2. C n H 2n + Br 2 C n H 2n Br 2
3.3. C n H 2n + HCl C n H 2n+1 Cl
3.4. C n H 2n + H 2 O C n H 2n+1 OH
3.5. nC n H 2n + … полимер
2. C n H 2n C n H 2n-2 + H 2
![РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНГАНАТА КАЛИЯ (реакция Е.Е.Вагнера) Н 2 С=СН 2 + [O] + H 2 O H 2 C - CH 2 OH OH этиленгликоль (этандиол-1,2) ! Качественная реакция на непредельность углеводорода – на кратную связь](https://fsd.videouroki.net/html/2022/01/20/v_61e97730a4ac5/img12.jpg)
РЕАКЦИИ ОКИСЛЕНИЯ
МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНГАНАТА КАЛИЯ
(реакция Е.Е.Вагнера)
Н 2 С=СН 2 + [O] + H 2 O H 2 C - CH 2
OH OH
этиленгликоль
(этандиол-1,2)
! Качественная реакция на непредельность углеводорода – на кратную связь

РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ
Это процесс соединения одинаковых молекул в более крупные.
ПРИМЕР: n CH 2 =CH 2 (-CH 2 -CH 2 -)n
этилен поли этилен
(мономер) (полимер)
n – степень полимеризации, показывает число молекул, вступивших в реакцию
-CH 2 -CH 2 - структурное звено
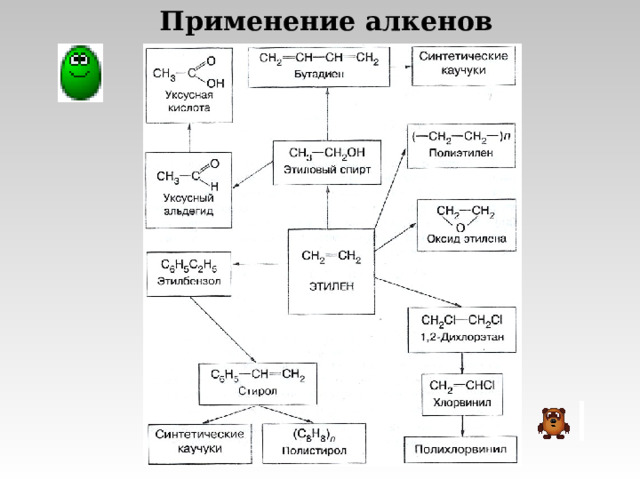
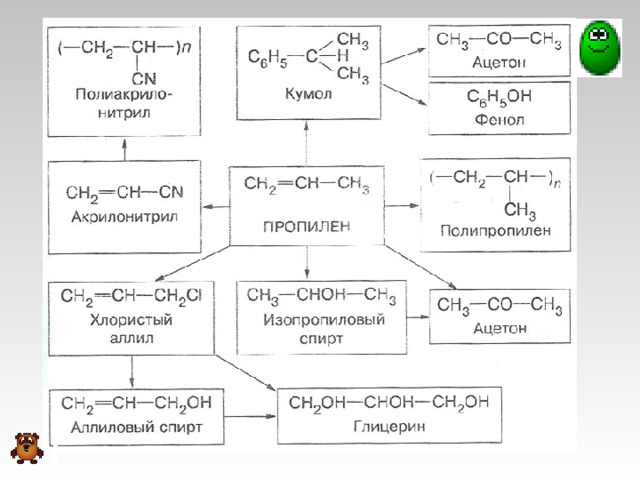
Применение алкенов

Контрольные вопросы
1. Вставьте в текст соответствующие слова и символы из скобок.
Алкенами называются углеводороды, содержащие в молекуле одну … (одинарную, двойную, тройную) связь и имеющие общую формулу …( C n H 2n+2 , C n H 2n , C n H 2n - 2 ). Атомы углерода, связанные кратной связью, находятся в состоянии …( sp -, sp 2 -, sp 3 -) гибридизации. Угол между осями гибридных орбиталей равен …(90 0 ,109 0 28 ' ,120 0 ,180 0 ). Каждый из таких атомов углерода образует с соседними атомами …(одну, две, три, четыре) σ -связи и … (одну, две, три, четыре) π -связь. Длина углерод-углеродной связи в этилене … (больше, меньше), чем в этане, и равна (0,154 нм, 0,120 нм, 0,134 нм).

2. Алкены можно также назвать:
а) этиленовыми углеводородами,
б) олефиновыми углеводородами,
в) непредельными углеводородами,
г) все предыдущие ответы верны.
3. Число σ и π -связей в молекуле этена равно соответственно:
а) 1 и 1, б) 4 и 2, в) 5 и 1, г) 4 и 1.
4. Состав октена отражает общая формула:
а) C n H 2n+2 , б) C n H 2n , в) C n H 2n - 2 , г) C n H 2n -6

5. Соотнесите:
тип углеводорода: 1) алканы, 2) алкены;
формула: а) C 2 H 4 , б ) CH 4 , в) C 7 H 16 ,
г) C 12 H 24 , д) C 6 H 12 , е) C 3 H 8 .
6. Тип гибридизации атомов углерода в пропене
CH 2 = CH – CH 3 слева направо:
а) sp 2 , sp 2 , sp 2 , б) sp 2 , sp, sp 3 ,
в) sp, sp, sp 2 , г) sp 2 , sp 2 , sp 3 .
7. Двойная связь в алкенах состоит из:
а) одной σ - и одной π -связи, б) двух π -связей,
в) двух σ -связей, г) верного ответа нет.
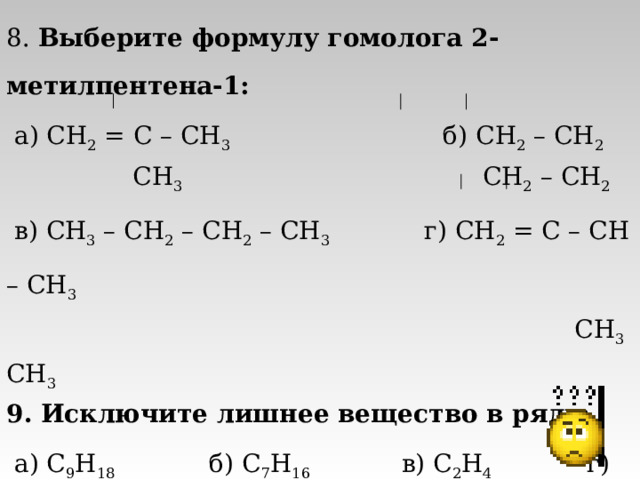
8. Выберите формулу гомолога 2-метилпентена-1:
а) CH 2 = C – CH 3 б ) CH 2 – CH 2
CH 3 CH 2 – CH 2
в) CH 3 – CH 2 – CH 2 – CH 3 г) CH 2 = C – CH – CH 3
CH 3 CH 3
9. Исключите лишнее вещество в ряду:
а) C 9 H 18 б) С 7 H 16 в) C 2 H 4 г) C 5 H 10
10. Молекула этана имеет строение:
а) плоское, б) тетраэдрическое,
в) линейное, г) пирамидальное.
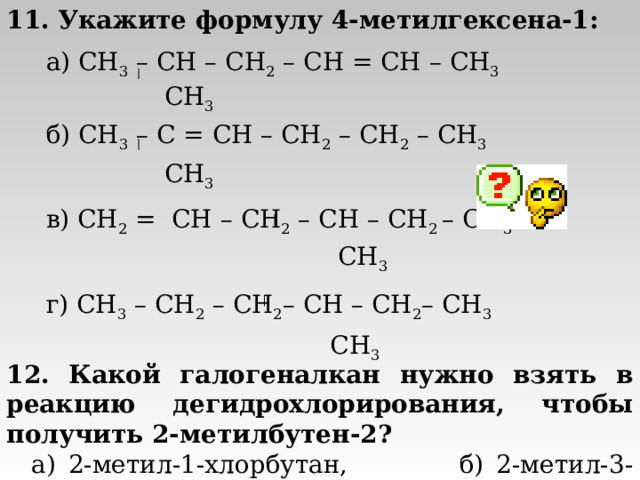
11. Укажите формулу 4-метилгексена-1:
а) CH 3 – CH – CH 2 – CH = CH – CH 3
CH 3
б) CH 3 – C = CH – CH 2 – CH 2 – CH 3
CH 3
в) CH 2 = CH – CH 2 – CH – CH 2 – CH 3
CH 3
г) CH 3 – CH 2 – CH 2 – CH – CH 2 – CH 3
CH 3
12. Какой галогеналкан нужно взять в реакцию дегидрохлорирования, чтобы получить 2-метилбутен-2?
а) 2-метил-1-хлорбутан, б) 2-метил-3-хлорбутан,
в) 2-метил-4-хлорбутан, г) 2-метил-2,3-дихлорбутан
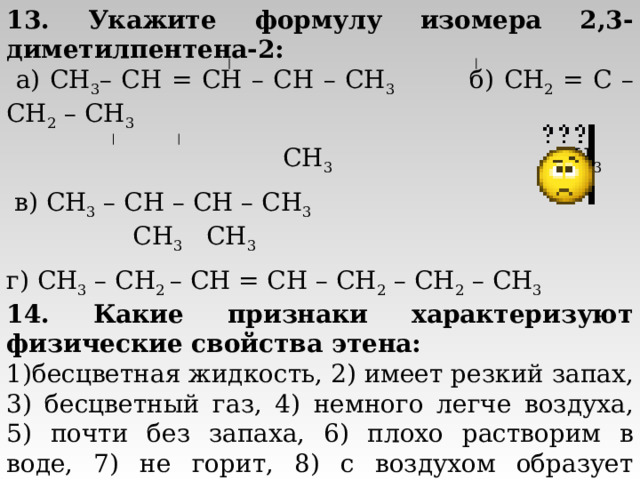
13. Укажите формулу изомера 2,3-диметилпентена-2:
а) CH 3 – CH = CH – CH – CH 3 б) CH 2 = C – CH 2 – CH 3
CH 3 CH 3
в) CH 3 – CH – CH – CH 3
CH 3 CH 3
г) CH 3 – CH 2 – CH = CH – CH 2 – CH 2 – CH 3
14. Какие признаки характеризуют физические свойства этена:
- бесцветная жидкость, 2) имеет резкий запах, 3) бесцветный газ, 4) немного легче воздуха, 5) почти без запаха, 6) плохо растворим в воде, 7) не горит, 8) с воздухом образует взрывоопасные смеси?
а) 3,4,5,6,8; б) 1,2,6,7; в) 2,3,4,6,8; г) 3,4,6,8.

15. Какой тип реакции не характерен для алкенов?
а) замещение б) присоединение
в) окисление г) полимеризации
16. Реакция присоединения водорода называется:
а) гидрированием б) гидрогалогенированием
в) гидратацией г) дегидрированием
17. В реакции бромирования пропена образуется: а) 1,3- дибромпропан б) 1-бромпропан
в) 2-бромпропан г) 1, 2- дибромпропан
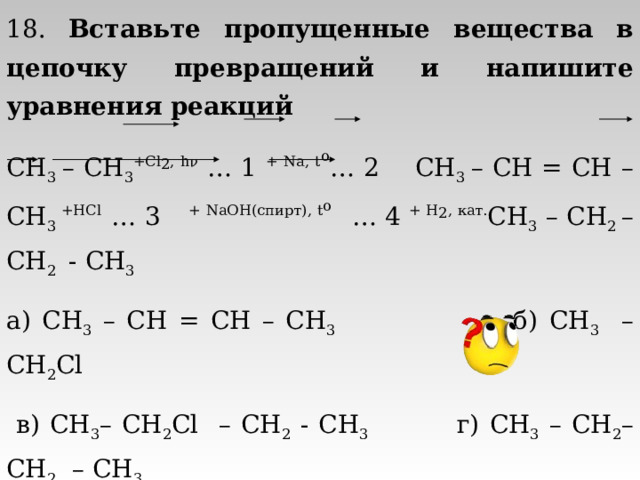
18. Вставьте пропущенные вещества в цепочку превращений и напишите уравнения реакций
CH 3 – CH 3 + Cl 2 , h ν … 1 + Na, t o … 2 CH 3 – CH = CH – CH 3 +HCl … 3 + NaOH( спирт ) , t o … 4 + H 2 , кат. CH 3 – CH 2 – CH 2 - CH 3
а) CH 3 – CH = CH – CH 3 б) CH 3 – CH 2 Cl
в) CH 3 – CH 2 Cl – CH 2 - CH 3 г) CH 3 – CH 2 – CH 2 – CH 3
Ответы
- двойную, C n H 2n , sp 2 -, 120 0 , одну, одну, 0,134 нм
- Г
- В
- Б
- 1- б, в, е; 2- а, г, д
- Г
- А
8. А
9. Б
10. А
11. В
12. Б
13. Г
14. А
15. А
16. А
17. Г
18. 1-б, 2-г, 3-в, 4-а.

 Получите свидетельство
Получите свидетельство Вход
Вход











 Презентация по теме Алкены (1.26 MB)
Презентация по теме Алкены (1.26 MB)
 0
0 2097
2097 113
113 Нравится
0
Нравится
0



