Разработала Артеменко Вера Павловна, учитель химии МОУ СОШ №28 г. Белгорода.
Данный урок включает в себя элементы групповой проектной деятельности учащихся, которые заранее разбиваются на группы по интересам, работают с литературой и Интернет-ресурсами по проблемным вопросам, готовят отчет в виде сообщений и слайдов презентации, из которых впоследствии совместно с учителем составляется единая презентация к уроку. Учитель играет роль координатора и некоторые моменты нового материала дает лекционно. Ввиду большого объема изучаемого материала целесообразно проводить данный урок спаренным.Проектный метод позволяет ученикам реализовать свои творческие способности и реализовывать личностные возможности.
Урок химии в 10 классе.
Тема: Строение и свойства алканов.
Цели:
1)Дать учащимся понятие о предельных углеводородах, их химическом, пространственном и электронном строении. Познакомить с понятиями гомологи, правилами названия веществ и составления формул по систематической номенклатуре;
2) Уметь объяснять тетраэдричное строение молекулы метана, записывать молекулярные и структурные формулы предельных УВ, различать понятия «гомолог» и «мзомер». Составлять формулы гомологов и изомеров для данного органического вещества;
3) Знать химические свойства предельных УВ, уметь составлять уравнения реакций и указывать условия их протекания. Знать способы получения и области применения предельных УВ. Продолжить формирование мировоззренческих понятий.
4) Воспитывать у учащихся навыки групповой творческой деятельности, чувство взаимопомощи и патриотизма.
Оборудование: презентация, мультимедийный проектор, видеофрагменты химических опытов, тетради, наборы шаростержневых моделей молекул.
Ход урока:
1. Вступительное слово учителя.
-Ребята! Сегодня на уроке мы изучим группу органических веществ, называемую предельными углеводородами. Не проходит ни одного дня, в течение которого вы бы ни разу не столкнулись дома или на улице с этими веществами: каждый день вы включаете на кухне газ, чтобы разогреть пищу, пользуетесь автомобильным транспортом, двигатели которого работают на органическом топливе, живете в домах, большинство отделочных материалов в которых содержат производные предельных углеводородов и т.д. Готовясь к этому уроку, творческие группы нашли много интересного и важного материала о строении, свойствах и применении алканов, и подготовили свои отчеты. Давайте же постараемся быть внимательными и хорошо запомнить новый материл. Итак, слово предоставляется группе геологов. Они расскажут вам о нахождении алканов в природе.
П. Изучение нового материала.
Группа «Геологи». Сообщение учащихся, иллюстрируемое слайдами.
1. Алканы в природе (Сообщение учащегося).
Предельные углеводороды распространены в природе довольно широко. В недрах Земли содержаться огромные запасы газа. Природный газ содержит в основном метан, а в качестве примесей этан, пропан и др. Попутный нефтяной газ отличается пониженным содержанием метана, но содержит больше его гомологов. Высшие алканы входят в состав нефти. Состав нефти из разных месторождений непостоянен. Метан может образовываться при гниении растительных остатков на дне болот, откуда происходит одно из его названий - болотный газ.
Метан содержится в атмосфере планет-гигантов (Сатурн, Юпитер), а также в атмосфере их спутников, например, Титана. Твердые углеводороды иногда образуют залежи минерала, получившего название "горный воск" или озокерит. Его месторождения встречаются в горах Тянь-Шаня и Памира.

Крупнейшие местороджения природного газа в России:
Понятие о предельных углеводородах ( Рассказ учителя, работа со словарем терминов).
Учитель: Проблемный вопрос: Почему алканы называются «предельными углеводородами»?
АЛКАНЫ - это углеводороды с общей формулой Сп Н2п + 2 в молекулах которых между атомами углерода имеются только одинарные (сигма) связи.
В молекулах алканов имеются только одинарные  - связи. Все четыре валентности атома углерода в молекулах алканов полностью, т.е. до предела, насыщены атомами углерода и водорода. Между атомами углерода отсутствуют кратные связи. Отсюда происходят другие названия этих углеводородов - насыщенные или предельные.
- связи. Все четыре валентности атома углерода в молекулах алканов полностью, т.е. до предела, насыщены атомами углерода и водорода. Между атомами углерода отсутствуют кратные связи. Отсюда происходят другие названия этих углеводородов - насыщенные или предельные.
Алканы образуют гомологический ряд. Определение: Гомологи – это вещества, сходные по строению и химическим свойствам, но отличающиеся друг от друга на группу атомов –СН2( гомологическую разность).
Первые четыре представителя ряда алканов имеют тривиальные названия (см. таблицу №1).
Словарная работа учащихся: записать термины: гомологи, гомологический ряд, гомологическая разность.
Таблица №1. «Гомологический ряд алканов»
(первые десять представителей).
| ННазвание алкана | формула | радикал | Формула |
| Метан | СН4 | метил | СН3 |
| Этан | С2Н6 | этил | С2Н5 |
| Пропан | С3Н8 | пропил | С3Н7 |
| Бутан | С4Н10 | бутил | С4Н9 |
| Пентан | С5Н12 | пентил | С5Н11 |
| Гексан | С6Н14 | гексил | С6Н13 |
| Гептан | С7Н16 | гептил | С7Н15 |
| Октан | С8Н18 | октил | С8Н17 |
| Нонан | С9Н20 | нонил | С9Н19 |
| Декан | С10Н22 | децил | С10Н21 |
2) Строение молекулы метана как представителя алканов:
Учитель. Проблемный вопрос: Как вы думаете, что общего между молекулой метана и пакетом молока? ( Учащиеся предлагают разные варианты ответов).
Сейчас группа «Математиков и физиков» поможет нам разобраться в данном вопросе, рассказав об особенностях строения молекул алканов. Не забывайте конспектировать важнейшие вопросы в тетрадь и работать со словарем терминов.
Выступление группы «Математики и физики». Сообщение учащихся.

Простейшим представителем ряда алканов является метан. Особенности строения его молекулы связаны с явлением гибридизации.

В молекулах алканов атом углерода находится в состоянии sp3 - гибридизации. Данный факт позволяет предположить, что их молекулы имеют объемное строение. Молекула метана, например, как экспериментально установлено имеет тетраэдрическую форму. Гибридные орбитали валентных электронов атома углерода направлены к вершинам тетраэдра, где они перекрываются с электронными облаками атомов водорода, образуя прочные и одинаковые по свойствам химические связи. Взаимное отталкивание имеющих одинаковый объем и заряд электронных облаков приводит к их симметричному расположению в пространстве под тетраэдрическими углами 109 о 28/ (рис. 1а).

Учитель: Теперь вы можете ответить на проблемный вопрос изученного раздела?
Сделаем вывод:

В молекулах алканов с большим числом углеродных атомов атомы углерода в цепи расположены не по прямой линии, как в структурных формулах, а зигзагообразно. Причина этого в тетраэдрическом направлении валентных связей атомов углерода (рис.1б).
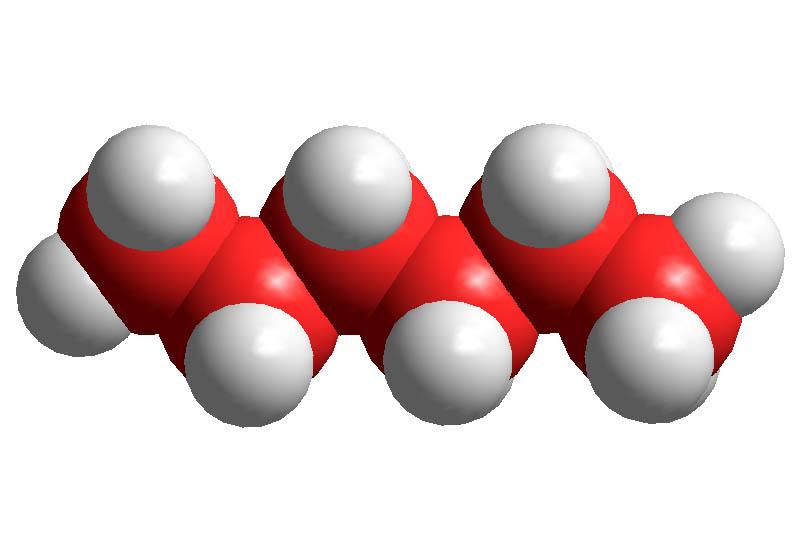

З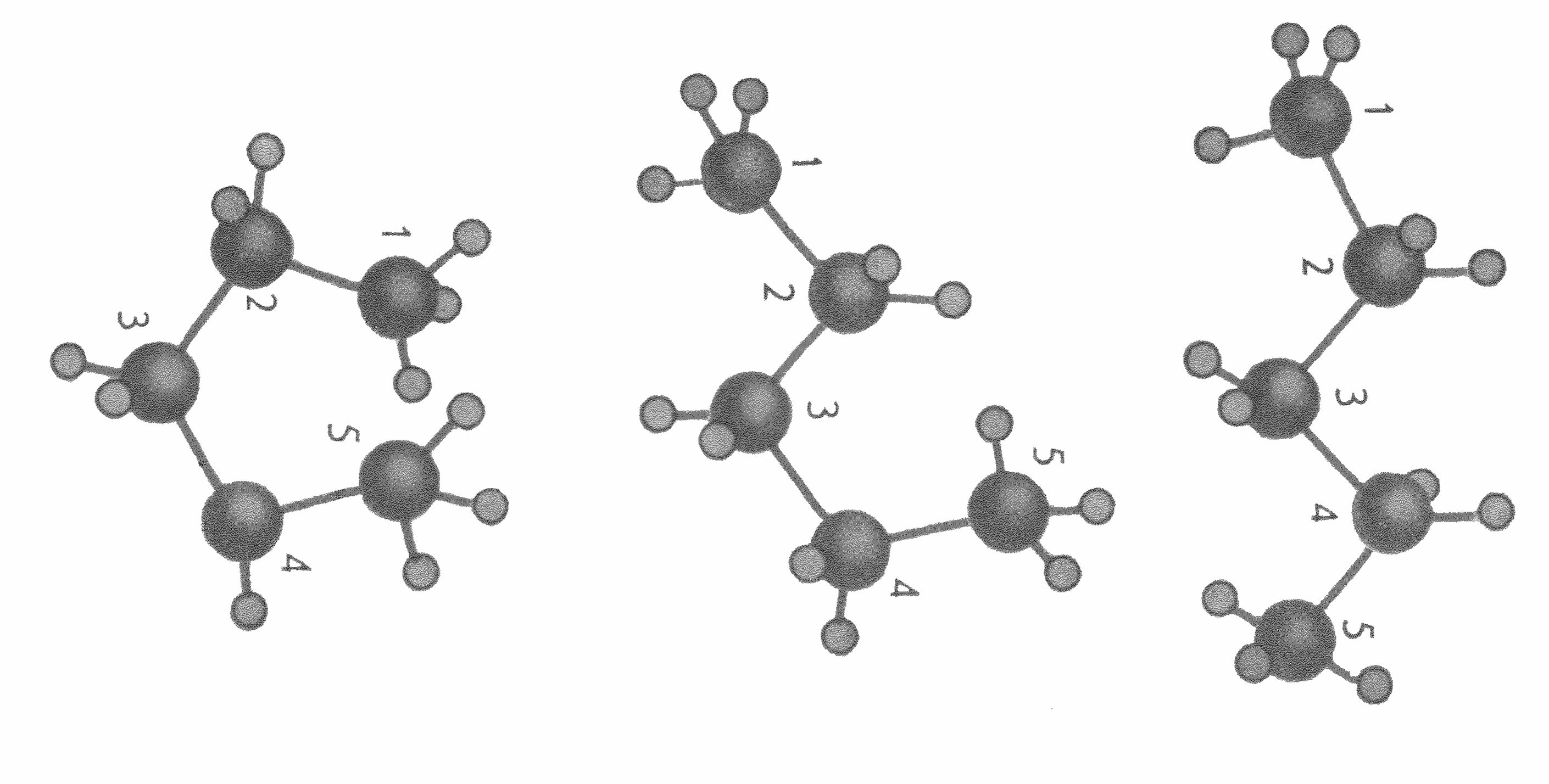 игзагообразная цепь атомов углерода, особенно в длинноцепочечных молекулах, может принимать различные пространственные формы.
игзагообразная цепь атомов углерода, особенно в длинноцепочечных молекулах, может принимать различные пространственные формы.
Это связано с тем, что атомы в молекуле могут относительно свободно вращаться вокруг химических (С-С) связей. Такое свободное вращение существует в молекулах как проявление теплового движения. Различные геометрические формы молекул, переходящие друг в друга путем вращения вокруг простых связей, называют конформациями или поворотными изомерами (конформерами).
Задание для учащихся от группы «Математики и физики»: пользуясь набором шаростержневыз моделей составить несколько молекул конформеров алканов). Обсуждение результатов работы.
Учитель: Для алканов, как и для всех органических соединений характерно явление изомерии. Число изомеров для представителей гомологического ряда алканов растет с увеличением числа атомов углерода в молекуле. Характерным видом изомерии алканов является структурная изомерия (изомерия углеродного скелета), то есть существуют алканы как с линейной, так и разветвленными углеродными цепями.

3. Физические свойства алканов. Сообщение учащегося из группы «Физиков».
Первые четыре представителя ряда алканов - это газы, начиная с пентана - жидкости, а углеводороды с числом атомов углерода выше 16 при обычной температуре представляют собой твердые вещества. Углеводороды с разветвленной цепью кипят при более низкой температуре, чем соответствующие им соединения нормального строения, а температура плавления, наоборот, выше у изомеров с разветвленной цепью.
Предельные углеводороды - соединения неполярные. Они легче воды и практически нерастворимы в ней, однако, они способны растворяться в большинстве органических растворителей, в том числе и друг в друге. Жидкие алканы сами являются хорошими растворителями для многих органических веществ. Газообразные и твердые алканы не имеют запаха, жидкие алканы обладают характерным "бензиновым" запахом.
4) Номенклатура алканов (основная – систематическая).
Работа в тетради. Демонстрация слайда и таблицы.
Учитель:
2-метил, 3-этил, 4-хлор, 2,5,6-трибромоктан.
Не звезда это, не птица, и уж точно не банан!
Что за странное названье?
Как узнать? Вот наказанье!
Может новое лекарство? Африканский ритуал?
Колдовское заклинанье? Переход в другой астрал?
Тарабарщина сплошная! Мне вовек не разгадать…
-Нет, дружок! -сказал учитель,- Надо химию лишь знать.
Я открою тебе тайну – это только лишь алкан,
2-метил, 3-этил, 4-хлор, 2,5,6-трибромоктан.
Ребята! Названия органических веществ трудно запомнить, но глядя на формулу и соблюдая определенные правила вы сможете дать название даже самому сложному веществу. Сейчас вы изучите алгоритм составления названий алканов, а в дальнейшем легко давать названия и другим классам органических соединений. Для этого вам потребуются определенные знания по русскому языку и математике.
Префикс+корень+суффикс.
Алгоритм составления названий органических соединений
Выбирают наиболее длинную (главную) цепь и нумеруют ее ближе к тому концу, к которому стоит радикал ( заместитель, обозначен желтым цветом)
(3) (4) (5) (6) (7)
СН3 – СН – СН 2 – СН2 – СН2 – СН – СН2 – СН3
! !
(2) СН 2 СН 2 – СН2 – СН3
! (8) (9) (10)
(1) СН3
Данное вещество называется: 3-метил, 7-этилдекан
2. Название строится в следующей последовательности:
А) ПРЕФИКС: состоит из цифры, указывающей на номер углеродного атома, возле которого стоит радикал. Например: 3- и пишется название самого радикала. Например: 3-метил,7-этил……. Если молекула содержит несколько одинаковых радикалов, то после перечисления всех цифр, указывающих их местоположение, к радикалу добавляют числовую приставку ( ди –два, три – три, тетра – четыре). Например: 2,3 – диметил………….., или 3,4,5 – триэтил…….
Б) КОРЕНЬ: ставится в соответствии с гомологическим рядом алканов ( смотри по количеству атомов углерода в главной цепи)
В) СУФФИКС: у алканов суффикс «АН».
4. Химические свойства алканов.
Учитель: Проблемный вопрос: Почему алканы считают химически инертными веществами?
Пришло время познакомиться с химическими свойствами предельных углеводородов. Сейчас эксперы-химики их группы «Химиков» дадут нам общую характеристику химических свойств алканов. (Сообщения учащихся).
Химик 1: В молекулах предельных углеводородов все атомы связаны друг с другом прочными - связями, а валентности углеродных атомов полностью насыщены водородом. Поэтому предельные углеводороды не могут вступать в реакции присоединения. В обычных условиях алканы химически инертны. На них не действуют щелочи, кислоты, сильные окислители, щелочные металлы. По этой причине одно из названий алканов - парафины ( от лат. parum affinis - малое сродство).
В химические реакции алканы вступают только при сообщении им достаточно большого количества энергии. Это может происходить при нагревании или УФ - облучении. Характер разрыва связей может быть различным в зависимости от условий протекания реакции. Может произойти разрыв С-Н связи и последующая замена атома водорода на другой атом или группу атомов или же разрыв С-С связи. Эти связи обладают незначительной полярностью, поэтому при их разрыве образуются не ионы, а радикалы, т.е. идет разрыв связей по гомолитическому механизму.
Химик 2: Сейчас мы рассмотрим реакции замещения алканов, протекающие с разрывом С-Н связей:
Реакции замещения у алканов.
Галогенирование (действие галогенов). Является важнейшей реакцией характерной для галогенов. Эта реакция протекает на свету или при нагревании. Как было доказано академиком Н.Н.Семеновым, эта реакция носит радикально-цепной характер, то есть идет через образование свободных радикалов.
При хлорировании в первую очередь будет происходить разрыв связи в молекуле хлора (Cl-Cl). Для разрыва ее связи достаточна энергия кванта света, поглощаемого молекулой.
 Cl : Cl hv Cl . + Cl .
Cl : Cl hv Cl . + Cl .
Образовавшиеся атомы хлора имеют на внешнем электронном слое по одному неспаренному электрону, т.е. являются свободными радикалами, которые обладают очень высокой химической активностью. При сближении такого радикала с молекулой метана, он вырывает из нее атом водорода с одним электроном, образуя хлороводород, а молекула метана превращается в свободный радикал. Этот новый радикал существует в свободном состоянии очень короткое время, за которое он взаимодействует с другой молекулой хлора, образуя молекулу хлорметана:




Н H











 Н С + Cl Cl Н С Сl + Cl
Н С + Cl Cl Н С Сl + Cl


 Н H
Н H
Вновь образовавшийся атом хлора взаимодействует со следующей молекулой метана, образуя еще раз хлороводород и радикал метил. Данный процесс может продолжаться до тех пор, пока не будут израсходованы реагенты или не исчезнут свободные радикалы, что может наступить, например, при их соединении друг с другом.
Подобные реакции, которые представляют собой цепь последовательных превращений, называют цепными реакциями. Они протекают по свободнорадикальному механизму.
hv
1

 ) СН3 СН3 + Сl2 CH2Cl CH3 + HCl
) СН3 СН3 + Сl2 CH2Cl CH3 + HCl
hv






 2) CH3 CH CH3 + Br2 CH3 CBr CH3 + HBr
2) CH3 CH CH3 + Br2 CH3 CBr CH3 + HBr
CH3 CH3
Реакция замещения атома водорода в молекулах алканов подчиняется определенным закономерностям. В первую очередь замещения протекает у наименее гидрированного атома углерода (см. пример №2)
Химик 3. (Сообщение учащегося).
Нитрование (Реакция Коновалова). При обычной температуре предельные углеводороды устойчивы к действию концентрированной азотной кислоты и практически с ней не взаимодействуют. При нагревании эта кислота действует как окислитель. Эта реакция была впервые осуществлена в 1888 году М.И.Коноваловым при действии на алканы разбавленной азотной кислотой при нагревании = 140о С. Реакция нитрования приводит к образованию нитросоединений и ее протекание идет согласно "правила замещения".
NO2





 CH3 CH CH3 + HNO3 CH3 C CH3 + H2O
CH3 CH CH3 + HNO3 CH3 C CH3 + H2O


CH3 CH3
2. Реакции окисления алканов
Горение. При обычных температурах алканы устойчивы к действию кислорода воздуха. Однако, при поджигании они горят с образованием углекислого газа и воды. Характер горения зависит от числа углеродных атомов в молекуле углеводорода. С увеличением их числа яркость пламени повышается. Это происходит вследствие неполного сгорания углеродных частиц, которые, раскаляясь, придают соответствующий цвет пламени. Высшие алканы при горении могут сильно коптить, выделяя сажу (чистый углерод).
C nH2n+2 + O2 CO2 + H2O
nH2n+2 + O2 CO2 + H2O
(Просмотр видеоопыта)
Когда горят газообразные вещества, они хорошо смешиваются с воздухом и поэтому обычно сгорают полностью. При горении, например, расплавленного парафина кислорода для окисления всего углерода не хватает, и он выделяется в свободном виде. Реакция горения сильно экзотермична, что находит практическое применение в промышленности и быту.
2. Каталитическое окисление алканов.
Кроме реакции окисления происходящей при сгорании алканов в промышленности широко применяется каталитическое окисление алканов в результате которого получаются разнообразные кислородосодержащие соединения: спирты, карбоновые кислоты, альдегиды, кетоны и т. п. Данный процесс можно изобразить следующей схемой:


 Алкан Гидропероксид Спирт Альдегид
Алкан Гидропероксид Спирт Альдегид
Химик 4. (Сообщение учащегося).
3. Реакции разложения алканов
1. Пиролиз При сильном нагревании без доступа воздуха происходит полное разложение алканов на простые вещества.
t
 CH4 C + 2H2
CH4 C + 2H2
1. Крекинг
С 16Н34 С8Н18 + С8Н16
16Н34 С8Н18 + С8Н16
4. Отношение алканов к раствору перманганата калия и бромной воды.
Чтобы отличить предельные углеводороды от непредельных используют растворы перманганата калия и брома. Давайте посмотрим, что происходит при пропускании метана через эти растворы. (Просмотр видеоопытов)
Вывод: Предельные углеводороды не вступают в реакции присоединения. Для них характерны реакции замещения , окисления и разложения. Алканы не обесцвечивают раствор перманганата калия и бромную воду.
5.Выступление группы «Экологи и технологи».
Учитель: Экологи и технологи так и не разрешили спор: Алканы – это зло, или благо? Сейчас мы прослушаем их аргументы, и постараемся их примирить.
Технологи.(Сообщения учащихся).
Получение и применение алканов. Чаще всего алканы получают из природного газа. В промышленности метан можно получить из синтез-газа, а в лаборатории с помощью гидролиза карбида алюминия или сплавлением солей уксусной кислоты со щелочами.
Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека. Из одного только метана производят тысячи различных веществ. ( См. схему на слайде). Широко используются в промышленности и его гомологи. Газообразные алканы (метан и пpопан-бутановая смесь) используются в качестве ценного топлива. Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей. Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода до 15) - пpозpачная жидкость без запаха и вкуса, используется в медицине, паpфюмеpии и косметике. Вазелин (смесь жидких и твеpдых пpедельных углеводоpодов с числом углеpодных атомов до 25) пpименяется для пpиготовления мазей, используемых в медицине. Паpафин (смесь твеpдых углеводоpодов С19-С35) - белая твеpдая масса без запаха и вкуса (tпл= 50-70°C) - пpименяется для изготовления свечей, пpопитки спичек и упаковочной бумаги, для тепловых пpоцедуp в медицине и т.д. В современной нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Нормальные предельные углеводороды средней молекулярной массы используются как питательный субстрат в микробиологическом синтезе белка из нефти. Большое значение имеют галогенопроизводные алканов, которые используются как растворители, хладоагенты и сырье для дальнейших синтезов.
Экологи: «О вреде алканов».
Одним из основных источников загрязнения атмосферы является транспорт. Примерно 40 % всего общего антропогенного загрязнения атмосферы в России приходится на долю автомобильного транспорта. Топливо для двигателей внутреннего сгорания - бензин или дизельное топливо, полученное в результате переработки нефти, - состоит в основном из углеводородов. При полном сгорании топлива в качестве продуктов должны образовываться углекислый газ и вода. Так как для достижения максимальной мощности двигателя всегда используется избыток топлива, то часть его не окисляется до конца, в результате чего в атмосферу выбрасывается элементарный углерод (сажа) и оксид углерода (II), оказывающий вредное воздействие на организм человека. В состав бензина входят и алканы. Соединения углеводородов, выброшенных с выхлопными газами и представляющие собой смесь нескольких сотен химических соединений, являются причиной многих хронических заболеваний. Токсичны также и пары бензина, которые являются углеводородами. Углеводороды принимаю активное участие в образовании биологически активных веществ, вызывающих раздражение слизистых глаз, горла, носа и их заболевание, и наносящих вред окружающей нас среде.
Углеводородные соединения оказывают наркотическое действие на центральную нервную систему, могут быть причиной хронических заболеваний, а некоторые обладают отравляющими свойствами. Углеводороды при определенных метеорологических условиях активно способствуют образованию смога
Интересные факты: Американские ученые создали новый вид биотоплива, не отличающийся от обычного бензина, с помощью бактерий, перерабатывающих углеводы из различных типов промышленных и сельскохозяйственных отходов. Группа разработчиков сумела с помощью методов генной инженерии "научить" безвредные бактерии E.coli вырабатывать несвойственный им тип химических соединений - так называемых насыщенных углеводородов или алканов. Именно алканы являются ключевым компонентом бензина, а потому такое биотопливо может быть сразу после получения отправлено в распределительные сети заправочных станций, существующие сегодня.
Учитель: Так кто же из них прав? Алканы –это действительно благо для человечества или зло? Каково ваше мнение? ( Беседа с учащимися, которые высказывают свое мнение, учитель грамотно подводит их к выводу).
Сделаем вывод: Алканы необходимы человечеству, но только грамотное использование и новые технологии помогут избежать загрязнения окружающей среды при использовании их в промышленности и снизить опасность экологических катастроф.
Ш. Закрепление изученного материала.
1. Тест по теме «Алканы»
Готовимся к ЕГЭ!
1.Гомологический ряд алканов описывается общей формулой
а) СnH2n-2
б) CnH2n
в) СnH2n+2
г) CnH2n+1
2. В пропане связи углерод-углерод:
а) одинарные
б) двойные
в) полуторные
г) Пи-связи
3. Молекула метана имеет форму
а) пирамиды
б) параллепипеда
в) тетраэдра
г) конуса
4. Для алканов характерна гибридизация:
а) SP
б) SP2
в) SP4
г)SP3
5. Угол между атомами углерода в алканах составляет:
а) 120 градусов
б) 90 градусов
в) 109 градусов
г) 110 градусов
6. Углеводородный Радикал – это
а) группа атомов, соединённая с функциональной группой молекулы.
б) группа атомов, отличающаяся от метана на СН2-
в) группа атомов, имеющая положительный заряд
г) группа атомов, которая называется функциональной
7. Установите порядок для определения названия углеводорода
а) Определяют местонахождение радикалов
б) Выбирают самую длинную цепь и нумеруют атомы углерода в ней
в) Определяют корень названия по числу атомов углерода в длинной цепи
г) Составляют приставку в виде цифр и греческих числительных
8. Установите соответствие:
1. Пропан а) СН3-СН2-СН2-СН2-СН2-СН2-СН2- СН3
2. Пентан б) СН3-СН2-СН3
3. Бутан в) СН3-СН2-СН2-СН3
4. Октан г) СН3-СН2-СН2-СН2-СН3
9. Среди данных формул найдите 2 изомера:
а) СН3-СН2-СН2-СН2-СН3
б) СН3-СН2-СН2-СН3
в) СН3-СН-СН2-СН3
\
СН3
10. Формулы только алканов записаны в ряду:
а) С3Н6, С2Н4, С6Н14
б) С4Н10, С2Н6, С3Н8
в) С2Н2, С3Н8, С6Н6
г) С6Н6, С4Н8, С2Н6
Взаимопроверка учащихся. Правильные ответы:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| в | а | в | г | в | а | Б,а,г,в | 1-б, 2-а, 3-г 4-в | А,в | б |
2.Индивидуальная работа у доски.
Закончить уравнения, назвать получившиеся вещества, указать области их
применения.
А) C4H10 + O2 =
Б) этан + Cl2 =
В) C5 H12 →
(Если позволяет время, можно предложить и другие реакции или решить задачу).
3.Решите задачу: В состав органического вещества входит углерод, массовая доля которого – 92,23% и водород массовая доля которого 7,77%. Относительная плотность паров этого вещества по водороду равна 13. Определите молекулярную формулу вещества.
1У. Рефлексия. Подведение итогов урока.
Учитель: Сегодня на уроке вы изучили предельные углеводороды - алканы, узнали много нового, интересного об их строении, свойствах и получении. Познакомились с основными направлениями их использования человеком. Заканчивая наш урок, я хочу спросить вас, выполнили ли мы задачи, поставленные в начале изучения данной темы? Поднимите руки те, кому сегодня удалось расширить свои знания о алканах. Молодцы! А теперь определите свое место на «Горе успеха» сегодняшнего урока. . Я рада, что у большинства из вас настроение улучшилось и вы ощущаете себя покорителями вершины знаний. . Спасибо за урок, вы хорошо поработали.
У. Д/З: § 7-8 , упр. 13-17 (с. 28), задачи 1-2, ЕГЭ: 1.4.3. 1.4.4.
Анкетные данные:
1. Артеменко Вера Павловна,
2. Учитель химии МОУ СОШ № 28 г. Белгорода
3. 30.09.1964 года рождения,
4. Прож. 308000 г. Белгород, улица Белгородского полка д.25 кв.36, тел (4722 ) 33-80-36 дом. , 8-960-620-31-92(мобильный).
5. Паспорт: 1409 031803, выдан Отд. №3 ОУФМС России по Белгородской области г. Белгорода, 20.10.2009 года, адрес прописки: 308000 г. Белгород, улица Белгородского полка д.25 кв.36.
6. Страховое свидетельство государственного пенсионного страхования
№ 018-427-906-58
7. ИНН: 312304721500 от 11.05.2001 года, серия 31 № 000303874
16

 Получите свидетельство
Получите свидетельство Вход
Вход








 игзагообразная цепь атомов углерода, особенно в длинноцепочечных молекулах, может принимать различные пространственные формы.
игзагообразная цепь атомов углерода, особенно в длинноцепочечных молекулах, может принимать различные пространственные формы.
 Cl : Cl hv Cl . + Cl .
Cl : Cl hv Cl . + Cl .

















 Разработка урока "Алканы. Строение, свойства, применение" (1.99 MB)
Разработка урока "Алканы. Строение, свойства, применение" (1.99 MB)
 0
0 4132
4132 682
682 Нравится
0
Нравится
0


