
Химические свойства воды

I . Взаимодействие с металлами.
1. Щелочные и щелочно-земельные металлы бурно реагируют с водой при обычных условиях с образованием щёлочи и водорода.
2 Na + 2 H 2 O = 2 NaOH + H 2
гидроксид натрия
едкий натр
каустическая сода
Ca + 2 H 2 O = Ca ( OH ) 2 + H 2
гидроксид кальция
известковая вода
известковое молоко
гашёная известь
пушёнка
2К + 2Н 2 О = 2КОН + Н 2
гидроксид калия
едкое кали
Li вступает в реакцию медленно, Na – бурно, K может воспламениться за счет теплоты реакции, Rb и Cs реагируют со взрывом.

- Взаимодействие с металлами.
2. Металлы, стоящие в РСЭП от магния до водорода, реагируют с водой при температуре красного каления с образованием оксида металла и водорода.
до 570 0 С
3 Fe + 4 H 2 O = Fe 3 O 4 + 4 H 2
выше 570 0 С
Fe + H 2 O = FeO + H 2
Mg + H 2 O = MgO + H 2
раск частично растворяется в воде
Mg + 2H 2 O = Mg(OH) 2 + H 2
раск м/р
3. Амальгамированный алюминий (сплав алюминия со ртутью) бурно реагирует с водой при обычных условиях с образованием основания и водорода.
2 Al + 6 H 2 O = 2 Al ( OH ) 3 + 3 H 2
амальгам.
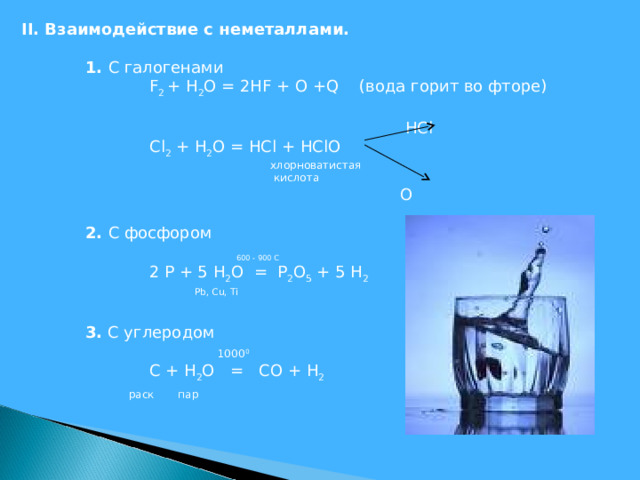
II . Взаимодействие с неметаллами.
1. С галогенами
F 2 + Н 2 О = 2НF + О + Q (вода горит во фторе)
HCl
Cl 2 + H 2 O = HCl + HClO
хлорноватистая
кислота
О
2. С фосфором
600 - 900 C
2 P + 5 H 2 O = P 2 O 5 + 5 H 2
Pb, Cu, Ti
3. С углеродом
1000 0
С + H 2 O = СО + H 2
раск пар

III . Взаимодействие с основными оксидами.
Оксиды щелочных и щелочно-земельных металлов образуют щёлочи.
Na 2 O + H 2 O = 2NaOH
CaO + H 2 O = Ca ( OH ) 2 (гашение)
негашёная
жжёная известь
кипелка
В aO + H 2 O = В a ( OH ) 2
баритова вода
IV . Взаимодействие с кислотными оксидами.
Образует кислоты с растворимыми кислотными оксидами.
SO 3 + H 2 O = H 2 SO 4 ( серная кислота )
SO 2 + H 2 O = H 2 SO 3 ( сернистая кислота )
CO 2 + H 2 O = H 2 CO 3 (угольная кислота)
P 2 O 5 + 3 H 2 O = 2 H 3 PO 4 (ортофосфорная)
Cl 2 O 7 + H 2 O = 2 HClO 4 (хлорная кислота)

- Взаимодействие с гидридами.
NaH + H 2 O = NaOH + H 2
CaH 2 + 2 H 2 O = Ca ( OH ) 2 + 2 H 2
- Взаимодействие с солями.
С некоторыми солями образует кристаллогидраты (вещества, содержащие в своём составе кристаллизационную воду), с другими протекает гидролиз.
CuSO 4 + 5H 2 O = CuSO 4 . 5H 2 O
белый голубой
CuSO 4 . 5H 2 O – медный купорос
AlCl 3 + H 2 O = Al(OH)Cl 2 + HCl

VII . Гидролиз бинарных соединений.
Al 2 S 3 + 6 H 2 O = 2 Al ( OH )3 ↓ + 3 H 2 S ↑
Mg 3 N 2 + 6 H 2 O = 3 Mg ( OH ) 2 + 2 NH 3 ↑
Ca 3 P 2 + 6H 2 O = 3Ca(OH) 2 + 2PH 3 ↑
Al 4 C 3 + 12H 2 O = 4Al(OH) 3 ↓ + 3CH 4 ↑
CaC 2 + 2H 2 O = Ca (OH) 2 + C 2 H 2 ↑
Mg 2 Si + 4H 2 O = 2Mg(OH) 2 + SiH 4 ↑
VIII. Электролиз воды.
эл.ток
2 H 2 O = 2 H 2 + O 2

 Получите свидетельство
Получите свидетельство Вход
Вход











 Презентация "Химические свойства воды" (2.44 MB)
Презентация "Химические свойства воды" (2.44 MB)
 0
0 2450
2450 147
147 Нравится
0
Нравится
0


