
Красноярская средняя школа № 1
Жирнова Лариса Николаевна
учитель химии
высшей категории


Цель:
Ознакомление с разнообразием представителей данного класса, изучение общих черт строения, классификации, номенклатуры, физических свойств и областей применения карбоновых кислот на основе имеющихся знаний о некоторых особенностях наиболее распространенных карбоновых кислот, результатов лабораторных опытов, теоретических и практических исследований.

Тест
1 . К классу предельных альдегидов принадлежит вещество состава
1) С n H 2 n -2 O 3) С n H 2 n O
2) С n H 2 n +2 O 4) С n H 2 n O 2
2 . Вещество состава С 2 Н 4 О может быть
1) многоатомным спиртом 3) кислотой
2) альдегидом 4) простым эфиром
3. Гомологом бутаналя является
1) пропаналь 3) бутанол-1
2) бутанон 4) бутан
4. Для пропаналя характерна изомерия
1) углеродного скелета 3) межклассовая
2) геометрическая 4) оптическая
5. Число σ-связей в молекуле ацетальдегида равно
1) 2 3) 5
2) 3 4) 6
6 . Для формальдегида не характерны реакции
1) присоединения 3) окисления
2) замещения 4) восстановления

7 . При нагревании ацетальдегида со свежеосаждённым гидроксидом меди( II )
наблюдается
1) появление жёлтого, а затем красного осадка
2) превращение голубого осадка гидроксида меди( II ) в чёрный
3) растворение осадка и образование голубого раствора
4) растворение осадка и образование васильково-синего раствора
8. Образование «серебряного зеркала» в реакции с аммиачным раствором оксида
серебра доказывает, что в молекуле вещества содержится
1) карбоксильная группа 3) альдегидная группа
2) двойная связь между атомами С и О 4) атом углерода в sp 2 -гибридном состоянии
9. При окислении пропаналя образуется
1) пропан 3) пропановая кислота
2) пропанол-1 4) пропанол-2
10. С помощью аммиачного раствора оксида серебра можно различить растворы
1) метанола и этанола 3) ацетальдегида и пропаналя
2) этанола и этаналя 4) глицерина и этиленгликоля
11. С гидроксидом меди( II ) реагируют оба вещества
1) глицерин и пропаналь 3) этанол и фенол
2) ацетальдегид и этанол 4) фенол и формальдегид
12. При восстановлении бутаналя получается
1) бутанол-1 2) бутановая кислота 3) бутанол-2 4) дибутиловый

Ответы:
1-----3
2-----2
3-----1
4-----3
5-----4
6-----2
7------1
8------3
9------3
10-----2
11-----1
12-----1

Баллы Оценка
11—12 ----------- «5»
8---10 ----------- «4»
4----7 ----------- «3»
0 ---3 ----------- «2»
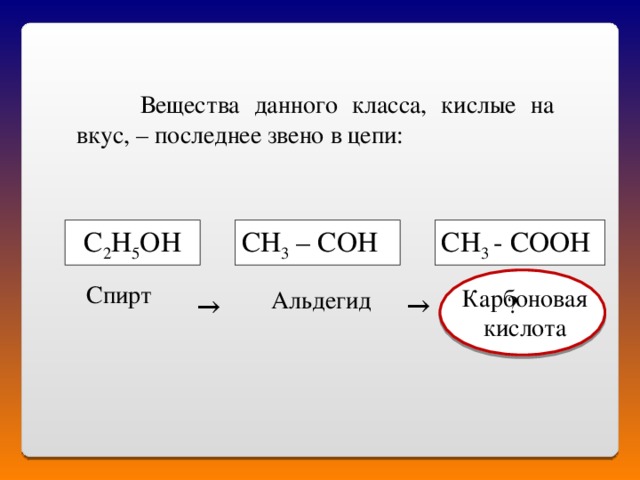
Вещества данного класса, кислые на вкус, – последнее звено в цепи:
CH 3 – COH
CH 3 - COOH
C 2 H 5 OH
Спирт
Карбоновая кислота
Альдегид
→
?
→

Почему данные кислоты имеют первое слово
« КАРБОНОВЫЕ »?

НООС – CH – CH 2 – COOH
׀
OH
2 –гидрокси –бутандиовая кислота

С H 3 – CH – COOH
׀
OH
2 – гидрокси пропановая кислота

OH
׀
HOOC – CH 2 – C – CH 2 - COOH
׀
COOH
3 - гидрокси пентантриовая кислота

HOOC – CH – CH – COOH
│ │
ОН ОН
2,3 - дигидрокси бутандиовая кислота












Ежедневно делайте зарядку для глаз от 2 до 5 минут!
Будьте здоровы!

ИНСТРУКТИВНАЯ КАРТА № 1
Карбоновые кислоты: определение, классификация, гомологические ряды
- Напишите общую формулу для карбоновых кислот. Дайте определение понятию “карбоновые кислоты”.
2. Напишите структурные формулы простейшей карбоновой кислоты и 3 ее ближайших гомологов, их номенклатуры. Выделите функциональную группу.
3. Какие названия кислот по тривиальной номенклатуре вам уже известны? Каково в большинстве случаев, происхождение этих названий? Познакомиться с принципами международной номенклатуры ИЮПАК и тривиальными названиями карбоновых кислот.
4. На листе ватмана оформите опорный конспект по вашей теме, подготовьте краткое сообщение на 5 минут.


ИНСТРУКТИВНАЯ КАРТА № 2
Карбоновые кислоты: изомерия, номенклатура
1. Составьте все возможные структурные формулы органических соединений, соответствующие формуле С 5 Н 10 О 2 . Сделайте вывод о видах изомерии предельных карбоновых кислот.
2. Изучите физические свойства уксусной кислоты по плану:
- Определите агрегатное состояние вещества при н. у.
- Изучите цвет вещества и его прозрачность
- Определите наличие запаха
Вспомните, как правильно определять запах!
- Проверьте растворимость кислоты в воде
- Опишите результаты исследования:
Агрегатное состояние __________________
Цвет _____________________
Запах ____________________________
Растворимость в воде __________________________
3. На листе ватмана оформите опорный конспект по вашей теме, подготовьте краткое сообщение на 5 минут.


ИНСТРУКТИВНАЯ КАРТА № 3
Карбоновые кислоты: общие способы получения
- Вспомните и напишите уравнения реакций получения уксусной кислоты из представителя: а) спиртов, в) альдегидов. Укажите особенности условий протекания реакций.
Какие окислители могут быть использованы в этих случаях?
На основании выполненных упражнений обобщите способы получения карбоновых кислот.
- Перечислите области применения карбоновых кислот:
3. На листе ватмана оформите опорный конспект по вашей теме, подготовьте краткое сообщение на 5 минут.



Что вы знаете о функциях аскорбиновой кислоты и содержании ее в продуктах питания?
Суточная норма, рекомендуемая для потребления аскорбиновой кислоты – 60 мг.

ИНСТРУКТИВНАЯ КАРТА № 4
Карбоновые кислоты: химические свойства
(на примере уксусной кислоты)
- Проведите химические реакции и запишите уравнения химических реакции
- 1. Взаимодействие с карбонатом натрия
- 1. Взаимодействие с карбонатом натрия
1.2. Взаимодействие с гидроксидом натрия
1.3. Взаимодействие с магнием
1.4. Взаимодействие с оксидом железа
2. На листе ватмана оформите опорный конспект по вашей теме, подготовьте краткое сообщение на 5 минут.

Некоторые лекарственные препараты нельзя запивать целым рядом напитков, в том числе кислые фрукты и соки, маринады, блюда с уксусом нельзя употреблять в пищу наряду с антибиотиками пенициллинового ряда и эритромицином.
Как вы думаете, чем вызван данный запрет?
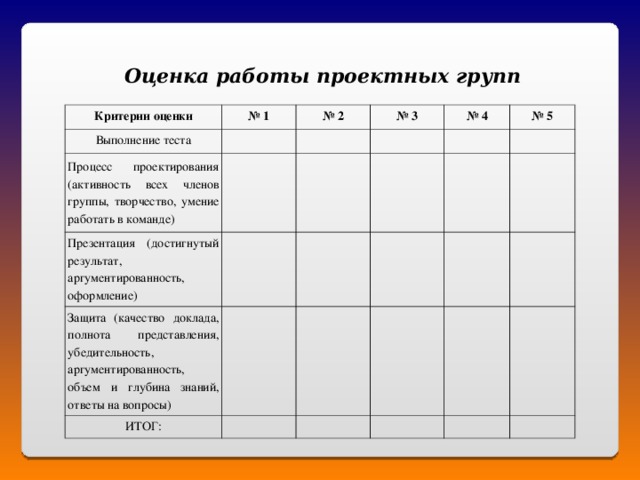
Оценка работы проектных групп
Критерии оценки
№ 1
Выполнение теста
№ 2
Процесс проектирования (активность всех членов группы, творчество, умение работать в команде)
№ 3
Презентация (достигнутый результат, аргументированность, оформление)
№ 4
Защита (качество доклада, полнота представления, убедительность, аргументированность, объем и глубина знаний, ответы на вопросы)
ИТОГ:
№ 5

Домашнее задание:
стр. 193 – 201
упр. 1, 2, 5, 6, 7 стр. 211

Рефлексия



 Получите свидетельство
Получите свидетельство Вход
Вход


















































 Кислоты карбоновые (2.99 MB)
Кислоты карбоновые (2.99 MB)
 0
0 1573
1573 123
123 Нравится
0
Нравится
0








