Катализаторы и катализ
Каждый из вас, наверняка, слышал такую народную мудрость: «Умный в гору не пойдёт, умный гору обойдёт»? Она как раз подходит к нашему уроку, посвящённому катализаторам. Вспомните, катализаторы – это вещества, которые изменяют скорость химической реакции, но сами при этом не расходуются. Все химические реакции, которые протекают в присутствии катализатора, называются каталитическими.
Вы, конечно, же, помните, чтобы вещества начали взаимодействовать друг с другом, их частицам нужно сообщить определённую энергию, которая называется энергией активации.

Катализаторы понижают эту энергию, потому что они соединяются с одним из реагирующих веществ и проводят его вдоль «энергетической горы» на встречу с другим веществом с меньшими затратами энергии. Поэтому в присутствии катализатора химические реакции протекают не только быстрее, но и при более низкой температуре. Т.е., катализаторы ускоряют химические реакции, но сами остаются неизменными.

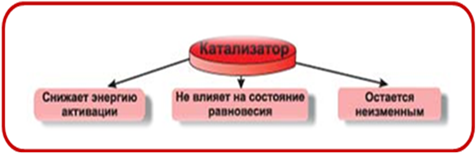
Использование катализатора приводит к тому, что одни и те же вещества будут реагировать по-разному.
Например, реакция окисления аммиака. Обычно, при горении аммиака образуется азот и вода, но в присутствии катализатора аммиак окисляется до оксида азота (II) и воды.


Большую часть продукции, производимой химическими производствами, получают на основе использования катализаторов. Каталитическими являются процессы получения серной кислоты, азотной кислоты, синтетического каучука, пластмасс, лекарственных препаратов, получение из твёрдого угля жидкого топлива, переработки нефти и природного газа.
Биологические катализаторы белковой природы называются ферментами. Они участвуют в сложных процессах, протекающих в пищеварительной системе, крови и клетках животных и человека.
Например, слюна содержит фермент птиалин, который катализирует превращение крахмала в сахар. Если пожевать хлеб или картофель дольше обычного, то во рту можно почувствовать сладкий вкус. Желудочный сок содержит пепсин, который катализирует расщепление белков. В организме человека около тридцати тысяч различных ферментов, каждый из них – катализатор соответствующей реакции. В живом организме благодаря ферментам все биологические процессы протекают при обычных условиях.
Сам процесс изменения скорости химической реакции или пути, по которому она протекает, называется катализом. Важной характеристикой каталитической реакции (катализа) является однородность и неоднородность катализатора и реагирующих веществ.
Поэтому различают:
· гомогенный
· гетерогенный катализ
При гомогенном (однородном) катализе реагирующие вещества и катализатор находятся в одном агрегатном состоянии, а при гетерогенном катализе у них разное агрегатное состояние.
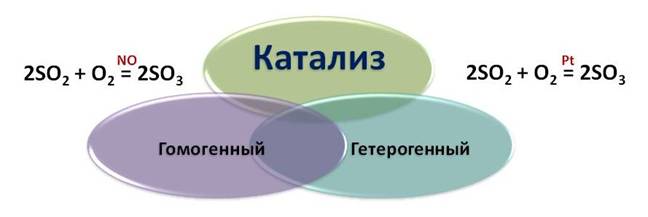
Если используют ферменты в катализе, тогда он называется ферментативным.
Этот вид катализа известен человеку с глубокой древности. Благодаря ферментативному расщеплению органических веществ, человек научился печь хлеб, варить пиво, изготавливать вино и сыр. В стиральных порошках тоже используют ферменты, именно они позволяют избавиться от пятен.




Ребята, конечно же, в каждой аптечке вы можете увидеть пероксид водорода (Н2О2), в повседневной жизни его часто называют перекисью водорода. На его упаковке всегда указан срок годности, потому что со временем он разлагается на воду и кислород. Однако этот процесс протекает очень медленно, и увидеть выделение газа кислорода вы сможете, если откроете сосуд, где долгое время хранился пероксид водорода. Но если в сосуд, где находится пероксид водорода добавить оксид марганца (IV), то реакция разложения сразу же протекает.
MnO2
2H2O2 = 2H2O + O2
Попробуем поэкспериментировать? Для этого, нальём в стаканчик раствора перекиси водорода, а затем сюда же добавим немного порошка оксида марганца (IV), после чего мы можем наблюдать бурное выделение пузырьков газа. Чтобы доказать, что выделившийся газ является кислородом, поднесём к верхней части стаканчика тлеющую лучинку, лучинка вспыхнет из-за скопившегося кислорода.
Попробуйте охарактеризовать эту реакцию по всем признакам классификации.
Так, эта реакция разложения, потому что из одного исходного сложного вещества (пероксида водорода) образуются новые: сложное вещество (вода) и новое простое вещество (кислород). Эта реакция необратимая, т.к. протекает только в одном направлении (между левой и правой частью уравнения стоит знак равенства). Эта реакция экзотермическая, т.к. протекает с выделением незначительного количества теплоты, ведь в опыте не требуется нагревание.

Эта реакция окислительно-восстановительная, потому что кислород изменяет свою степень окисления: с -1 до -2 и до 0, поэтому кислород одновременно является и окислителем и восстановителем в этой реакции.

Эта реакция гетерогенная, т.к. в результате разложения образуется жидкость и газ. Реакция является каталитической, т.к. катализатор участвует в этой реакции.
Само собой разумеется, что это гетерогенный катализ, потому что катализатор и катализируемое вещество находятся в разных агрегатных состояниях.

Кроме этого, различные опыты показали, что катализаторы строго специфичны для конкретных реакций.
Например, в реакции получения аммиака из водорода и азота катализатором является железо, при получении оксида серы (VI) из оксида серы (IV) катализатором является оксид ванадия (V).
В уравнениях химических реакций формулы катализаторов записывают над знаком равенства или обратимости или пишут «катализатор».

Катализатором реакции взаимодействия алюминия и йода является обычная вода. Если к порошку алюминия добавить йод, а затем прилить несколько капель воды, то вещества бурно реагируют.

Кусочки моркови, мяса, картофеля разлагают пероксид водорода с выделением кислорода. Это действует фермент каталаза. Фермент каталаза содержится почти во всех растительных и животных клетках, но при варке он разрушается.

Давайте с вами, проведём небольшой эксперимент. Мы исследуем некоторые пищевые продукты на наличие в них фермента каталазы. Нальём в шесть пробирок раствора перекиси водорода. И поместим по очереди: в первую – кусочек сырого картофеля, во вторую – кусочек варёного картофеля, в третью – кусочек сыра, в четвёртую – дрожжей, в пятую – кусочек сырой печени, в шестую – варёной печени. Посмотрим, что же будет происходить.

В первой, четвёртой и пятой пробирке мы можем наблюдать вскипание раствора, в остальных ничего не происходит. Почему? При нагревании фермент каталаза разрушается, поэтому в переработанных продуктах его нет, и разложение перекиси водорода не происходит.
Если в пробирку с раствором перекиси водорода добавить несколько капель морковного сока, то происходит характерное вскипание раствора из-за выделяющегося кислорода. Это вскипание произошло из-за того, что морковный сок не подвергался термической обработки и в нём сохранился фермент каталаза. Естественно, что в данном случае протекает гомогенный катализ, ведь перекись и сок находятся в одном агрегатном состоянии.

Катализаторы не только удешевляют производственные процессы, но и вносят вклад в охрану окружающей среды. Так, современные автомобили снабжены каталитическим устройством, внутри которого находятся керамические ячеистые носители катализатора (платины и родия). Проходя через них, различные вредные вещества превращаются в углекислый газ, азот и воду.

Для химических процессов важны не только катализаторы, которые ускоряют реакции, но и вещества, способные их замедлять. Такие вещества называются ингибиторами. Чаще всего используются ингибиторы коррозии металлов.
Мы с вами сами сможем убедиться в действии ингибиторов. Проведём эксперимент: поместим в две пробирки по грануле цинка и нальём в каждую раствора серной кислоты. А затем в первую пробирку добавим немного уротропина. Что же мы видим? В первой пробирке значительно меньше выделяется водород. Значит, уротропин является ингибитором и значительно замедлил процесс взаимодействия цинка с серной кислотой.
Zn + H2SO4 = ZnSO4 + H2↑
Кроме этого, в жизни мы часто используем и такие понятия, как антиоксидант или антиокислитель.
Что же представляют собой эти вещества? Вы, наверное, замечали, что если долго хранить сливочное масло на воздухе, то постепенно оно изменяет цвет, вкус, приобретает неприятный запах, это всё происходит из-за процессов окисления. Поэтому, чтобы продукты не портились, в них добавляют антиоксиданты.
В организме человека также происходят процессы окисления, что ведёт к различным заболеваниям и старению организма. Человек получает антиоксиданты с продуктами питания, содержащих каротин (витамин А), витамин Е.



Теперь вам будут понятны такие термины, как катализаторы, катализ (гомогенный и гетерогенный), ингибиторы и ферменты.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 18642
18642

