Понятие об аминокислотах. Белки
Аминокислоты – это органические соединения, содержащие карбоксильную группу – СООН и аминогруппу – NH2.
Поэтому состав аминокислот можно выразить формулой NH2 – CH – COOH
|
R

Аминокислоты можно рассматривать как производные карбоновых кислот, у которых атом водорода в радикале замещён на аминогруппу.
Например из уксусной кислоты получается аминоуксусная кислота NH2 – CH2 – COOH.

Карбоксильная группа и аминогруппа определяют химические свойства аминокислот. Так аминогруппа определяет основные свойства вещества, потому что может присоединять к себе катион водорода за счёт наличия свободной пары электронов у азота. А карбоксильная группа определяет кислотные свойства аминокислот.

Поэтому аминокислоты – это органические вещества, которые обладают основными и кислотными свойствами, так как содержат амино- и карбоксильную группу. То есть аминокислоты являются амфотерными соединениями.
Аминокислоты – бесцветные кристаллические вещества, хорошо растворимы в воде и малорастворимы в органических растворителях. Они могут быть сладкими, безвкусными и горькими.
Аминокислоты – это кирпичики, из которых строятся молекулы белков. Благодаря наличию кислотной и основной групп молекулы аминокислот взаимодействуют друг с другом и образовывают полимеры – белки.


Это реакция поликонденсации. Таким образом, реакции поликонденсации – это реакции получения полимеров, которые сопровождаются образованием побочного низкомолекулярного соединения, например воды.
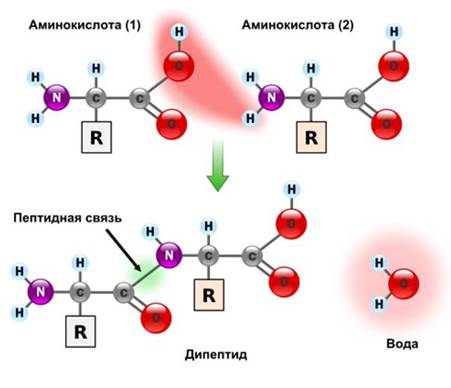
При образовании дипептида между остатками аминокислот возникает связь, которую называют пептидной. Она образуется между остатком карбоксильной группы одной аминокислоты (-СО-) и остатком аминогруппы (-NH-) другой аминокислоты (– СО – NH –).
Эта связь повторяется в полимере много раз, поэтому полимер и называется полипептидом.
Из остатков аминокислот строятся полипептиды – белки. Поэтому при расщеплении белков образуются аминокислоты.
Например, немецкий химик-органик и биохимик Э.Г. Фишер, который является лауреатом Нобелевской премии, занимался химией углеводов и белков. Он синтезировал ряд физиологически активных веществ, внедрял в синтез химических соединений ферменты.

Существует более двадцати аминокислот, а белков множество. Каждый организм имеет свой собственный неповторимый набор белков, который лишь иногда бывает схожим у близких родственников. Как тридцать три буквы алфавита образуют множество слов, так и двадцать аминокислот образуют множество белков благодаря чередованию аминокислот.

Так, определённая последовательность чередования аминокислот определяет первичную структуру белка.
Большая заслуга в изучении в открытии строения белковой молекулы принадлежит русскому биохимику А.Я. Данилевскому. Это русский биохимик, один из основоположников отечественной биохимии. Он работал в области химии ферментов и белков.

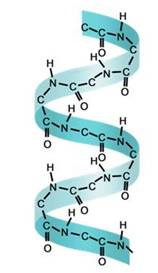
Вторичная структура белка – это упорядоченное свёртывание полипептидной цепи в спираль. В расшифровке вторичной структуры белка принимали участие многие выдающиеся учёные разных стран. В середине двадцатого века было доказано существование в белке вторичной структуры. За исследование природы химической связи во вторичной структуре белка Л. Полинг получил Нобелевскую премию.
Третичная структура белка – более сложная конфигурация, чем спираль. Она напоминает по форме клубок.

Четвертичная структура – это несколько полипептидных цепей, расположенных в пространстве. Пример четвертичной структуры белка – гемоглобин.

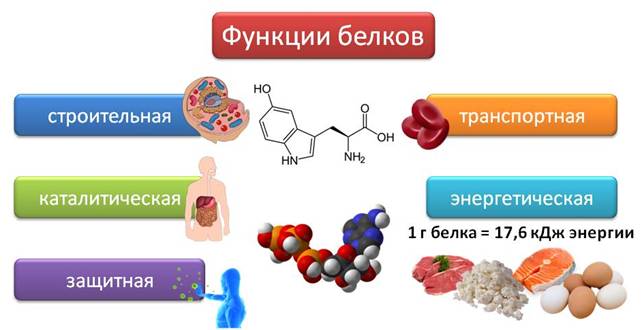
Белки выполняют ряд функций в организме. Прежде всего, это строительная функция, ведь белки являются составной частью оболочки, ядра, цитоплазмы, клеточного сока, семян.
Все наиболее значимые процессы в организме идут с помощью биологических катализаторов – ферментов. Поэтому белки выполняют ещё и каталитическую функцию.
Немаловажной функцией белков является защитная функция. Особые белки – антитела и антитоксины участвуют в формировании защитного свойства организма – иммунитета.
Такой белок крови, как гемоглобин является переносчиком кислорода, поэтому он выполняет транспортную функцию.
Кроме этого, белки выполняют ещё и энергетическую функцию, так как при распаде белков до конечных продуктов выделяется энергия. При полном расщеплении один грамм белка выделяется 17,6 кДж энергии. Главными поставщиками белков служит мясо, рыба, яйца, творог.
Белки способны гидролизоваться до аминокислот, то есть разлагаться водой в присутствии кислот или щелочей. В результате гидролиза разрушается первичная структура белка.

Для белков характерно такое свойство, как денатурация. Это разрушение белка при нагревании или изменении кислотности среды, при действии радиации, щелочей, солей тяжёлых металлов. Этот процесс можно наблюдать при варке яиц (повышение температуры) или при скисании молока (изменение кислотности среды). При денатурации сохраняется первичная структура белка.
Белки горят и при этом появляется запах горящего рога и жжённого пера.
Для белков характерны цветные реакции, которые являются качественными реакциями на белки.
Если налить в пробирку раствора белка и прибавить несколько капель концентрированной азотной кислоты, то образуется белый осадок. Если нагреть содержимое пробирок, то белый осадок окрашивается в жёлтый цвет. Если этот раствор охладить и добавить концентрированный раствор аммиака, то окраска становится оранжевой. Это так называемая ксантопротеиновая реакция. Эта реакция доказывает наличие бензольных колец в остатках аминокислот.
Если в пробирку налить раствора белка и добавить столько же раствора щёлочи, а затем несколько капель раствора медного купороса, то белок окрашивается в красно-фиолетовый цвет. Эта качественная реакция на белок называется биуретовой. Эта реакция указывает на наличие в белках пептидных связей.
Белки различны по растворимости в воде. Например, белки шерсти, шёлка, ногтей, рога, перьев – нерастворимы в воде, а белки крови, лимфы, пищеварительных соков – растворимы.

Белки – не только питательные вещества для человека и животных, но и сырьё для промышленности. Из шерсти изготавливают ткани, а из рога – пуговицы и гребни. Белки кожи и хрящей идут на изготовление клея. Желатин употребляется в пищевой промышленности, а также при изготовлении фотоплёнки и фотобумаги. Кожи животных используют в кожевенной промышленности.

Таким образом, аминокислоты – это органические амфотерные соединения, содержащие в составе молекулы две различные фуекциональные группы – карбоксильную и аминогруппу. Аминокислоты могут взаимодействовать друг с другом с образованием пептидов. Белки – это полипептиды, построенные из остатков аминокислот. Различают первичную, вторичную, третичную и четвертичную структуру белка. Белки подвергаются гидролизу, денатурации, им свойственны цветные реакции.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 7677
7677


