Алканы относятся к насыщенным углеводородам, то есть к органическим соединениям, в составе которых содержаться только одинарные С – С связи.
Наиболее часто в природе встречается метан. Он представляет собой бесцветный газ, который легче воздуха, не имеет запаха. Метан образуется в природных условиях при разложении без доступа воздуха остатков растительных и животных организмов. Метан ещё называют болотным газом из-за того, что в небольшом количестве он выделяется в заболоченных местах. Больше всего метана в природном газе, там его содержание достигает 95 %. Метан вместе с этаном, пропаном и бутаном содержится в попутных нефтяных газах и в угольных пластах.
Высшие алканы входят в состав пчелиного воска, восковых покрытий листьев, плодов и семян растений, они встречаются также в виде озокерита.
Все насыщенные углеводороды образуют ряд, в котором любой член ряда отличается на одну или несколько групп – СН2 –, которая называется гомологической разностью. Сам ряд углеводородов называется гомологическим рядом, а члены гомологического ряда – гомологами. Первые представить этого ряда – метан, второй – этан, третий член ряда – пропан, а четвёртый – бутан. Состав гомологического ряда алканов можно выразить общей формулой CnH2n+2. Буква n показывает число атомов углерода, которые содержатся в молекуле конкретного углеводорода. Например, в молекуле гептана содержится 7 атомов углерода, значит его молекулярная формула С7Н16.
Рассмотрим электронное и пространственное строение алканов. Например, молекулярная формула метана СН4. Связи между атомом углерода и водорода являются равноценными и называются σ-связями. В электронной формуле метана валентные связывающие электроны показаны в виде точек. Каждая химическая связь изображается чёрточкой при записи структурной формулы.
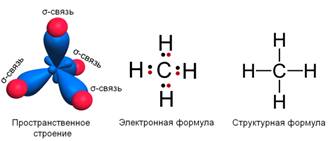
Установлено, что молекула метана имеет тетраэдрическое строение. В центре тетраэдра – атом углерода, а атомы водорода находятся в вершинах тетраэдра. Такое расположение связей обусловлено взаимным отталкиванием электронных облаков связей С – Н.

Пространственное строение других алканов аналогичное. Например, у пропана такое же тетраэдрическое строение, углы между связями 109028´, поэтому атомы углерода находятся не по прямой линии, а зигзагообразно. Особенностью одинарной связи между атомами углерода является возможность свободного вращения атомов вокруг этой связи, поэтому углеродная цепь алканов может принимать различную форму. Длина этой углерод-углеродной связи С – С в молекуле алканов равна 0,154 нм.

Алканы могут иметь неразветвлённое и разветвлённое строение. Названия алканов по Международной номенклатуре образуются добавлением суффинка – ан к греческим названиям чисел, которые показывают число атомов углерода в составе молекулы. Первые четыре представителя гомологического ряда алканов имеют тривиальные названия: с одним атомом углерода – метан, двумя – этан, тремя – пропан и четырьмя – бутан.
Радикалы, или алкильные группы имеют названия такие же, как названия алканов, только суффикс –ан заменяется на суффикс –ил. Например, радикал – СН3 называется метил, с двумя атомами углерода – этил, с тремя – пропил или изопропил и так далее.
Для того, чтобы назвать алкан нужно выбрать самую длинную цепь, нумерацию начинают с того конца, где ближе заместители. Затем называют заместители в алфавитном порядке.
Назовём следующий углеводород.

Определяем слева или справа начинать отсчёт. Заместители ближе с правой стороны, поэтому отсчёт начинаем справа налево. От третьего атома углерода отходят два одинаковых заместителя. Поэтому название этого углеводорода будет 3,3-диметилгексан.
Приведём ещё один более сложный пример названия алкана.

Первое, что нужно сделать – это найти главную цепь, то есть цепь, имеющую самое большое число атомов углерода. Предположим, начнём отсчёт слева. Главная цепь содержит 10 атомов углерода. Теперь попробуем пронумеровать справа. Главная цепь и в этом случае содержит 10 атомов углерода. Выбираем за главную цепь ту, которая содержит большее число разветвлений. Обозначим заместители. Их всего 5. У нас есть заместители, которые называются метил, этил и пропил. Слева заместители отходят от третьего атома углерода, справа – от второго. Приоритет отдаётся тому направлению, где ближе первое разветвление. Значит, нумерацию начинаем справа. Согласно правилам современной номенклатуры, названия радикалам нужно давать в том порядке, в каком они находятся по алфавиту. Получается, что первым мы будим называть метил, потом, пропил, в последнюю очередь – этил. Так как метил не один, а их три, то название углеводорода будет следующим: 2,6,8-триметил, далее у пятого атома углерода радикал пропил, поэтому 5-пропил, 8-этилдекан.

Для алканов, как и для других органических соединений, характерно явление изомерии, то есть явление существования различных соединений, имеющих один и тот же качественный и количественный состав, но разное строение.
Для насыщенных углеводородов – алканов изомерия начинается с бутана. Например, у бутана и изобутана одна и та же молекулярная формула – С4Н10, но разное химическое строение. Так, в бутане с неразветвлённой цепью атомов центральный атом связан с двумя атомами углерода, а в изобутане, где разветвлённая цепь атомов, центральный атом связан с тремя атомами углерода. Поэтому бутан и изобутан являются изомерами. Кроме того, что у этих веществ различное строение, они ещё имеют и различные свойства.

Различают изомерию структурную и пространственную. Одним из видов структурной изомерии является изомерия углеродного скелета. Так, у пентана есть 3 изомера. Это нормальный пентан, который имеет неразветвлённую цепь атомов углерода, 2-метилбутан, или изопентан, а также 2,2-диметилпропан, или неопентан.

Если посмотреть гомологический ряд алканов, то можно увидеть, что первые четыре члена этого ряда являются газами и имеют температуру кипения ниже комнатной. Алканы с С5 – С15 – жидкости, а алканы, которые имеют 16 и более атомов углерода – твёрдые вещества. С увеличение относительной молекулярной массы температуры плавления и кипения увеличиваются. Алканы практически не растворимы в воде.
Таким образом, общая формула алканов CnH2n+2. Длина С – С связи равна 0,154 нм. Для метана и его гомологов характерно тетраэдрическое строение. Основу названия алканов определяет самая длинная цепь атомов углерода, начиная с того конца, где ближе находится заместитель. Для алканов характерна изомерия углеродного скелета.

 Получите свидетельство
Получите свидетельство Вход
Вход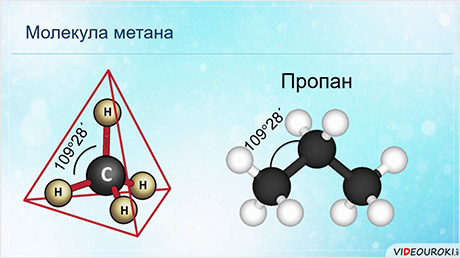



 0
0 14949
14949

