
3 октября 2012 г
7 класс
Учитель: Чупра Н. Б.

До XX века ученые считали, что все вещества могут находиться в одной из трех фаз — газообразной, жидкой или твердой. Именно эти фазы и названы агрегатными состояниями вещества.
Однако современная наука шагнула далеко вперед и теперь известно о существовании десятка агрегатных состояний вещества, а по поводу нескольких состояний идут жаркие споры о том, считать их агрегатными или нет.
Сейчас все мы уверенно вспоминаем целых четыре агрегатных состояния, которые теоретически могут принимать любые вещества. Это газ, жидкость, твердая фаза и плазма. В каждой из фаз одно и то же вещество по-разному ведет себя в физическом и химическом отношении, что и дает право говорить именно о качественно разных состояниях.

Цели урока:
Обучающая: сравнить свойства и выяснить особенности молекулярного строения одного и того же вещества в разных агрегатных состояниях.
Развивающая: Обратить внимание учащихся на окружающие нас вещества, и стремиться к объяснению их свойств в разных агрегатных состояниях.
Воспитывающая: Продолжать формировать навыки четких ответов на вопросы, выделять главное в изучаемом материале.

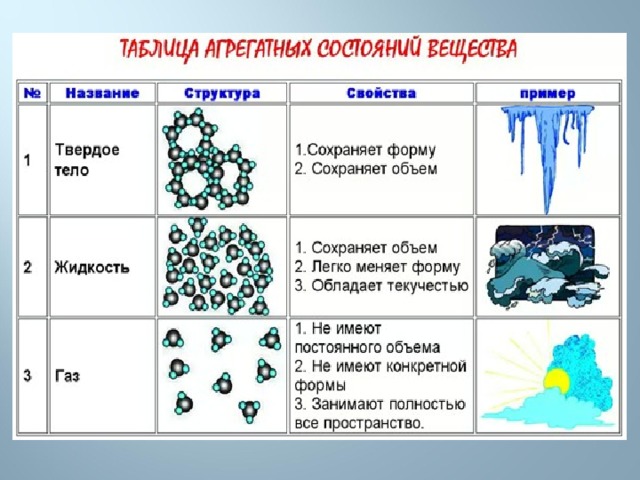
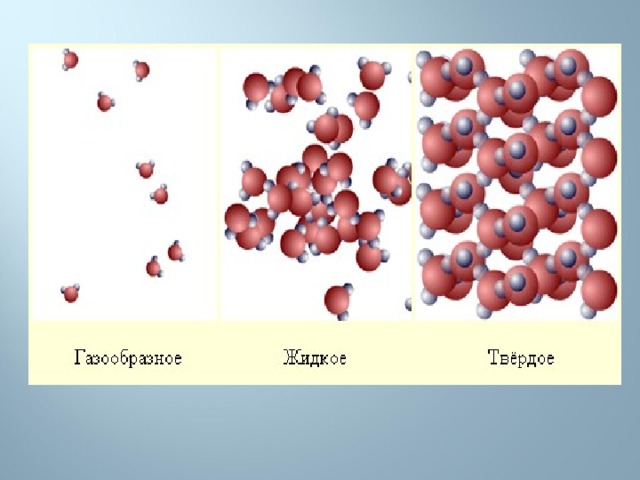
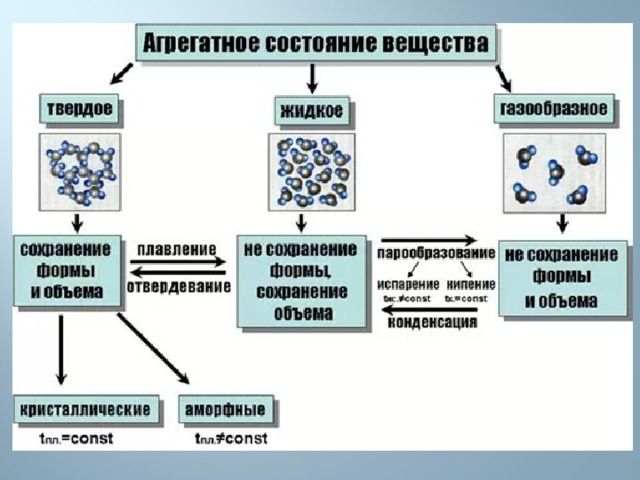
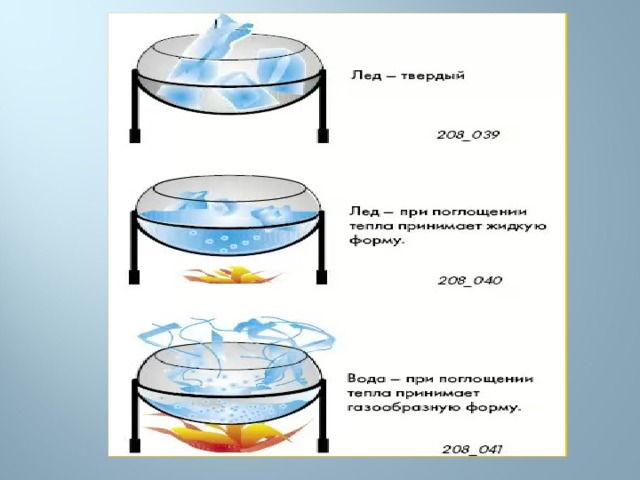
В газе молекулы или атомы вещества находятся на расстояниях, в десятки раз превышающих размеры частиц. Такое состояние возможно выше температуры кипения данного вещества — в теории можно «вскипятить» и превратить в пар даже самые тугоплавкие металлы. Газы не могут сохранять форму и объем - они полностью занимают предоставленное им пространство. При этом любой газ очень легко подвергнуть сжатию, а при приложении определенных сил это сжатие приведет к сжижению.

В жидкости расстояния между молекулами примерно сравнимы с размерами самих частиц, поэтому жидкости почти не сжимаются и не заполняют весь предоставленный им объем, как это делают газы. При повышении температуры жидкость превращается в газ, а при понижении — в твердое тело. Это правило соблюдается не всегда, о чем речь пойдет несколько ниже, при описании сверхкритического флюида.

В твердых телах атомы, ионы или молекулы расположены в строгом порядке, образуя кристаллическую решетку. Именно поэтому твердые тела могут сохранять свою форму и обладают такими качествами, как твердость, прочность, пластичность и т. д.

Плазма — это высокотемпературное состояние вещества, обладающее уникальными характеристиками. В плазме нельзя говорить об атомах или молекулах, так как происходит частичная или полная ионизация, то есть потеря атомами электронов. Проще говоря, в плазме существуют отдельно электроны, ионы (атомы, потерявшие внешние электроны) и даже «голые» атомные ядра (это возможно при крайне высоких температурах).


Именно эти четыре фазы веществ окружают нас в обычной жизни. Однако мало кто знает, что существуют еще более экзотические агрегатные состояния, в которых вещество приобретает удивительные свойства.
Сверхкритический флюид — нечто среднее между жидкостью и газом. Такое состояние получается при определенных давлениях и температурах, наблюдаемых в так называемой критической точке. Сверхкритический флюид очень плотен, но его вязкость близка к вязкости газов, он обладает высочайшей растворяющей способностью и крайней текучестью. Интересно, что вещества в этом состоянии (например, сверхкритическая вода) не являются лабораторной диковинкой, а активно применяются в различных областях промышленности.

Конденсат Бозе — Эйнштейна представляет собой бозонную жидкость, охлажденную почти до абсолютного нуля («почти» — это миллионные доли градуса выше нуля). Вещество в таком состоянии начинает «искать» наиболее выгодную, с энергетической точки зрения, позицию, вследствие чего может перемещаться без трения, вытекать из сосудов по стенкам и т. д.
Еще одним интересным агрегатным состоянием вещества является фермионный конденсат. Как понятно из названия, он состоит из фермионов (частиц, составляющих все вещество, — электронов, протонов, нейтронов и т. д., а также соединенных особым образом пары атомов), охлажденных до низких температур. Вещество в этом состоянии обладает сверхпроводящими свойствами, сохраняющимися при повышении температуры.

Ряд самостоятельных агрегатных состояний вещества объединяется в так называемую вырожденную материю. Сюда относятся ферми-газ, нейтронное вещество (из него состоят нейтронные звезды, плотность такого вещества доходит до 100 миллиардов тонн в кубическом сантиметре!), кварк-глюонная плазма («облако», состоящее из свободных кварков и глюонов, такое состояние возможно только при столкновении некоторых элементарных частиц с очень высокой энергией) и еще несколько совсем уж необычных и непонятных даже для самих ученых состояний.
Все это — самые исследованные и вполне объяснимые, с точки зрения современной науки, агрегатные состояния вещества. Однако существует еще множество состояний, которые пока не изучены должным образом и официально не причислены к фазовым состояниям вещества. Только одни их названия рождают самые фантастические ассоциации: сильно и слабо симметричное вещество, сверхтвердое тело, странное вещество...

I . Тесты с выбором ответа
У вопросов есть ответы,
Не ищи нигде совета.
Все ответы прочитай,
Только нужный выбирай.
Молекулы воды, льда и водяного пара
А) отличаются друг от друга.
Б) не отличаются друг от друга.
Промежутки между молекулами минимальны в
А) жидкостях,
Б) газах,
В) твердых телах.
Твердое, жидкое и газообразное агрегатное состояние
А) могут иметь все вещества.
Б) имеет только вода.
В) имеют только некоторые вещества.

Загадки
Внимание! Сейчас загадки.
Ответ для них бывает краткий.
Найдя отгадку, не спешите,
Агрегатность укажите.
Где-то жидкость, где-то газ,
Расскажите мне сейчас.
Твердым тело может быть,
Постарайтесь не забыть.
Есть невидимка: в дом не просится, а прежде людей бежит.
Над рекой, над долиной повисла белая холстина.
С неба пришел, в землю ушел.
На всех садится, никого не боится.
Что в гору не выкатишь?
Рассыпался горох на семьдесят дорог, никто его не подберет: ни царь, ни царица, ни красная девица.

Отгадки: 1- воздух (газ); 2-туман (скопление водяных капелек в воздухе вблизи земли, то есть жидкость); 3- дождь (жидкость); 4-снег (твердое тело); 5- Вода (жидкость); 6- град (твердое тело).

Задачи с рисунками
Вот рисунок и вопрос,
Жду от вас ответа.
Должен кратким быть ответ,
Так же точным быть при этом.

На огне котел стоит,
А в котле вода кипит.
Жидкость стала убывать.
Что же стало прибывать?


В трубку дует стеклодув,
Ваза получается.
Здесь расплавленным стеклом
Форма заполняется.
Свойство жидкости назвать
Всем нам предлагается.

Кого можно так назвать?
«Оседлые».
Их можно так назвать.
Бегут на месте годы,
Не могут место поменять.
«Кочевники» то там, то тут,
На месте долго не живут.
«Бродяги» взад-вперед снуют,
Без отдыха везде бегут.
Сухой лед - это интересно
Холодильник без электричества! Что там внутри? Сухой лед! Почему он «сухой» и откуда берется?
Сухой лед - это замерзший углекислый газ, иначе диоксид углерода (CO2).
CO2, как и большинство веществ, может существовать в виде газа, жидкости и твердого тела - сухого льда.
При атмосферном давлении и комнатной температуре СО2 существует только в виде углекислого газа, который не имеет ни цвета, ни запаха и в полтора раза тяжелее воздуха.
В атмосфере Земли содержится около 0,03% углекислого газа, и он необходим для живых организмов и растений.
Знаете ли вы, что в природе CO2 содержится еще и в вулканических газах.
В Италии близь Неаполя есть, так называемая, «собачья пещера». Вход в пещеру – это самая высокая точка пещеры, дальше наклон вниз. Из-за вулканической деятельности в пещере усиленно выделяется и скапливается углекислый газ. Его концентрация в нижних слоях воздуха в пещере составляет около 70%. Для всего живого такое количество углекислого газа в воздухе смертельно, в том числе и для забегающих туда собак. Надо ли говорить, почему этой пещере дали такое имя.

Знаете ли вы, что человек при вдыхании воздуха даже с 8% содержанием СО2 в течение 30 минут задыхается. А в воздухе, выдыхаемом человеком, углекислого газа 4%.
Где же углекислый газ доставляет нам истинное наслаждение?
Конечно, в газированной воде!
Ее научились делать в конце 19 века после того, как был найден способ получения углекислого газа. СО2 хорошо растворяется в жидкостях, причем в спирте куда лучше, чем в воде, и чем ниже температура жидкости, тем лучше растворимость. Именно способность хорошо растворяться в воде позволило использовать СО2 в производстве газированных напитков. При растворении в воде СО2 образует угольную кислоту, которая улучшает вкусовые качества газированных напитков и не дает размножаться бактериям.

В магазинную газированную воду CO2 закачивается под давлением. Например, при давлении в 5 атм газирование воды происходит лучше, чем при нормальном давлении. Поэтому-то и шипит газированная вода, когда вы открываете купленную бутылку. Газ выделяется до тех пор, пока жидкость не придет в равновесие с воздухом. «Убрать» газ из газированной воды совсем легко, если поместить ее под колокол вакуумного насоса и создать там низкое давление.
Под действием давления при температурах от –56 до 31о С углекислый газ легко сжижается и получается жидкая углекислота.
В 1940 году научились производить жидкий СО2.

Поскольку критическая температура для СО2 выше комнатной (31 ° C), жидкий СО2 можно хранить под давлением в специальных герметических баллонах (критическая температура – это температура, выше которой CO2 при сколь угодно большом давлением невозможно перевести в жидкое состояние).
Внутри СО2-баллонов при комнатной температуре создают высокое давление (65-70 атм), равное давлению насыщенного пара, при котором жидкость и газ находятся в равновесии. В результате газ больше не образуется, и баллоны не взрываются.
Углекислота в баллонах применяется, например, в огнетушителях, для производства газированной воды, в пневматическом оружии, для накачивания шин и камер велосипедных колес.
Наконец-то дошли до сухого льда!

Если жидкую углекислоту из баллона, где она находится под большим давлением, вылить наружу, то она начинает стремительно испаряться. При испарении температура жидкости понижается, и не успевшая испариться вылившаяся углекислота замерзнет. В результате получится рыхлый углекислый "снег"– замерзший углекислый газ.
Именно так впервые в 1834г. обнаружил сухой лед французский химик Чарльз Thilorier.
Как делают в промышленности сухой лед ?
Промышленный способ получения сухого льда был разработан в 1923 году.
Принцип таков: очищенный углекислый газ сжижают, охлаждая его при высоком давлении, и хранят в больших емкостях. Для получения сухого льда жидкий СО2 подают в закрытую камеру гидравлического пресса, где понижают давление до атмосферного. При резком снижении давления из СО2 образуются рыхлый снег и очень холодный газ. Затем снег прессуют под давлением 30-50 атм и получают сухой лед, а газ откачивают, сжижают и возвращают в резервуар для хранения.
Современные установки выпускают сухой лед в виде крошки, гранул и брикетов

Сухой лед при нормальном атмосферном давлении имеет температуру минус 78° C и обладает странным свойством – испаряться без перехода в жидкое состояние. Этот процесс называется «возгонка» или «сублимация». Испаряющийся при этом газ имеет очень низкую температуру и конденсирует в воздухе водяные пары, поэтому присутствие углекислого газа в воздухе можно определить косвенно по наличию тумана (или, как распространено говорить, дыма).

Знаете ли вы, что ученым при помощи космических аппаратов удалось зафиксировать на Марсе плотные облака, состоящие из сухого льда – отвердевшего диоксида углерода.
Кроме того, в полярных областях Марса обнаружены дюны, покрытые твердым углекислым газом - сухим льдом.
Знаете ли вы, что в современном мире сухой лед нашел применение и в очень необычных, интересных устройствах – это дым-машины или иначе генераторы тумана.
Придумали, например, машину для Хэллоуина, которая создает мыльные шары, наполненные туманом, или, например, дым-машины для представлений и концертов.
Знаете ли вы, что бросив в пламя несколько кусочков сухого льда, можно быстро потушить горящий бензин.
Знаете ли вы, что сухой лед привлекает комаров. Если насыпать немного сухого льда, то комары полетят на испаряющийся углекислый газ и, скорее всего, забудут про вас. Наверно, это у них в генах, ведь углекислый газ является продуктом дыхания всех теплокровных.

Если зажечь свечу в стакане, а затем положить туда кусок сухого льда, так что свеча быстро гаснет.
Это объясняется тем, что при контакте с теплым стаканом сухой лед быстрее испаряется и заполняет большую часть стакана тяжелым углекислым газом.

Еще более впечатляющей выглядит ситуация, когда тяжелый углекислый газ «наливают» в стакан с горящей свечой. Углекислый газ так тяжел, что, несмотря на поднимающийся теплый воздух от горящей свечи, опускается вниз на дно.

Как же попроще получить сухой лед?
Удобнее всего вылить жидкую углекислоту из огнетушителя в матерчатый мешок. Здесь она будет свободно испаряться, мешок окутывается туманом, а внутри образуется « углекислый снег».
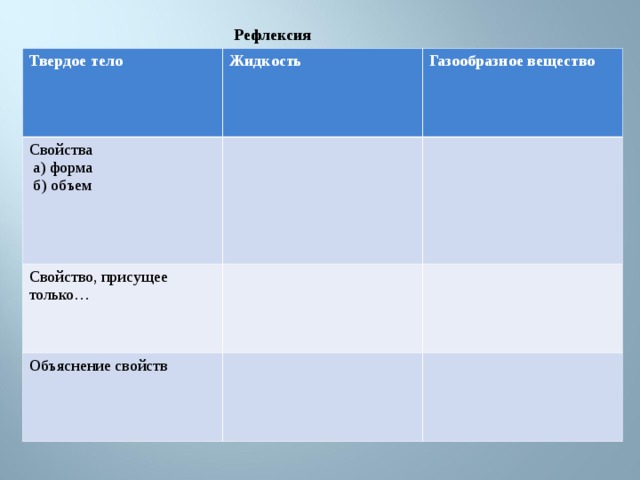
Рефлексия
Твердое тело
Жидкость
Свойства
а) форма
б) объем
Газообразное вещество
Свойство, присущее только…
Объяснение свойств

 Получите свидетельство
Получите свидетельство Вход
Вход










 Урок "Три состояния вещества" (2.71 MB)
Урок "Три состояния вещества" (2.71 MB)
 0
0 1474
1474 39
39 Нравится
0
Нравится
0


