08.11.2016
Преподаватель: Батрякова А.А.
Тема урока: Основные физические и химические свойства неметаллов. Нахождение в природе.
Цель урока: обобщить сведения об особенностях строения атомов неметаллов; научить определять степени окисления; закрепить знание особенностей строения, физических и химических свойств простых веществ — неметаллов; закрепить умение составлять уравнения химических реакций, характеризующих свойства неметаллов.
Задачи:
Образовательные: обобщить и систематизировать знания о физических и химических свойствах неметаллов
Воспитательные: продолжить формирование научного мировоззрения
Развивающие: способствовать развитию логического мышления (умения сравнивать, обобщать, делать выводы)
Тип урока: урок усвоения новых знаний.
Метод проведения: словесные (рассказ, объяснение, беседа); проблемно-поисковый.
Ход урока:
Организационный этап.
Актуализация знаний.
Изучение нового материала.
Закрепление.
Заключение.
Организационный этап.
Приветствие. Проверка готовности к уроку.
Актуализация знаний.
Вспомним ранее пройденные понятия.
«Мозговой штурм»
Какие элементы называют металлами? Дайте определение.
(Металлы – это химические элементы, атомы которых отдают электроны внешнего, а некоторые – и предвнешнего электронного слоя, превращаясь в положительные ионы).
Укажите положение металлов в ПСХЭ.
(Левый нижний угол от диагонали бор – астат).
Что происходит со свойствами металлов в главных подгруппах? В периодах? (Металлические свойства в главных подгруппах сверху вниз усиливаются, в периоде слева направо – ослабевают)
Чем являются металлы в соединениях? (Восстановители).
Какой вид химической связи и тип кристаллической решетки характерен для металлов?
(Металлическая).
Какие физические свойства характерны для металлов?
(Металлический блеск, пластичность, высокая теплопроводность, электропроводимость, твердость, прочность, магнитные свойства).
Изучение нового материала.
1. Положение неметаллов в ПС
Неметаллы расположены в основном в правом верхнем углу ПС, условно ограниченном диагональю бор-астат. р-элементы. Самым активным является фтор. В простых в-вах – ковал. непол. связь.
2. Особенности строения атомов неметаллов.
Во внешнем электронном слое атомов неметаллов находится от трёх до восьми электронов.

Для атомов неметаллов, по сравнению с атомами металлов характерны:
меньший атомный радиус;
четыре и более электрона на внешнем энергетическом уровне.
Отсюда и такое важнейшее свойство атомов неметаллов – тенденция к приёму недостающих до 8 электронов, т.е. окислительные свойства. Качественной характеристикой атомов неметаллов, т.е. своеобразной мерой их неметалличности, может служить электроотрицательность, т.е. свойство атомов химических элементов поляризовать химическую связь, оттягивать к себе общие электронные пары. Электроотрицательность – мера неметалличности, т.е. чем более электроотрицателен данный химический элемент, тем ярче выражены неметаллические свойства.
3. Кристаллическое строение неметаллов-простых веществ. Аллотропия.
Если металлы – простые вещества образованы за счет металлической связи, то для неметаллов – простых веществ характерна ковалентная неполярная химическая связь. В отличие от металлов неметаллы – простые вещества, характеризуются большим многообразием свойств. Неметаллы имеют различное агрегатное состояние при обычных условиях:
газы – H2, O2, O3, N2, F2, Cl2;
жидкость – Br2;
твердые вещества – модификации серы, фосфора, кремния, углерода и др.
Гораздо богаче у неметаллов и спектр цветов: красный – у фосфора, красно-бурый – у брома, желтый – у серы, желто-зеленый – у хлора, фиолетовый – у паров йода. Элементы – неметаллы более способны, по сравнению с металлами, к аллотропии.
Способность атомов одного химического элемента образовывать несколько простых веществ называется аллотропией, а эти простые вещества – аллотропными видоизменениями или модификациями.
4. Физические свойства неметаллов.
Ковкость отсутствует
Блеска нет
Теплопроводность (только графит)
Цвет разнообразный: желтый, желтовато-зеленый, красно-бурый.
Электропроводность (только графит и черный Фосфор.)
Агрегатное состояние:
газообразное(H2, O2, Cl2 ,F2, O3)
твердое (Р, С)
жидкое (Br2)
5. Химические свойства неметаллов.
Неметаллы в химических реакциях могут быть восстановителями и окислителями (фтор, кислород.) Уравнения записать на доске (обучающиеся).
7. Водородные соединения неметаллов.
В отличие от металлов неметаллы образуют газообразные водородные соединения. Их состав зависит от степени окисления неметаллов.
| -4 | -3 | -2 | -1 |
| RH4 → | RH3 → | H2R → | HR |
Летучие водородные соединения неметаллов можно разделить на три группы:
1) Хорошо растворимые в воде (HCl, HBr, HJ, H2S, H2Se, NH3), которые диссоциируют на ионы, проявляя кислотные и основные свойства.
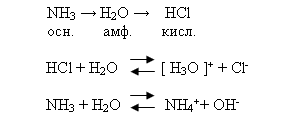
2) Соединения, разлагаемые водой:
BH3 + 3H2O = H3BO3 + 3H2↑
3) Летучие водородные соединения
CH4, PH3, которые не взаимодействуют с водой.
По периоду в ПС химических элементов с увеличением порядкового номера элемента – неметалла усиливается кислотный характер водородного соединения.
SiH4 → PH3 → H2S → HCl
Выводы:
Элементы-неметаллы расположены в главных подгруппах III–VIII групп ПС Д.И. Менделеева, занимая её верхний правый угол.
На внешнем электронном слое атомов элементов-неметаллов находятся от 3 до 8 электронов.
Неметаллические свойства элементов усиливаются в периодах и ослабевают в подгруппах с увеличением порядкового номера элемента.
Высшие кислородные соединения неметаллов имеют кислотный характер (кислотные оксиды и гидроксиды).
Атомы элементов-неметаллов способны как принимать электроны, проявляя окислительные функции, так и отдавать их, проявляя восстановительные функции.
Закрепление.
1) Вставьте слова, пропущенные в тексте.
Атомы ____ в отличие от атомов ____ легко принимают наружные электроны, являются ____
2) Вставьте слова , пропущенные в тексте.
Неметаллические свойства элементов с увеличением порядкового номера в периодах ____
В группах неметаллические свойства элементов ____
3) Пользуясь периодической таблицей, запишите молекулярные формулы высших кислородных соединений неметаллов III периода.
4) Запишите формулы водородных соединений элементов VII А группы. Как изменяются кислотные свойства с увеличением порядкового номера элемента?
5) Какую высшую степень окисления имеют следующие элементы?
| Азот | +6 |
| Хлор | +5 |
| Сера | +4 |
| Кремний | +7 |
6) Определите, окислителем или восстановителем является сера в следующих реакциях:
H2+S=H2S
S —
2SO2 + O2 → 2SO3
S —
7) Наиболее ярко выраженные неметаллические свойства проявляет вещество, образованное из атомов, в которых число электронов во внешнем электронном слое равно____.
• 4 • 5 • 6 • 7
8) Наиболее электроотрицательными являются атомы…..
• серы • фосфора • кремния • хлора
9) Типичному неметаллу соответствует следующая схема распределения электронов по электронным слоям:
2, 1
2, 8, 2
2, 8, 7
Поменяйтесь тестом с соседом и проверьте тест вместе со мной.
Заключение.
Обсуждение урока, выставление оценок, рефлексия.
Домашнее задание: Тема 4.5, стр. 134 №3

 Получите свидетельство
Получите свидетельство Вход
Вход












 Урок по химии на тему "Основные физические и химические свойства неметаллов. Нахождение в природе." (29.44 KB)
Урок по химии на тему "Основные физические и химические свойства неметаллов. Нахождение в природе." (29.44 KB)
 0
0 1842
1842 139
139 Нравится
0
Нравится
0


