Конспект урока по химии в 9 классе
«Великий углерод»
подготовила
учитель химии
МБОУ СОШ№1с.Гизель
Пригородного района
РСО-Алания
Солтанова Виктория Казбековна

Тема урока: "Великий углерод"
Цель урока: обобщить знания об углероде и его соединениях, о круговороте углерода, показать взаимосвязь веществ.
Задачи урока:
Образовательные:
Выявление и оценка степени овладения учащимися системой знаний об элементах и их соединениях на примере углерода, а также комплексом навыков и умений для успешного применения полученных знаний на практике, совершенствовать практические умения и навыки работы с лабораторным оборудованием и химическими реактивами.
Развивающие:
Развивать у учащихся умения сравнивать, наблюдать, обобщать, делать выводы;
Используя дополнительный материал, способствовать возрастанию познавательной активности учащихся.
Развивать внимание, логическое мышление, культуру речи учащихся, общую эрудицию.
Воспитательные:
Воспитывать бережное отношение к окружающей среде, любовь к родному краю, формирование научной системы взглядов на мир.
Тип урока: урок обобщения.
Методы урока: словесные, словесно-наглядные, интерактивные, практические, проектная деятельность.
Оборудование: периодическая система химических элементов Д.И. Менделеева, мультимедийная презентация, компьютер. проектор, интерактивная доска, модели кристаллических решеток алмаза и графита, мел, мрамор, ракушки, древесный уголь, активированный уголь, коллекция углеродсодержащих минералов, минеральная вода, жемчуг, простой карандаш, яйцо.
Ход урока 1.Организационный момент.
2.Эммоциональный настрой.
Учитель:
Добрый день!
Первым делом гоним лень,
На уроке не молчать,
Всем работать, отвечать!
В мире много интересного,
Нам порою неизвестного.
Миру знаний нет предела.
Так скорей друзья за дело!
3. Обобщение и систематизация знаний.
Учитель: Обратите внимание на предметы, которые лежат на демонстрационном столе. Как вы думаете, что объединяет эти предметы и как они связаны с темой нашего сегодняшнего урока?
(Во всех этих веществах содержится элемент углерод).
Учитель:
И какова же тема нашего сегодняшнего урока?
Учащиеся предлагают тему урока. "Углерод и его соединения".
Учитель: Правильно, но я хочу назвать наш урок "Великий углерод!" (Слайд1)
Эпиграфом нашего урока будут следующие слова: «Все в природе взаимосвязано, и ничто не исчезает бесследно и не возникает ниоткуда». (Слайд2)
Цель нашего урока- обобщить знания об углероде и его соединениях.
Перед каждым из вас "Паспорт углерода", который нужно заполнить. На это задание я вам даю несколько минут. Пожалуйста, приступайте к его выполнению. (Слайд3)
(Один учащийся работает на интерактивной доске).
Паспорт углерода (Слайд4).
Имя: Углерод- русское название
Carboneum- латинское название.
Пол: мужской
Дата рождения- Элемент в свободном виде и его соединения известны с древнейших времен.
Место проживания: 2 период, IV А группа.
Некоторые дополнительные данные:
порядковый номер-6

 относительная атомная масса-12
относительная атомная масса-12
заряд ядра- +6
+6
666
Фото (схема строения атома): 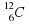
2 4
Электронная конфигурация: 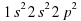
Сфера деятельности: восстановитель, окислитель.
Ближайшие родственники:
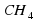 - метан
- метан
CO- оксид углерода(II)
СО2- оксид углерода (IV)
Н2СО3 - угольная кислота и ее соли.
Учитель: Отлично! Мы видим, что у нашего героя много родственников. Познакомимся с природными соединениями углерода. Рассмотрите коллекции, которые у вас лежат на столах. Сейчас мы с вами узнаем, какие из этих образцов можно встретить на территории республики РСО-Алания. (Ученический проект "Природные соединения углерода, встречающиеся на территории республики РСО-Алания.)
Учитель: Давайте вспомним, что такое аллотропия?
(Аллотро́пия — существование двух и более простых веществ одного и того же химического элемента, различных по строению и свойствам — так называемых аллотропных модификаций или форм.)
Учитель: А какие аллотропные видоизменения углерода вы знаете?
(Алмаз, графит, графен, фуллерен, карбин). (Ученический проект "Аллотропия углерода").
Учитель: Я надеюсь, что вы много интересного узнали из этого проекта.
Теперь мы с вами перейдем к кислородсодержащим соединениям углерода. На ваших столах лежит карточка "Программированный опрос "Оксиды углерода"". Ознакомьтесь с ее содержанием и напротив номера задания-утверждения напишите формулу оксида углерода, к которому относится это утверждение. (Пока учащиеся выполняют задание, звучит тихая музыка).
Программированный опрос "Оксиды углерода".
1.Молекула этого оксида состоит из одного атома углерода и одного атома кислорода.
2. Связь между атомами в молекуле- ковалентная полярная.
3. Газ, практически нерастворимый в воде.
4. В молекуле этого оксида один атом углерода и два атома кислорода.
5. Запаха и цвета не имеет.
6. Газ, растворимый в воде.
7.Не ядовит.
8. Несолеобразующий.
9. Горюч.
10. Яд.
11. Образуется при дыхании живых существ.
12. Образуется при неполном сгорании топлива.
13. Используется при газировании воды и напитков.
(Ответы на задания программированного опроса: СО- 1, 2, 3,5, 8, 9, 10,12;
СО2- 2, 6,7,11,13). (Слайд5)
Учитель: Я хочу обратить ваше внимание на то, что CO- оксид углерода(II)
СО2- оксид углерода (IV)- это газообразные вещества, и с ними нужно обращаться осторожно. Сейчас мы с вами узнаем, какую опасность эти оксиды таят в себе. (Ученический проект " Оксиды углерода").
Учитель: В последнее в республике участились случаи отравления газом. В 2013 году в республике от угарного газа погиб 21 человек. С начала нового 2014 года от отравления угарным газом в Северной Осетии погибло восемь человек. Я надеюсь, что эта информация очень важна для каждого из присутствующих в этом классе.
Учитель :Следующий ближайший родственник углерода- это угольная кислота.
Ребята, как вы думаете, если выпить Н2СО3, то повлияет ли она на организм человека и если да, то как?
( Ребята приходят к выводу, что раствор H2CO3 входит в состав различных напитков.)
(Учитель открывает бутылочку с минеральной водой.)
Учитель: Что вы наблюдаете? Какой процесс происходит?
(Учащиеся составляют уравнение реакции).
Учитель: А что вы знаете о природных минеральных водах, которыми богата наша республика?
Учитель: Несмотря на то, что угольная кислота является слабой, она все-таки образует соли. Вспомните, какие соли образует угольная кислота и как они называются?
( Средние, кислые; карбонаты , гидрокарбонаты).
Учитель: А теперь проведем небольшой эксперимент. В трех пробирках находятся растворы сульфата натрия, хлорида натрия и карбоната натрия.
Определите, в какой пробирке находится карбонат натрия.(Учащиеся выполняют эксперимент). (Слайд6)
Учитель: Что вы наблюдаете и как называется эта реакция? Составьте уравнение реакции.
(Наблюдается выделение оксид углерода (IV). Это качественная реакция на карбонат-ион).
Учитель: Посмотрите на доску. Что видите?
(Слайд с изображением сталактитов и сталагмитов). (Слайд7)
Что за образования свисают со сводов пещеры?
Что за наросты на полу?
Прокомментируйте протекающие процессы, напишите уравнения реакций.
(Сталактиты и сталагмиты в подземных пещерах образованы известняком, выделяющимся из просачивающегося через трещины в сводах пещер раствора гидрокарбоната кальция. Гидрокарбонат кальция образуется при взаимодействии известняка с водой и углекислым газом по обратной реакции.
СаСО3+ H2О + СО2 → Ca(HCO3)2
Ca(HCO3)2 → СаСО3+ H2О + СО2)
Учитель: Углерод обладает таким полезным свойством, как адсорбция. Что такое адсорбция и где применяют это явление?
(Адсорбция - поглощени газов или растворенных веществ на поверхности твердого тела или жидкости. Очистка от примесей (в производстве сахара и др.), для защиты органов дыхания (противогазы), в медицине (таблетки «Карболен»)
Учитель: Атомы углерода могут соединяться разнообразными способами между собой и с атомами многих других элементов, образуя огромное разнообразие веществ. Их химические связи могут возникать и разрушаться под действием природных факторов. Так возникает круговорот углерода в природе: из атмосферы – в растения, из растений – в животные организмы, из них – в неживую природу и т.д. (Слайд8). Где углерод, там многообразие веществ, где углерод, там самые разнообразные по молекулярной архитектуре конструкции. Неоценимо значение соединений углерода в жизни человека – повсюду нас окружает связанный углерод: в атмосфере и литосфере, в растениях и животных, в нашей одежде и пище. Соединения углерода играют большую роль и в существовании самого человеческого организма.
Он повсюду на Земле –
В нефти, в газе и в угле.
А ещё без Углерода
Не живет совсем природа.
Все живые существа
Состоят из вещества,
В нем приятель Углерод
Обязательно живёт.
И внутри меня и мамы
Углерода килограммы!
Поэтому изучение этого химического элемента так важно! Для того чтобы знать свойства этих веществ что надо знать?
Учитель: Итак, соединения углерода очень распространены. Кроме ископаемого угля, в недрах Земли находятся большие скопления нефти, представляющей сложную смесь различных углеродсодержащих соединений, преимущественно углеводородов. В земной коре встречаются в огромных количествах соли угольной кислоты, особенно карбонат кальция. В воздухе всегда имеется углекислый газ. Растительные и животные организмы состоят из веществ, в образовании которых главное участие принимает углерод. Таким образом углерод – царь живой природы.
4. Рефлексия. (Слайд9).
Учитель: Предлагаю вам составить синквейн. Синквейн происходит от французского “пять”. Это нерифмованное стихотворение из пяти строк, которые строятся по правилам. Правила составления синквейна:
Первая строка — тема синквейна, заключает в себе одно слово (обычно существительное или местоимение), которое обозначает объект или предмет, о котором пойдет речь.
Вторая строка — два слова (чаще всего прилагательные или причастия), они дают описание признаков и свойств выбранного в синквейне предмета или объекта.
Третья строка — образована тремя глаголами или деепричастиями, описывающими характерные действия объекта.
Четвертая строка — фраза из четырёх слов, выражающая личное отношение автора синквейна к описываемому предмету или объекту.
Пятая строка — одно слово-резюме, характеризующее суть предмета или объекта.
Углерод;
жизнеутверждающий, адсорбирующий;
украшает, строит, рисует;
образует аллотропные видоизменения;
великий.
Учитель: В качестве домашнего задания я вам предлагаю осуществить цепочку превращений . (Слай10).
C → CH4 → CO2 → Na2CO3 →NaHCO3 → CO2 → CaCO3 →CO2
Учитель: За активную и плодотворную работу вам в награждение этот салют. (Опыт "Звездный дождь" В фарфоровой чашечке тщательно смешайте шпателем равные количества (по 5-7 г) порошков железа, древесного угля и перманганата калия. Полученную смесь перенести в железный или фарфоровый тигель, закрепленный в фарфоровом треугольнике, который находится на кольце штатива. Нагрейте тигель в пламени газовой горелки. Через 3-5 минут из тигля начнут разлетаться раскаленные частицы железа в виде снопа искр.)
Учитель: От трудов и от забот
Отдыхает Углерод.
Не тревожьте сладкий сон.
Почивать изволит он.
Не шумите у ворот:
Спит Великий Углерод».
Учитель: Благодарю вас за урок и те знания, которые вы сегодня показали. (Выставление оценок). Надеюсь, что теперь вы знаете, как тесно химия связана с жизнью человека и сможете по достоинству оценить эту науку по достоинству. Урок окончен. До свидания! (Слайд11).
Источники информации:
1. Химия. Первое сентября №6, 2011г., стр.30-34.
2. Химия. Первое сентября №1, 2008г., стр.45.
3. Химия. Первое сентября №11, 2009г., стр.36.
4.http://www.pandia.ru/text/78/187/47786.php
5. http://fs.nashaucheba.ru/docs/270/index-1242177.html
6. http://worldteacher.ru/1723-458.html
7. http://festival.1september.ru/articles/608942/
8. http://www.edu.cap.ru/Home/9301/uroki/uglerodiegosoedineniya.doc
9. http://yauchitel.ru/load/khimija/uroki_konspekty/konspekt_i_prezentacija_k_uroku_po_teme_quot_ugle rod_quot_dlja_9_klassa/122-1-0-563
10. http://konserva.com/page-ramki…
![]()
![]() - метан
- метан
 Получите свидетельство
Получите свидетельство Вход
Вход




 относительная атомная масса-12
относительная атомная масса-12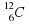
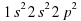
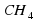 - метан
- метан








 Урок химии "Великий углерод" (45.04 КB)
Урок химии "Великий углерод" (45.04 КB)
 0
0 895
895 77
77 Нравится
0
Нравится
0


