План-конспект открытого урока по химии в 11 классе.
Тема: «Дисперсные системы». Урок новых знаний.
Цель:
Образовательная:
Сформулировать понятие дисперсной системы;
Познакомить с классификацией дисперсной системы;
Привлечь внимание учащихся к дисперсным системам большой практической значимости: суспензиям, эмульсиям, коллоидным растворам, истинным растворам, аэрозолям, пенам;
Продолжить формирование общеучебных умений (осуществлять самоконтроль, сотрудничать).
Развивающая:
Развивать умение использовать химическую терминологию;
Развивать мыслительные операции (анализ, синтез, установление причинно-следственных связей, выдвижение гипотезы, классификация, проведение аналогий, обобщение, умение доказывать, выделение главного);
Развивать интересы, способности личности;
Развивать умение проводить, наблюдать и описывать химический эксперимент;
Совершенствовать коммуникативные умения учащихся в совместной деятельности (умение вести диалог, выслушивать оппонента, аргументировано обосновывать свою точку зрения) и информационно – познавательную компетентность учащихся.
Воспитательная:
Продолжить развитие познавательных интересов учащихся;
Воспитывать культуру речи, трудолюбие, усидчивость;
Продолжить формирование ответственного, творческого отношения к труду.
Используемые технологии: ЭОР.
І. Организационный момент.
ІІ. Изучение нового материала. (Звучит песня Н. Добрынина «Синий туман», на демонстрационном столе коллекция дисперсных систем, используемых человеком в повседневной жизни)
- Как вы думаете, ребята, имеет ли прозвучавшая песня какое-нибудь отношение к теме сегодняшнего урока? Перед вами на столе находится коллекция дисперсных систем, мне бы хотелось чтобы вы попытались классифицировать эти системы на группы (ребята пытаются выполнить задание).
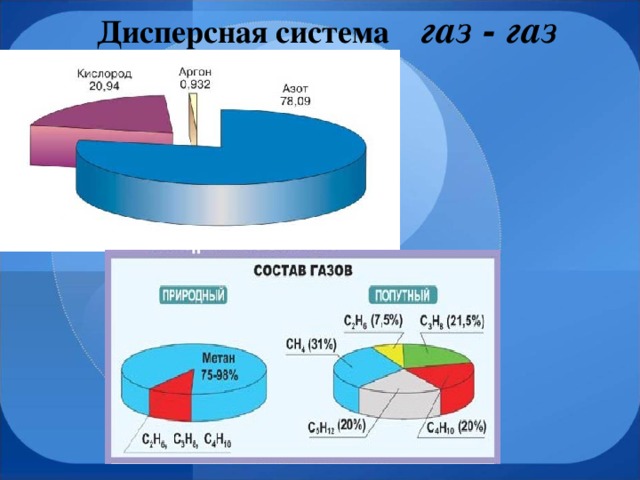
Мы живем в мире дисперсных систем. Посмотрите внимательно вокруг себя. Туман, пыль, снег – все это не только случайные неприятности, но и примеры дисперсных систем.
Большинство веществ окружающего нас мира, составляющих ткани живых организмов, гидросферу, земную кору и недра, космическое пространство часто представляют собой вещества в раздробленном, или, как говорят, дисперсном состоянии. Диспергирование означает раздробление.
- Как вы думаете какова цель сегодняшнего урока? (ответы детей)
Итак, цель нашего сегодняшнего урока – составить представление о дисперсных системах, их месте в природе и жизни человека, научиться характеризовать их свойства, объяснять причины большей или меньшей устойчивости.
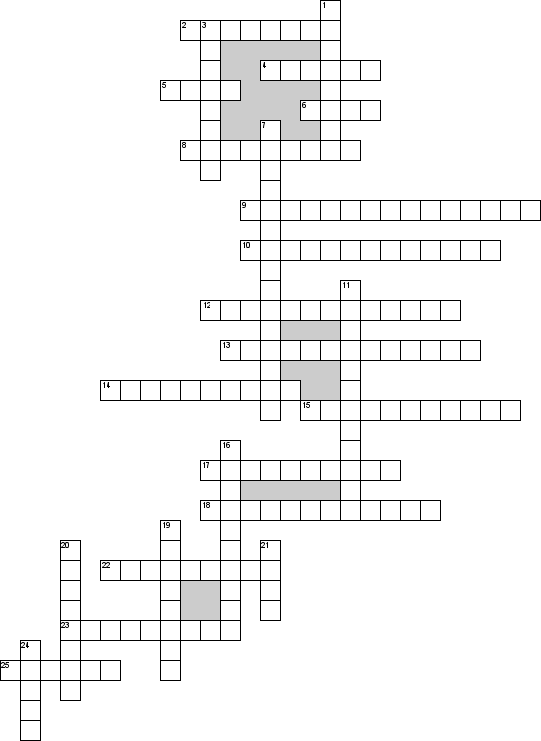
- Но, что же все таки такое, дисперсная система? (интерактивная схема – приложение 1).
Дисперсная система – это смесь, состоящая как минимум из двух веществ, которые совершенно или практически не смешиваются друг с другом и не реагируют друг с другом химически.
(
 На доске) Дисперсная система
На доске) Дисперсная система
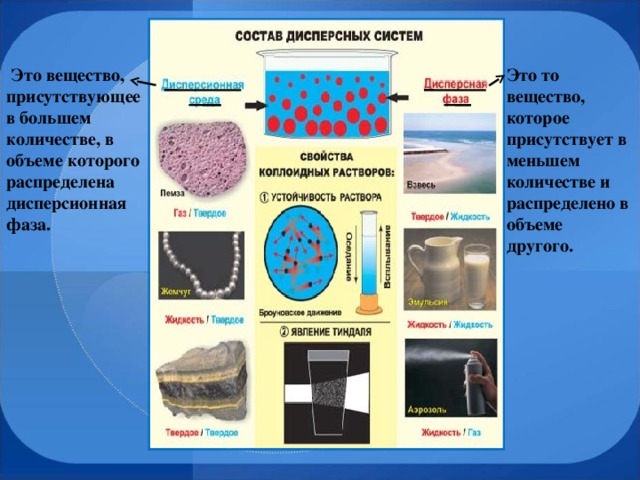
Дисперсионная среда Дисперсная фаза
В дисперсионной среде распределены частицы дисперсной фазы, которые могут быть твердыми, капельками жидкости или пузырьками газа. Дисперсная фаза мелко распределена в дисперсионной среде. (запись в тетради) . Наибольшее значение в практике имеют ДС, в которых средой является вода или другие жидкости, о них мы и поговорим подробнее.
Посмотрите на табл.2 стр.97. Составьте схему, отражающую виды ДС, на основе таблицы укажите размер частиц в каждой ДС.
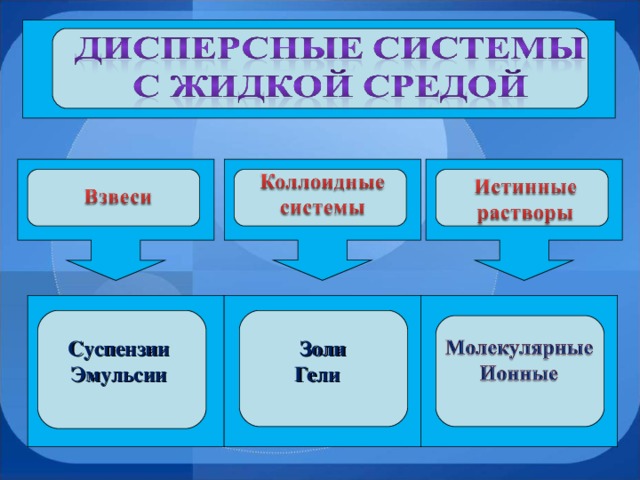
Истинные растворы, в которых в-во раздроблено до мельчайших частиц (молекул или ионов) размерами менее 1нм, вы изучали ранее, поэтому сегодня сосредоточим внимание на других ДС.
Тонкодисперсные системы с размерами частиц 1 – 100 нм также называют коллоидными системами (растворами) или золями (интерактивная схема). В зависимости от природы дисперсионной среды, коллоидные системы подразделяют на золи и гели (интерактивная схема).
- Коллоидные системы (коллоиды, др. греч.) – дисперсные системы, промежуточные между истинными растворами и грубодисперсными системами – взвесями и эмульсиями. Коллоидные частицы не видны в обычный микроскоп, они крупнее молекул, но простым глазом их увидеть все же нельзя, т.е. по виду растворы не различимы. Но такая необходимость возникает в практической деятельности. Как же отличить коллоидный раствор от истинного?
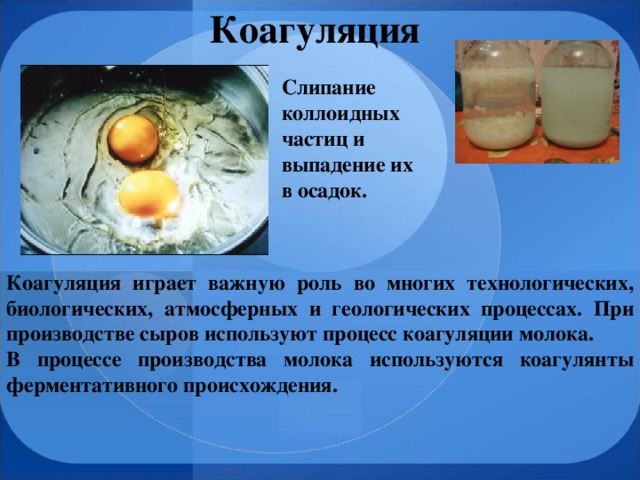
Путем долгих исследований в 1869 г. Тиндаль наблюдал образование светящегося конуса при пропускании пучка света через коллоидный раствор. Он объяснял это тем, что более крупные, чем в истинном растворе, частицы дисперсной фазы золя отражают свет от своей поверхности, и в сосуде с коллоидным раствором был виден светящийся конус, а в истинном растворе этого не наблюдалось. Позднее это явление получило название Эффекта Тиндаля (интерактивная схема). Для золей характерно явление коагуляции – слипание коллоидных частиц и выпадения их в осадок. Этот процесс наблюдается вследствие объединения более крупные агрегаты. (интерактивная схема)
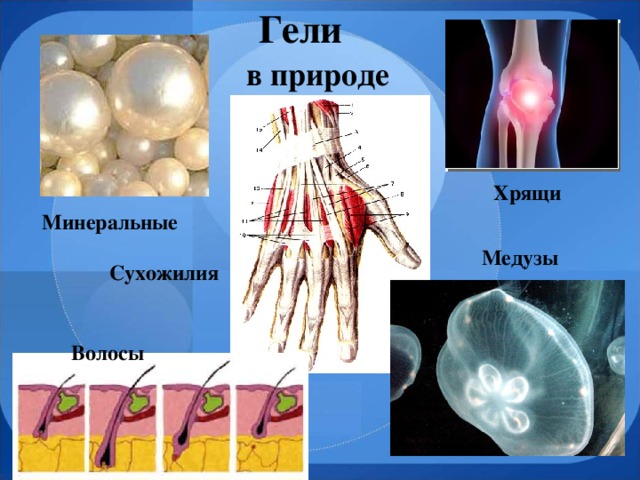
- Некоторые золи при осаждении увлекают за собой жидкую фазу (иногда даже полностью), образуя при этом с водой общую массу. Подобные осадки называются гелями или студнями. Чтобы было легче представить себе, что такое гель, приведем примеры бытовых гелей – желе, мармелад, яичный белок, студень (интерактивная схема)
Гелями могут быть дисперсные системы с жидкой и газообразной дисперсионной средой. Гели обладают одновременно свойствами жидкости и твердого тела. КА жидкости, гели текучи и пластичны, хотя они могут сохранять форму, как тв. тела, и могут быть сравнительно прочны и упруги. Эти свойства гелей обусловлены существованием в них пространственной сетки, образованной частицами дисперсной фазы, связанными между собой силами различной природы. Состояние жидкости в гелях непрочное. Они сравнительно легко изменяют свой объем при поглощении или отдачи дисперсионной среды. С течением времени из геля выделяется жидкая фаза и объем геля уменьшается. Это явление называется синерезисом, или старением геля (запись в тетради, интерактивная схема).
- А вот если у человека этот процесс затруднен (переход фибриногена в фибрин), на какое заболевание он может указывать? (гемофилия). Из курса биологии вам известно, что носителем гена гемофилии является….(женщина, а заболевают мужчины) . А, вы, знаете каких-нибудь выдающихся личностей у которых встречалось это заболевание? (Династия Романовых, которая царствовала более 300 лет, страдала этим заболеванием).
Рубиновые стекла, аморфные минералы, образовавшиеся в водных растворах и содержащие переменное количество воды, относятся к тв. гелям. Драгоценный камень агат – типичный минеральный гель, встречающийся в отложениях теплых источников, образуется также в процессе синерезиса.
- Мы достаточно подробно рассмотрели коллоидные растворы, теперь давайте поговорим о грубодисперсных системах. Посмотрите внимательно на схему в вашей тетради и скажите какие ДС относят к грубодисперсным? Используя материал учебника на стр.97-100, охарактеризуйте эти системы.
- А сейчас давайте маленько отдохнем и отгадаем небольшие загадки касающиеся ДС.
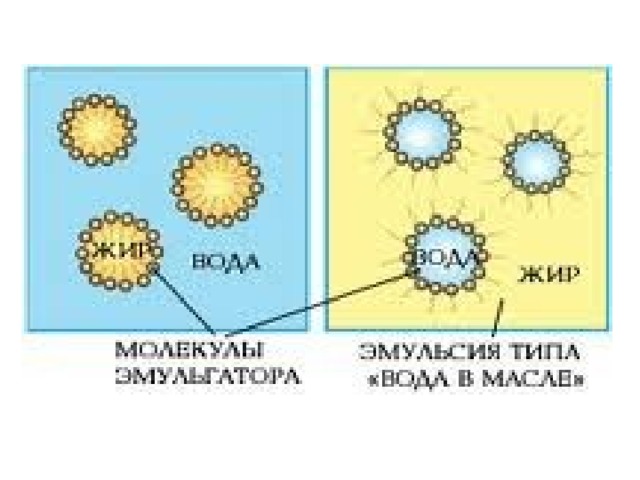
1. Превратите крупную австралийскую птицу – страуса, в жидкость со взвешенными в ней частицами другой жидкости. (Эму - эмульсия)э
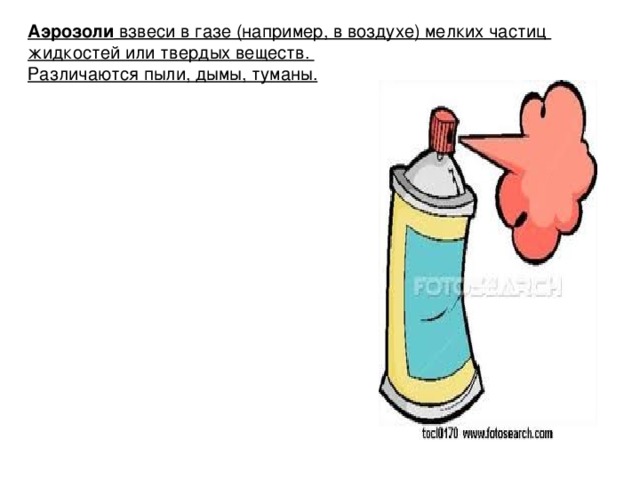
2. Как превратить атолл Роз в газ со взвешенными в нем мельчайшими частицами. (Роз – аэрозоль).
3. Название, какого раствора начинается с самой низшей школьной оценки? (Кол - коллоидный).
4. Из названий степного грызуна и города – областного центра черноземной зоны Росси составьте название жидкости со взвешенными в ней тв. частицами. (Суслик, Пенза - суспензия).
- Давайте выполним небольшой лабораторный опыт. У вас на столах находятся карточки- путеводители (приложение 2), которыми вы должны пользоваться при выполнении опыта. Не забываем о ТБ. После окончания работы сделайте вывод.
- Чем же обусловлено многообразие дисперсных систем? (Многообразие ДС обусловлено тем, что образующие их среды могут находиться в любом из трех агрегатных состояний).
Познакомившись с многообразием ДС, вспомним явления, которые происходят с ними, т.к они нередко встречаются в окружающей нас действительности и их необходимо учитывать при использовании. (синерезис, коагуляция, расслаивание эмульсий и суспензий, эффект Тиндаля).
- У ДС есть еще одно важной свойство – в-во в дисперсном состоянии стремиться поглотить другие в-ва. Подумайте и назовите пример всем известного в-ва из домашней или нашей школьной аптечки, которое в мелко дисперсном состоянии используется при отравлениях (активированный уголь)
ІІІ. Итог урока.
- А теперь давайте вернемся к нашей коллекции ДС, в начале нашего урока вы классифицировали все в-ва на группы еще незная правильную классификацию. Итак, есть ли какие-нибудь Системы, которые находятся не на своих местах . Давайте расставим все на свои места. *(дети исправляют ошибки, допущенные в начале урока при расстановки ДС, в это время звучит песня в исполнении В. Добрынина «Синий туман»).
- Охарактеризуйте место ДС в природе и жизни человека (дети формулируют значение ДС и записывают его в тетрадь, как итог урока).
ІV. Домашнее задание.
Прочитать параграф 11 «Дисперсные системы»;
Ответить на вопросы 10-11;
*Подготовьте сообщение «Дисперсные системы вокруг нас».
*Подобдерите и запишите песни о ДС (вид ДС выберите сами).
Приложение 1
http://fcior.edu.ru/card/8533/ponyatie-o-dispersnyh-sistemah-dispersionnaya-sreda-i-dispersnaya-faza-koagulayciya-sinerezis.html
Приложение 2
Карточка – путеводитель: В пробирку с 2 мл бензола прилейте 2 мл раствора хлорида натрия и взболтайте. После чего сделайте вывод о характере системы.

 Получите свидетельство
Получите свидетельство Вход
Вход
























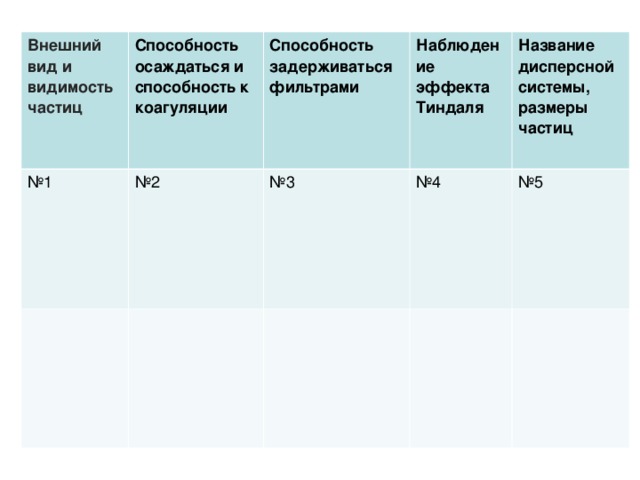










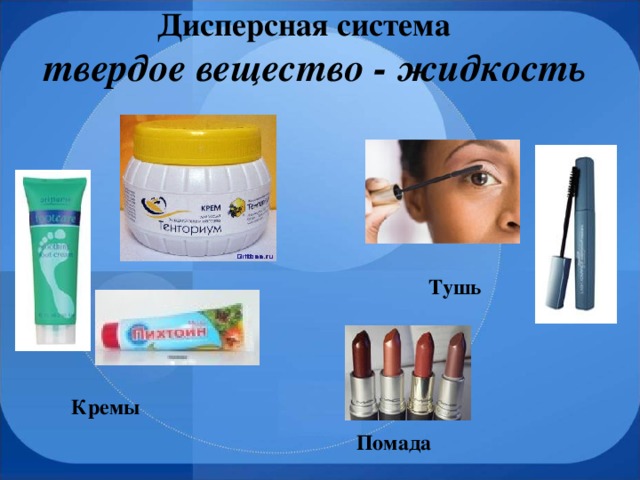

 100 нм. Это мутные системы, отдельные частицы которых можно заметить невооруженным глазом. Фаза и среда легко разделяются отстаиванием. Среда и фаза – жидкости Среда – жидкость, фаза – твердое вещество" width="640"
100 нм. Это мутные системы, отдельные частицы которых можно заметить невооруженным глазом. Фаза и среда легко разделяются отстаиванием. Среда и фаза – жидкости Среда – жидкость, фаза – твердое вещество" width="640"






















 Открытый урок "Дисперсные системы" (22.85 MB)
Открытый урок "Дисперсные системы" (22.85 MB)
 0
0 4300
4300 324
324 Нравится
0
Нравится
0




