
Основание как электролиты
 K 2 FeOH + ↔ Fe 2+ + OH - " width="640"
K 2 FeOH + ↔ Fe 2+ + OH - " width="640"
Основания - электролиты, которые при диссоциации образуют только один вид анионов - гидроксид-ионы ОН - .
Уравнение диссоциации с ильных оснований (щелочей)
NaOH Na + + OH -
Ba(OH) 2 Ba 2+ + 2OH -
Слабые многокислотные основания диссоциируют ступенчато.
Fe(OH) 2 FeOH + + OH - К 1 K 2
FeOH + ↔ Fe 2+ + OH -
 7 Метил- оранж " width="640"
7 Метил- оранж " width="640"
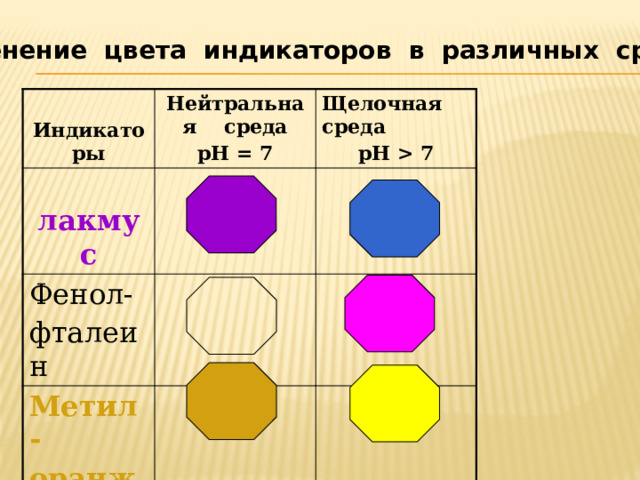
Изменение цвета индикаторов в различных средах
Индикаторы
Нейтральная среда
рН = 7
Щелочная среда
лакмус
Фенол-
фталеин
рН 7
Метил-
оранж

Общие свойства оснований :
1. Основания взаимодействуют с кислотами (реакция нейтрализации):
NaOH + HCl = NaCl + H 2 O
2. Взаимодействуют с кислотными оксидами
Ca(OH) 2 +SO3 =
3. Взаимодействуют с солями :
Cu(NO 3)2 + 2NaOH Cu(OH)2 ↓ + 2NaNO 3

Специфические свойства нерастворимых оснований:
При нагревании разлагаются
Fe(OH) 2 FeO + H 2 O
кислота

Амфотерные гидроксиды
способны вступать во взаимодействие как с кислотами так и со щелочами .
Очень слабые электролиты
H + + RO - ↔ ROH ↔ R + + OH -
1. Al(OH) 3 + HCl AlCl 3 + H 2 O
2. Al(OH) 3 + NaOH NaAlO 2 + 2H 2 O
3. При нагревании разлагается
Al(OH) 3 Al 2 O 3 + H 2 O

 Получите свидетельство
Получите свидетельство Вход
Вход











 Основание как электролиты (176.48 KB)
Основание как электролиты (176.48 KB)
 0
0 1311
1311 17
17 Нравится
0
Нравится
0


