Введение
Одним из способов изучения чистоты воздуха является исследование снега. Снеговой покров накапливает в своем составе практически все вещества, поступающие в атмосферу. В связи с этим снег можно рассматривать как своеобразный индикатор чистоты воздуха.
В зависимости от источника загрязнения и его удаленности изменяется состав снегового покрова, поэтому были взяты пробы снега на анализ в различных местах на территории д. Верхняя Мактама. А именно: у дороги по улице Октября, вблизи котельной, на территории птицефабрики, школы, в конце улицы Крупской, С. Хакима. В результате этих исследований выяснилось, что вблизи автодороги на ул. Октября, территории фабрики и школы снег содержит повышенное содержание соединений серы. Вблизи автомобильных дорог и котельных наблюдаются повышенное содержание соединений азота.
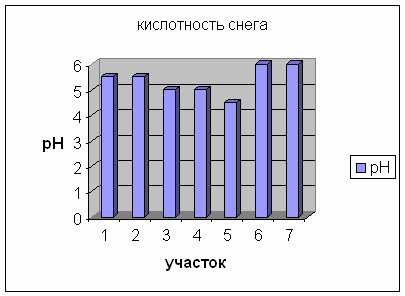
Информативным является показатель величины рН снеговых вод. В малозагрязненном снеге, взятом в конце ул. Крупской, С. Хакима он изменяется от 5,5 до 5,8. В близи котельной, как правило, рН снега имеет более высокие значения, т.е. обозначает слабощелочную или щелочную среду, что связано с выпадением зольных частиц, содержащих соединения гидрокарбонатов калия, магния, повышающий pH снеговой воды.
Вдоль автомобильной дороги, на территории фабрики и школы снеговой покров уменьшается, что свидетельствует о кислотности осадков, т.к. продукты сгорания содержат оксиды серы, азота и углерода.
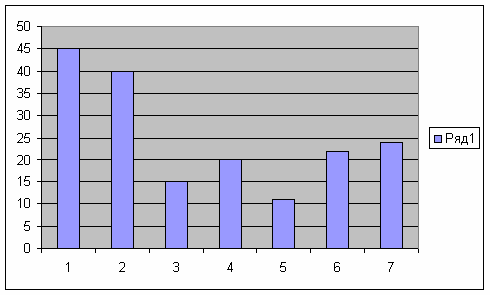
Хорошим показателем чистоты воздуха, на мой взгляд, является определение наличия нерастворимых веществ в снеговой воде. Для определения этого мы на всех участках набрали одинаковое количество снега – 3 кг. Сразу после таяния провели анализ на цвет, прозрачность и запах. Затем пробы профильтровали, высушили осадки на фильтре и взвесили. Даже невооруженным взглядом было видно, что самый грязный снег находился на территории фабрики и по улице Октября, здесь масса нерастворимых частиц превышала показатели других участков в несколько раз. Следующими по загрязненности шли участки котельной и территория школы.
Самыми чистыми оказались улицы Крупской, С. Хакима, но и там наблюдаются нерастворимые осадки, т.к. это районы частного сектора, где люди в зимнее время топят печи.
Определение кислотности снега
Промышленные предприятия выбрасывают в атмосферу оксиды азота и серы; соединяясь с водой, они образуют кислоты. Кислотные осадки губительно действуют на живые организмы, строения, памятники. Используя индикаторную бумагу, можно определить наличие кислот в осадках и предсказать, к каким последствиям приведет таяние снега.
Если в пробе pH меньше 5,6, то это говорит о кислотных выпадениях в изучаемом районе в течение зимы, что наблюдается на участках приближенных к фабрике: 3,5
Органолептические показатели снеговой воды. Прозрачность
Прозрачность снеговой воды зависит от количества взвешенных частиц и содержания химических веществ.
Мерой прозрачности служила высота столба воды (в см), при которой можно различить на белой бумаге стандартный шрифт с высотой букв 3,5 мм. Для определения прозрачности налили воду в высокий цилиндр с внутренним диаметром 2,5 см и дном из плоско отшлифованного стекла. Цилиндр установили неподвижно над шрифтом на высоте 4 см. Просматривая шрифт сверху через столб воды и доливая воду в цилиндр, нашли высоту столба воды.
Запах
Запах воды обусловлен наличием в ней пахнущих веществ, которые попадают в нее естественным путем.
Для определения запаха снеговой воды мы взяли ее 100 мл при комнатной температуре, налили в колбу вместимостью 200 мл с широким горлом, накрыли стеклом и встряхнули вращательными движениями. Открыв стекло, быстро определили запах и его интенсивность, используя таблицы, приведенные далее.
Характер и род запаха воды естественного происхождения.
Выявление химических загрязнений в снегу
Используя специальные методики, можно выявить в снеговой пробе конкретные химические вещества, которые попадают в снег из атмосферы. Для этого использовала отфильтрованную снеговую воду.
Методики определения химических веществ.
SO42-. К 10 мл пробы прибавить 1мл хлорида бария. При содержании SO42- возникает помутнение.
SO32- . К 10 мл пробы прибавить слабый раствор марганцовокислого калия. При содержании сульфит ионов розовый цвет исчезает.
S2-. К 10 мл пробы добавить нитрат серебра. Если есть сульфид ионы, то появиться слабое помутнение.
CL-. К 10 мл пробы добавить ацетат свинца. При наличии хлорид ионов выпадает осадок черного цвета.
NH4-. К 10 мл пробы добавить р-р щелочи сильной концентрации и подогреть. При наличии ионов аммония появится запах аммиака.
Весь материал - в документе.

 Получите свидетельство
Получите свидетельство Вход
Вход











 Определение состояния атмосферы (84 КB)
Определение состояния атмосферы (84 КB)
 0
0 444
444 30
30 Нравится
0
Нравится
0






