
Общая характеристика неметаллов
Образовательный портал"Мой университет"-www.moi-universitet.ru Факультет "Реформа образования"-www.edu-reforma.ru
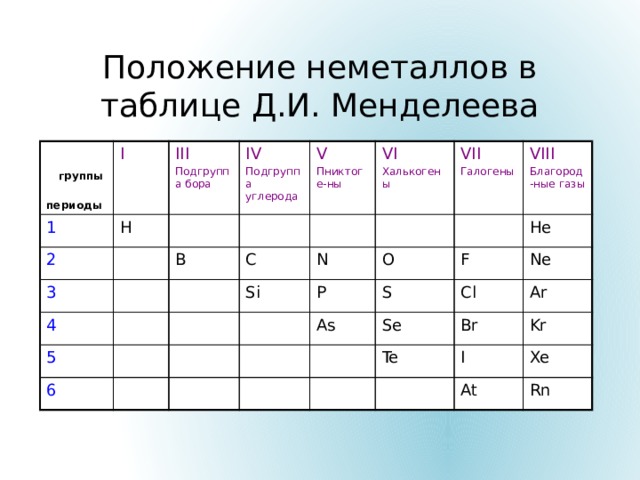
Положение неметаллов в таблице Д.И. Менделеева
группы
I
1
H
2
периоды
III
IV
3
Подгруппа бора
Подгруппа углерода
V
4
B
Пниктоге-ны
VI
5
C
Si
Халькогены
6
N
VII
Галогены
O
P
VIII
He
S
Благород-ные газы
F
As
Cl
Se
Ne
Ar
Te
Br
I
Kr
Xe
At
Rn
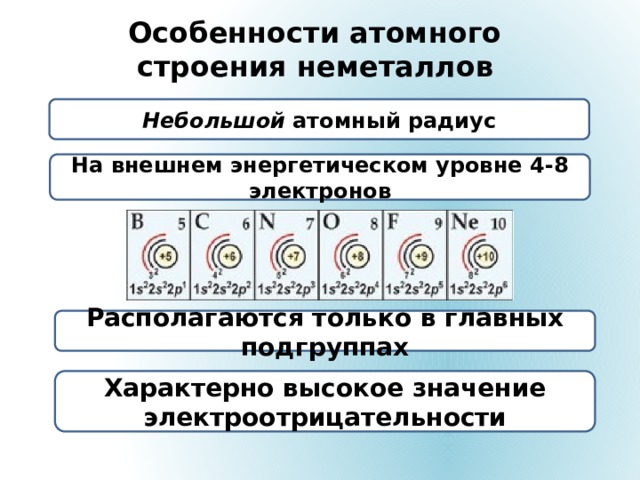
Особенности атомного строения неметаллов
Небольшой атомный радиус
На внешнем энергетическом уровне 4-8 электронов
Располагаются только в главных подгруппах
Характерно высокое значение электроотрицательности

Простые вещества - неметаллы
- Образованы за счет ковалентных неполярных связей
- Агрегатное состояние : в основном газы (H 2 , O 2 , N 2 , F 2 , Cl 2 ), летучие жидкости (Br 2 ) и легкоплавкие твердые вещества (P белый , I 2 , S)
Бром
Красный фосфор
Хлор
Йод
Сера
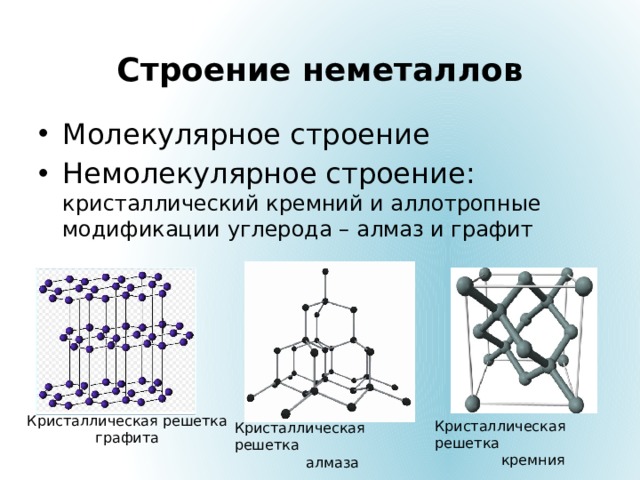
Строение неметаллов
- Молекулярное строение
- Немолекулярное строение: кристаллический кремний и аллотропные модификации углерода – алмаз и графит
Кристаллическая решетка
графита
Кристаллическая решетка
кремния
Кристаллическая решетка
алмаза

Физические свойства неметаллов
- Низкая электропроводность: неметаллы практически не проводят электрический ток. Исключение: алмаз и кремний
- Цвет и отсутствие металлического блеска неметаллы имеют разнообразную окраску, а металлическим блеском могут «похвастаться» только графит, кристаллический кремний и йод
йод
графит
кристаллический кремний

Химические свойства неметаллов
Могут выступать в качестве окислителей и восстановителей . Способность проявлять те или иные свойства определяются электроотрицательностью:
- Взаимодействие с металлами – кислород реагирует с Ме с образованием оксидов, сера – сульфидов, хлор – хлоридов: 2Сa + O 2 = 2CaO – оксид кальция Fe + S = FeS – сульфид железа (II) 2Al + 3Cl 2 = 2AlCl 3 – хлорид алюминия

Химические свойства неметаллов
- Взаимодействие с другими неметаллами – в роли окислителя выступает тот неМе, у которого выше электроотрицательность (см.слайд 9): 3F 2 + S = SF 6 – фторид серы (VI) O 2 + S = SO 2 – оксид серы (IV) Сl 2 + S = SCl 2 – хлорид серы (II) 3H 2 + N 2 = 2NH 3 – нитрид водорода или аммиак
- Окисление неМе сложных веществ – сильные окислители: F 2 , O 2 , Cl 2 : 2F 2 + 2H 2 O = 4HF + O 2 2SO 2 + O 2 = 2SO 3 – вторая стадия получения серной кислоты H 2 SO 4

 Получите свидетельство
Получите свидетельство Вход
Вход











 Общая характеристика неметаллов (940.89 KB)
Общая характеристика неметаллов (940.89 KB)
 0
0 1111
1111 113
113 Нравится
0
Нравится
0


