
СОСТАВЬТЕ МОЛЕКУЛЯРНЫЕ ФОРМУЛЫ АЛКАНОВ С ЧИСЛОМ УГЛЕРОДНЫХ АТОМОВ, РАВНЫМ:
- - 6
- - 8
- - 2
ДАЙТЕ НАЗВАНИЯ ПОЛУЧЕННЫМ СОЕДИНЕНИЯМ.
- СОСТАВЬТЕ МОЛЕКУЛЯРНЫЕ ФООМУЛЫ РАДИКАЛОВ, СООТВЕТСТВУЮЩИХ АЛКАНАМ ИЗ ПРЕДЫДУЩЕГО ЗАДАНИЯ. ДАЙТЕ ИМ НАЗВАНИЯ
- - 3
- - 7
- - 9
ДАЙТЕ НАЗВАНИЯ ПОЛУЧЕННЫМ СОЕДИНЕНИЯМ.
- СОСТАВЬТЕ МОЛЕКУЛЯРНЫЕ ФООМУЛЫ РАДИКАЛОВ, СООТВЕТСТВУЮЩИХ АЛКАНАМ ИЗ ПРЕДЫДУЩЕГО ЗАДАНИЯ. ДАЙТЕ ИМ НАЗВАНИЯ

АЛКЕНЫ С n H 2n
Цель урока: рассмотреть получение алкенов, химические свойства на основе их строения и применение алкенов.

АЛКЕНЫ
- АЦИКЛИЧЕСКИЕ НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ, КОТОРЫЕ СОДЕРЖАТ В МОЛЕКУЛЕ ОДНУ ДВОЙНУЮ СВЯЗЬ МЕЖДУ АТОМАМИ С
С n H 2n
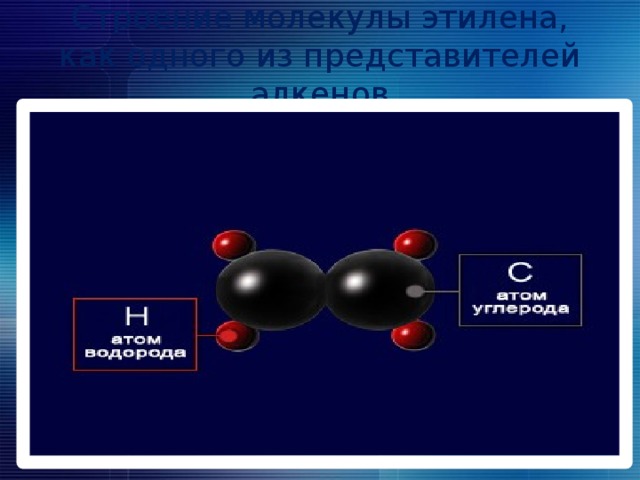
Строение молекулы этилена, как одного из представителей алкенов

Изомерия и гомологический ряд алкенов
Изомерия углеродного скелета:
CH 2 =CH-CH 2 -CH 3 бутен-1
CH 2 =C –CH 3 2- метилпропен
CH 3
Изомерия положения двойной связи:
CH 2 =CH-CH 2 -CH3 - бутен-1
CH 3 -CH=CH-CH 3 - бутен -2
Межклассовая изомерия:
CH 2 =CH-CH 2 -CH 2 -CH 3 - пентен
- циклопентан
Пространственная изомерия
CH 3 H
C=C транс- пентен-2
H C 2 H 5
H H
C=C цис-пентен-2
CH 3 C 2 H 5
Гомологический ряд:
C 2 H 4 этен
C 3 H 6 пропен
C 4 H 8 бутен
C 5 H 10 пентен
C 6 H 12 гексен
C 7 H 14 гептен
C 8 H 16 октен
C 9 H 18 нонен
C 10 H 20 декен
Клок Г.Д. учитель химии г.Нижневартовск

ЭТИЛЕН – РОДОНАЧАЛЬНИК ГОМОЛОГИЧЕСКОГО РЯДА АЛКЕНОВ

ПРАВИЛА ПОСТРОЕНИЯ НАЗВАНИЙ АЛКЕНОВ
- СТР. 35, СТР. 27

Получение алкенов
ДЕ ГИДРИРОВАНИЕ АЛКАНОВ
АЛК АН → АЛК ЕН + ВОДОРОД
Ni, t=500C
Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2
эт ан эт ен
(эт илен )
(-CH 2 -CH 2 -) n → t n CH 2 =CH 2
полиэтилен (мономер)
(полимер)

ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕ ГИДРАТАЦИЯ СПИРТОВ
СПИРТ → АЛК ЕН + ВОДА
Н Н Н 2 SO 4(конц.)
t≥140C ,
Н-С – С-Н → Н 2 С = СН 2 + Н 2 О
Н ОН
эт илен
ДЕ ГАЛОГЕН ИРОВАНИЕ
t
Н 2 С – СН 2 + Zn → Н 2 С = СН 2 + ZnBr 2
Br Br
1,2-дибромэт ан (эт илен )

ДЕ ГИДРО ГАЛОГЕН ИРОВАНИЕ
УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ
спиртовой
H H раствор
Н-С–С-Н+KOH→Н 2 С=СН 2 +KCl+H 2 O
Н Cl эт ен
хлорэт ан (эт илен )
Клок Г.Д. учитель химии г.Нижневартовск

Качественные реакции на этилен
Клок Г.Д. учитель химии г.Нижневартовск
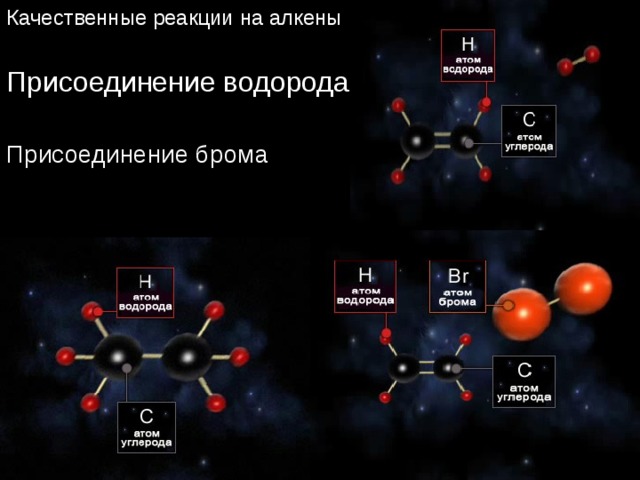
Качественные реакции на алкены
Присоединение водорода
Присоединение брома
Клок Г.Д. учитель химии г.Нижневартовск
6
![Гидрирование: CH 2 CH-CH 2 -CH 3 + H 2 → CH 2 – CH -CH 2 -CH 3 Н Н Галогенирование: CH 2 ── CH –CH 2 -CH 3 + Br 2 → CH 2 ─ CH ─ CH 2 ─ CH 3 Br Br Мягкое окисление: CH 2 ─ CH 2 + [ O] + H 2 O→ CH ─ CH OH OH O Глубокое окисление: CH 3 ─CH ─ CH─CH 3 +KMnO 4 +HNO 3 → 2 CH 3 ─C OH Клок Г.Д. учитель химии г.Нижневартовск](https://fsd.videouroki.net/html/2017/11/02/v_59fa78897528a/img13.jpg)
Гидрирование:
CH 2 CH-CH 2 -CH 3 + H 2 →
CH 2 – CH -CH 2 -CH 3
Н
Н
Галогенирование:
CH 2 ── CH –CH 2 -CH 3 + Br 2 →
CH 2 ─ CH ─ CH 2 ─ CH 3
Br
Br
Мягкое окисление:
CH 2 ─ CH 2 + [ O] + H 2 O→
CH ─ CH
OH
OH
O
Глубокое окисление:
CH 3 ─CH ─ CH─CH 3 +KMnO 4 +HNO 3 →
2 CH 3 ─C
OH
Клок Г.Д. учитель химии г.Нижневартовск
![Гидрогалогенирование: CH 2 ─ CH ─ CH 2 ─ CH 3 + HCl → CH 2 ─ CH ─ CH 2 ─ CH 3 Cl H Гидратация: CH 2 ─ CH ─ CH 2 ─ CH 3 + H 2 O H+ → CH 2 ─ CH ─ CH 2 ─CH 3 OH H Полимеризация: n CH 2 ─ CH 2 R+ vh → [ CH 2 ─ CH 2 ] n мономер Горение: CH 2 ═ CH 2 + 3O 2 → 2CO 2 +2H 2 O Клок Г.Д. учитель химии г.Нижневартовск](https://fsd.videouroki.net/html/2017/11/02/v_59fa78897528a/img14.jpg)
Гидрогалогенирование:
CH 2 ─ CH ─ CH 2 ─ CH 3 + HCl →
CH 2 ─ CH ─ CH 2 ─ CH 3
Cl
H
Гидратация:
CH 2 ─ CH ─ CH 2 ─ CH 3 + H 2 O H+ →
CH 2 ─ CH ─ CH 2 ─CH 3
OH
H
Полимеризация:
n CH 2 ─ CH 2 R+ vh →
[ CH 2 ─ CH 2 ] n
мономер
Горение:
CH 2 ═ CH 2 + 3O 2 →
2CO 2 +2H 2 O
Клок Г.Д. учитель химии г.Нижневартовск

Проверочная работа
1.Какие вещества, формулы которых приведены ниже относятся к:
а) алканам б) алкенам
С 6 Н 14 С 5 Н 8 С 4 Н 10 С 5 Н 10 С 3 Н 8 С 2 Н 2 С 2 Н 4 С 6 Н 6 С 7 Н 14
Алканы:
Алкены
гексан
С 6 Н 14
пентен
С 5 Н 10
бутан
С 4 Н 10
этилен
С 2 Н 4
С 3 Н 8
пропан
гептен
С 7 Н 14
Клок Г.Д. учитель химии г.Нижневартовск

Закончите уравнения реакций
CH 2 =CH–CH 3 + HCl →
CH 3 ─ CHCl ─ CH 3
CH 3 –CH=CH–CH 3 + H 2 →
CH 3 ─ CH 2 ─ CH 2 ─ CH 3
CH 3 –CH 2 –CH 3 → H 2 +
CH3 ─ CH ═ CH 2
CH 2 ═ CH─CH 2 ─CH 3 + O 2 →
4CO 2 + 4H 2 O
6
Клок Г.Д. учитель химии г.Нижневартовск

 Получите свидетельство
Получите свидетельство Вход
Вход











 Непредельные углеводороды - алкены (1.18 MB)
Непредельные углеводороды - алкены (1.18 MB)
 0
0 1310
1310 24
24 Нравится
0
Нравится
0


