Тема урока: «Гетероциклические соединения»
Цели урока:
1. Ввести понятие «ароматические гетероциклические соединения», рассмотреть состав и строение молекул пиридина и пиррола, охарактеризовать негативную роль табакокурения и наркомании в жизни человека (обучающая, воспитывающая).
2. Продолжить формирование научного мировоззрения (воспитывающая).
3. Способствовать развитию логического мышления (умения сравнивать, обобщать, делать выводы) (развивающая).
Оборудование:
Видеоурок РЭШ №13 https://resh.edu.ru/subject/lesson/6296/main/, ПСХЭ Д.И. Менделеева.
Ход урока
Подготовка к восприятию нового материала (10 мин)
Опрос учащихся по домашнему заданию.
Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения: карбонат кальция - оксид кальция - карбид кальция - ацетилен - бензол - нитробензол - анилин - триброманилин
Изучение нового материала (12 мин).
Гетероциклические соединения – вещества, в молекулах которых в состав цикла входит один или несколько атомов других элементов (O, S, N, P и др.).
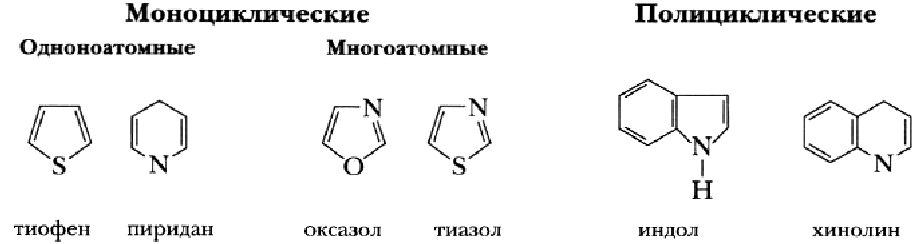
![]() тиофен
тиофен
Наиболее важное биологическое значение имеют азотсодержащие пяти- и шестичленные гетероциклы (пиридин, имидазол и никотиновая кислота).
Ароматические гетероциклы – соединения, имеющие плоский замкнутый цикл и сопряженную электронную систему, содержащую (4n+2) π-электрона, где n=1,2,3 и т.д.
Ароматические гетероциклы по свойствам напоминают бензол и др. ароматичекие соединения: высокая стабильность, не вступают в реакции присоединения, вступают в реакции замещения.
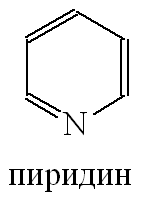
Пиридин C5H5N.
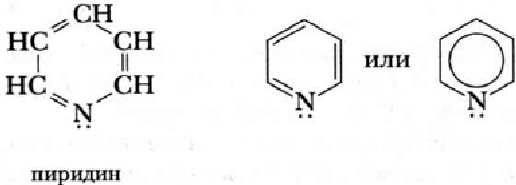
Молекула пиридина образуется в результате замены группы СН- на группу NH-. Атом азота в цикле имеет неподеленную пару электронов, которая не участвует в образовании σ-связей и сопряженной π-системы.
Физические свойства. Бесцветная жидкость, хорошо растворимая в воде и органических растворителях, с характерным неприятным запахом. Очень ядовит.
Химические свойства. Пиридин можно рассматривать как амин. Пиридин обладает основными свойствами благодаря паре электронов атома азота. Изменяет цвет индикатора. Присоединяет протон при реакциях с минеральными кислотами.
С трудом вступает в реакцию нитрования:
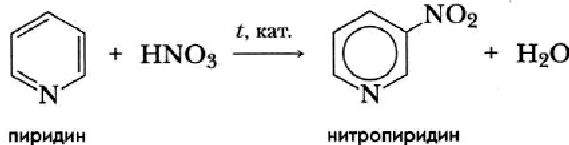
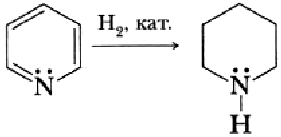
Вступает в реакцию гидрирования в присутствии катализатора:
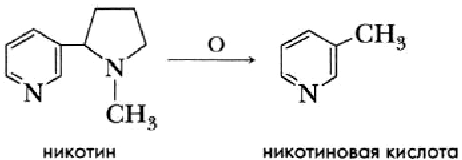
К производным пиридина относится алкалоид никотин:
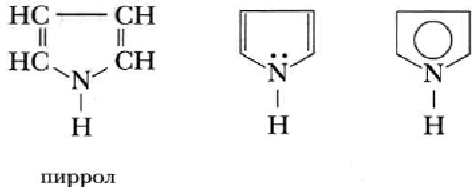
Пиррол
Строение молекулы. Молекула пиррола – пятичленный цикл с одним атомом азота в цикле. В создании ароматического кольца участвуют 4р-электрона атома углерода и неподеленная электронная пара атома азота.
Физические свойства. Пиррол – бесцветная жидкость, малорастворим в воде, на воздухе быстро окисляется (буреет).
Химические свойства. Проявляет ароматические свойства. Как бензол, вступает в реакцию восстановления водородом и нитрования. В отличие от бензола легко нитруется.
Ядро пиррола входит в состав хлорофилла, гемоглобина.
Закрепление нового материала (16 мин).
Решение задач: 1. Решение задачи на вычисление выхода продукта реакции.
Условие задачи: При йодировании 50 г пиррола получили 360 г тетрайодпиррола. Чему равен выход продукта реакции? Ответ запишите с точностью до десятых долей.
Шаг первый: вычислим молярную массу пиррола.
![]() М1 = 4·12 + 14 + 5·1 = 67 г/моль.
М1 = 4·12 + 14 + 5·1 = 67 г/моль.
Шаг второй: вычислим молярную массу тетрайодпиррола:
![]() М2 = 4·12 + 14 + 4·127 + 1 = 571 г/моль.
М2 = 4·12 + 14 + 4·127 + 1 = 571 г/моль.
Шаг третий: найдем количество тетрайодпиррола при 100%-ном выходе. Для этого составим пропорцию:
50 : 67 = х : 571, откуда х = (50·571) : 67 = 426 г.
Шаг четвертый: найдём выход продукта реакции.
(360 : 426)·100 = 84,5 %.
Ответ: 84,5.
2.Решение задачи на определение необходимого количества реагента.
Условие задачи: Взаимодействием ацетилена и формальдегида с последующей обработкой промежуточного продукта аммиаком получают пиррол. Выход реакции при использовании 20%-ного избытка аммиака составляет 85%. Какой объём аммиака (л), измеренный при нормальных условиях, необходим для получения 0,5 кг пиррола?
Ответ запишите с точностью до десятых долей.
Шаг первый: В молекуле аммиака один атом азота и в молекуле пиррола тоже один атом азота, то есть для получения 1 моль пиррола требуется (без учёта избытка) 1 моль аммиака. При нормальных условиях 1 моль аммиака занимает объём, равный 22,4 л.
Шаг второй: вычислим молярную массу пиррола:
![]() М1 = 4·12 + 14 + 5·1 = 67 г/моль.
М1 = 4·12 + 14 + 5·1 = 67 г/моль.
Шаг третий: составим пропорцию и найдём необходимый объём аммиака.
х : 22,4 = 500 : 67. (0,5 кг = 500 г). х = 167 л.
Шаг четвёртый: найдём объём аммиака с учётом 20%-ного избытка.
167 л – 100 %;
V л – 120 %.
V = (167·120) : 100 = 200,6 л.
Ответ: 200,6.
IV. Подведение итогов учебного занятия, рефлексия (2 мин).
"Синквейн".
В конце урока обучающимся предлагается написать синквейн на основе изученного материала. Синквейн – это пятистрочная строфа.
1-я строка – одно ключевое слово, определяющее содержание синквейна;
2-я строка – два прилагательных, характеризующих данное понятие;
3-я строка – три глагола, обозначающих действие в рамках заданной темы;
4-я строка – короткое предложение, раскрывающее суть темы или отношение к ней;
5-я строка – синоним ключевого слова (существительное).
Пиролл
Важный, бесцветный.
Лечит, работает, переносит.
Молекулы хлорофилла, гемоглобина образует.
Жизнь.
V. Домашнее задание: §30, презентацию подготовить по теме: «Табакокурение и наркомания – угроза жизни человека» - 10 слайдов.
![]()

 Получите свидетельство
Получите свидетельство Вход
Вход












 Конспект урока по химии в 10 классе "Гетероциклические соединения" (168 KB)
Конспект урока по химии в 10 классе "Гетероциклические соединения" (168 KB)
 0
0 1655
1655 253
253 Нравится
0
Нравится
0


