Тема урока: Алкены. Состав, строение, получение и применение алкенов.
Цель: изучить строение, состав ,свойства и способы получения алкенов.
Задачи урока:
Образовательные – развить полученные ранее теоретические представления об умении давать названия соединений по систематической номенклатуре, познакомить учащихся с гомологическим рядом алкенов. Рассмотреть особенности их химического и электронного строения. Рассмотреть промышленные и лабораторные способы получения алкенов. Показать место и значение алкенов среди углеводородов. Углубить и конкретизировать понятия о сигма-связи и пи - связях, о механизмах химических реакций
Воспитательные – продолжить формирование естественнонаучной картины мира, а также общеучебных навыков: внимания, эстетики оформления записей лекционного материала, умения наблюдать, формулировать выводы и обобщать информацию.
Развивающие – развить умение учащихся на основе теоретических знаний сравнивать, анализировать, обобщать, логически рассуждать, устанавливать взаимосвязь строения и свойств веществ, умения составлять уравнения химических реакций с участием непредельных углеводородов.
Тип урока
Урок формирования и совершенствования знаний.
Методы обучения – словесные, наглядные, исследовательские. Метод проблемного изложения, диалогический метод, устный опрос, устный и письменный контроль, самоконтроль, лабораторная работа.
Оборудование: прибор для получения газов, этиловый спирт, концентрированная серная кислота, спички, спиртовка, песок, презентация по этилену, таблицы «Строение молекулы этилена» , конструктор атомов.
Ход урока:
1 . Приветствие учеников.
-За этот период времени вы уже успели изучить некоторые классы органических соединений. Давайте вспомним, какие классы вы уже знаете, и какое практическое применение они имеют?
-алканы общая формула СnH2n+2,применяеются как топливо, горючее для двигателей внутреннего сгорания, растворители, для получения фреонов.
-Сегодня мы познакомимся еще с одним классом неорганического соединения.
Общая формула этого класса СnH2n
Гомологический ряд начинается со 2 атома углерода
Посмотрим на строение этого класса, возьмите конструктор и соберите вещество, которое содержит 2 атома углерода исходя из общей формулы, вычислите количество атомов водорода.
-С2Н4
- Какие вы видите изменения по сравнению с аланами?
-Появилась 2-я связь
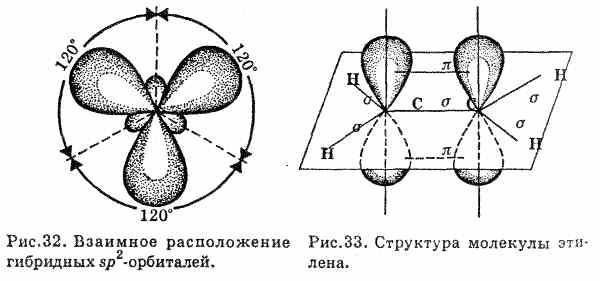
-Правильно, а это означает, что углерод при 2-ой связи находиться SP2-гибридизации одна s- и две р-орбитали смешиваются по форме, давая три гибридные орбитали, которые образуют -связи. Третья р-орбиталь каждого из этих двух атомов используется для образования -связи между ними и поэтому в гибридизации не участвует. Все атомы молекулы этилена (и все -связи) лежат в одной плоскости, угол между -связями равен 120° р-орбитали обоих атомов углерода ориентированы перпендикулярно этой плоскости, при их «боковом» перекрывании образуется -связь. Плотность -связи (условная плотность, в которой лежит максимум ее электронной плотности) перпендикулярна плоскости -связей, двойные связи не равноценны ; сигма - связь – более прочная ; пи –связь- легче рвется, более реакционноспособна, при двойной связи атомы находятся в одной плоскости ;электроны «пи» связи образуют боковое перекрывание.
Показываю невозможность вращения атомов углерода вокруг двойной связи на моделях, длина связи 0,134 нм и этот класс называется алкены или непредельные углеводороды или олефины (от лат. olefiant - масло — старое название, но широко используемое в химической литературе. Поводом к такому названию послужил хлористый этилен, полученный в XVIII столетии, — жидкое маслянистое вещество.
http://files.school-collection.edu.ru/dlrstore/0abb8989-4185-11db-b0de-0800200c9a66/x10_064.swf
Систематические названия алкенов производятся от корней названий алканов с заменой суффикса – ан – ен: С2Н4 – этен, С3Н6 – пропен, С4Н8 – бутен;
Сохраняются также традиционные названия с заменой суффикса – ан
на – илен: С2Н4 – этилен, С3Н6 – пропилен, С4Н8 – бутилен; использование названия амилен для алкена С5Н10 не рекомендуется.
Положение двойной связи С=С в изомерах строения (начиная с алкена С4) указывается цифрой после названия:
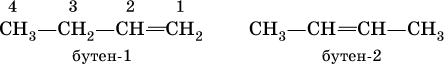
Радикал этилена – этенил СН2=СН – обычно называют винил, пропена – пропенил СН2=СН – СН2 – именуют аллил. При названии выбирают углеродную цепочку которая имеет 2-ю связь. Нумерацию цепи начинают с того конца, к которому ближе расположена эта связь. Посмотрите на таблицу( открываю ссылку) http://files.school-collection.edu.ru/dlrstore/0abb898b-4185-11db-b0de-0800200c9a66/x10_066.jpg
Получим этилен в лаборатории из этилового спирта с концентрированной . серной кислотой.
-Какие способы существуют по собиранию газов?
-Путём вытеснения воздуха, путём вытеснения воды.
-Как расположить газоотводную трубку, для сбора этилена, вверх или вниз
для вытеснения воздуха?
Доказать расчётом:
-Мг воздуха равно 29, Мг этилена равно 26.
Вывод: этилен легче воздуха, по этому газоотводную трубку располагаем
наверх.
- Можно ли собрать этилен путем вытеснения воды?
-Да , т.к этот газ плохо растворим в воде.
Собираем прибор для получения этилена методом вытеснения воздуха сначала на фланелеграфе
Собираем прибор, для получения этилена напоминаем о Т.Б.. При нагревание концентрированной серной кислоты с этиловый спиртом в присутствии кварцевого песка
С2Н5ОН = С2Н4 + Н2О в присутствии катализатора серной кислоты получаем этилен. Наблюдаем выделение бесцветного газа, получившиеся газ поджигаем и наблюдаем за характером пламени – светящее, немного коптящее.
- Учащие пишут реакцию и уравнивают ее.
С2Н4 + ЗО2= 2СО2+ 2Н2О
- Применение алкенов
1 – получение горючего с высоким октановым числом;
2 – пластмасс;
3 – взрывчатых веществ;
4 – антифризов;
5 – растворителей;
6 – для ускорения созревания плодов;
7 – получение ацетальдегида;
8 – синтетического каучука. рименение алкенов
Алкены — одни из наиболее важных органических соединений. Объясняется это их высокой реакционной способностью, доступностью и низкой стоимостью.
Этилен же является природным стимулятором созревания плодов. Его накопление в плодах ускоряет их созревания.
По этому этилен использует для искусственного ускорения созревания плодов. Это привело к мысли синтезировать подобное вещество. Это вещество было синтезировано учёными в1946г М.И.Кабачником и П. А.Российской и получило название (этрел) попадая в растение, разлагается с выделением этилена.(видео)
Опытами установлено, что для дозревания помидоров необходима концентрация этилена 1 :2000 т.е. на один объём этилена 2000 объёмов воздуха. Исходя, из этого решаем задачу.
Задача
Объём камеры для дозревания помидор равен 10м3 Рассчитайте, сколько надо взять этилового спирта (С2Н5ОН) чтобы получить, нужное вам для опыта количество этилена С2Н5ОН = С2Н4 + Н2О если опытами установлено, что для дозревания помидоров необходима концентрация этилена 1:2000, то есть 1 объём этилена на 2000 объёмов воздуха. Учитывая, что под действием этилена, томаты зреют за 5-6 дней, а без него - за 10-12 дней.
Какой объём воздуха (н.у.) потребуются для сжигания этилена полученного в результате данных условий? Объёмная доля кислорода в воздухе равна 21%.
Дано:
V(камеры )10 м3- 1 0000л
V(возд)= 1 : 2000
С2Н5ОН = С2Н4 + Н2О
Найти: m (С2Н5ОН)-? V (воздуха)-?
Решение:
С2Н5ОН =CН4+Н2О
1. Рассчитаем, какой V необходим для создания концентрации этилена 1:2000
в камере V 10000л.
V(С2Н4) 10000:2000= 5л ежедневно
2. на 6 дней
V(С2Н4 )=5*6=30л.
3.V (С2Н4) = 30л:22,4л/моль=1,339моль
4.ИзУХР
1моль(С2Н5ОН) — 1моль(С2Н4 )
X моль(С2Н5ОН) — 1,339моль(С2Н4)
Х (С2Н4)= 1,339моль
5. m= Мn
М(С2Н5ОН)= 12*2+1 *5+16+1=46г/моль
m= 46*1,339= 61г (С2Н5ОН)
6. С2Н4 + ЗО2= 2СО2+ 2Н2О
n (С2Н4) = V/Vm;
n (С2Н4)= 30л:22,4л/моль=1,339моль
ИзУХР
1 моль(С2Н4) ——— З моль(О2)
X моль(С2Н4)— — 1,339молъ(С2Н4)
X (О2)= 0,446 моль (О2 );
V (О2)= 22,4л/моль* 0,446моль= 9,99л
V возд.= V (О2)/ᵩ(О2)*100%
V возд.= 9,99л/21%*100%=47л
Вывод: На сегодняшнем уроке вы узнали не только о новом классе органического вещества его строении, а также получении и о практическом применении этилена и научились рассчитывать концентрацию его в воздухе, необходимую для дозревания плодов. Эта задача стоит остро перед государствами, у которых кроткое лето. Фрукты и овощи ввозятся из южных стран, где их собирают зелеными, чтобы они не испортились в дороге. В наших магазинах или на овощных базах фрукты подвергают действию этилена или этрела. Дома вы можете ускорить созревание томатов, если в комнату, теплицу поместить спелые яблоки, которые при созревании образуют этилен. А также повторили применение органических веществ/ Чтобы дополнить повторение я предлагаю вам написать тест.
Результаты теста вы узнаете сразу после его выполнения.
Теперь чуточку перед тестами отдохнем.
Я скажу себе, друзья,
Не боюсь я никогда
Ни диктанта, ни контрольной,
Ни стихов и ни задач,
Ни проблем и ни удач.
Я спокоен, терпелив,
Сдержан я и не хмурлив,
Просто не люблю я страх,
Я держу себя в руках.
Закрепление темы – тест
Тест по предельным непредельным углеводородам (Алкенам)
Вариант №1 Вариант №2
1.Среди перечисленных формул выберете алкен и запишите выбранную формулу буквой стоящей около выбранного вами ответа.
а) С3Н4 е) С4Н6
б) С3Н6 л) С4Н10
в) С3Н8 я) С4Н8
2.Какой тип гибридизации
у алкенов у алканов
выбранный ответ запишите буквой.
о) SР о) SР
п) SР3 и)SР3
р) SР2 с) SР2
3.Какое вещество обесцвечивает бромную воду, выбранный ответ запишите буквой.
д) СН4 е) С6Н6
а) С2Н4 л) С4Н10
г) С6Н6 м) С4Н8
4.Назовите вещество, выбранный ответ запишите буквой.
С6Н14 С4Н8
и)гексен д) бутан
п) бензол и) бутен
в) гексан с) бутин
5.Выберете правильный ответ
У какого углеводорода отсутствуют изомеры
л) гексан м) октан
о) метан х) пропан
с) пентан н) пентан
После того как вы ответили на вопросы теста и получили соответствующие буквы соберите из них слово. Вар-1 (Браво) Вар.-2 (Химия)

 Получите свидетельство
Получите свидетельство Вход
Вход












 Алкены, Состав, строение, получение и применение. (96 KB)
Алкены, Состав, строение, получение и применение. (96 KB)
 0
0 1070
1070 29
29 Нравится
1
Нравится
1


