На прошлых уроках мы уже затрагивали свойства твердых тел и говорили, что твердые тела иногда называются кристаллическими. Твердые тела сохраняют свой объем и форму в течение длительного времени. Итак, кристаллы — это твердые тела, молекулы (или атомы) которых занимают упорядоченные положения в пространстве. Например, если присмотреться, то можно убедиться, что все снежинки имеют правильную геометрическую форму.
Существует такое понятие, как анизотропия кристаллов, то есть зависимость физических свойств от направления внутри кристалла.
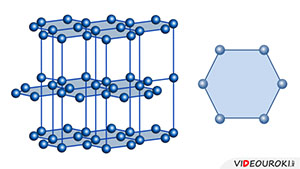
Пожалуй, один из самых наглядных примеров проявления анизотропии — это графитовый стержень карандаша. Когда вы пишете, слои графита остаются на бумаге. На это не нужно затрачивать много усилий. Однако, сломать графит поперек слоев довольно сложно. Конечно, карандаш ломается достаточно легко, но только потому, что стержень графита в нем довольно тонкий. Если мы рассмотрим кристаллическую решетку графита, то убедимся, что она имеет слоистую структуру.

Атомы углерода образуют правильные шестиугольники, и связи между этими шестиугольниками значительно прочнее, чем связи между слоями. Дело в том, что расстояние между слоями приблизительно вдвое больше, чем сторона шестиугольника.
Кристаллы классифицируются на монокристаллы и поликристаллы. Монокристаллы — это тела, состоящие из одиночного кристалла, а поликристаллы — это тела, состоящие из большого числа кристаллов.
Конечно же, в природе наиболее распространены поликристаллы. Почти все металлы являются поликристаллами. Примерами поликристаллов могут послужить медь, железо или свинец.

В качестве примера монокристаллов можно привести такие драгоценные камни, как рубин, алмаз или сапфир.

Кристаллы также классифицируются по типу связи атомов и молекул. Итак, существуют молекулярные кристаллы, ковалентные кристаллы, ионные кристаллы и металлические кристаллы.
Молекулярные кристаллы — это кристаллы, образованные из молекул. Как правило, такие кристаллы являются наименее прочными и имеют достаточно низкую температуру плавления. Например, молекулярные кристаллы образуются из водорода или гелия.
Ковалентные кристаллы — кристаллы, образованные посредством ковалентной связи. Ковалентные кристаллы, напротив, достаточно прочны и имеют высокую температуру плавления. Примерами ковалентных кристаллов могут послужить алмаз, германий или кремний.
Ионные кристаллы — это кристаллы, образующиеся за счет ионной связи, то есть связи посредством электростатического притяжения. Самым распространенным примером ионного кристалла является поваренная соль, которая состоит из ионов натрия и хлора.
Наконец, металлические кристаллы — это кристаллы, образующиеся за счет металлических связей. К таким кристаллам относятся все металлы.
Надо сказать, что не все твердые тела являются кристаллами. Также к твердым телам относятся аморфные тела, хотя они и обладают некоторыми свойствами жидкости. Несмотря на то, что аморфные тела могут сохранять свой объем в течение длительного времени, у них нет строгой кристаллической решетки. То есть порядок атомов не является таким строгим, как у кристаллов. Примерами аморфных тел могут послужить пластилин, канифоль или смола. В аморфных телах наблюдается такое явление, как изотропия, то есть их физические свойства одинаковы по всем направлениям. При низких температурах аморфные тела ведут себя как твердые, но при более высоких температурах, они начинают обладать свойствами жидкости. Например, при температуре 15-20 оС, вам придется приложить некоторые усилия, чтобы изменить форму капли смолы. Однако при температуре в несколько сотен градусов, смола начинает кипеть, и ведет себя как жидкость. Это нередко использовалось для обороны средневековых замков.
Рассмотрим еще один тип тел, который называется жидкими кристаллами. Жидкие кристаллы одновременно обладают анизотропией (что присуще кристаллам) и текучестью (что присуще жидкостям). Такое состояние вещества называется жидкокристаллическим. Со словом «жидкокристаллический», наверное, почти у всех ассоциируется монитор или телевизор. Дело в том, что существует определенная связь между повышением электрического напряжения и изменением ориентации молекул кристаллов. С помощью достаточно сложных манипуляций, таким образом, можно создавать различные изображения.
Если рассмотреть самый простой случай, то есть образование жидкого кристалла нитевидными молекулами, то можно отметить следующее: молекулы расположены параллельно друг другу, но при этом беспорядочно сдвинуты. Таким образом, строгая ориентация молекул существует только в небольших областях кристалла, а в общем объеме она не наблюдается.

Из-за этого, на границах этих областей происходит многократное преломление света, поэтому жидкие кристаллы непрозрачны. Если же поместить жидкий кристалл между двумя очень тонкими пластинами, то молекулы все же станут параллельны, что приведет к прозрачности кристалла. Используя различные напряжения, на различных участках дисплея можно отображать различные изображения. Но, это объяснение, конечно, дает очень и очень поверхностное представление о жидкокристаллических мониторах, а в действительности работа таких мониторов крайне сложна.
Существует отдельная ветвь физики, которая называется «физика твердого тела». В данный момент, эта наука занимается поиском различных способов создания неких материалов с заданными механическими и электромагнитными свойствами. Эта наука крайне важна, поскольку люди практически во всем используют твердые тела. Например, понимание поведения таких тел, как полупроводники или транзисторы — это яркий пример развития физики твердого тела.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 8750
8750

