Ферменты, или энзимы, − это органические катализаторы белковой природы, которые ускоряют реакции и необходимы для функционирования живых организмов.
В настоящее время известно более 2 000 ферментов. Эти ферменты обладают специфическими свойствами, поэтому и отличаются от неорганических катализаторов.
Во-первых, ферменты имеют большие значения относительной молекулярной массы. Молекуллярная масса их может варьировать от 105 до 107.
Второй особенностью ферментов является их селективность, то есть каждый фермент ускоряет только определённую реакцию или группу однотипных реакций.
В каждой клетке есть целый набор ферментов, которые разлагают белки до аминокислот, жиры до глицерина и жирных кислот, углеводы до моносахаридов. А из этих аминокислот, глицерина и жирных кислот, моносахаридов заново строятся белки, жиры и углеводы, которые необходимы организму.
Ещё И. П. Павлов назвал ферменты «носителями жизни».
Иван Петрович Павлов – русский учёный, физиолог, создатель науки о высшей нервной деятельности. В 1904 году стал лауреатом Нобелевской премии в области медицины и физиологии «за работу по физиологии пищеварения».

Избирательность ферментов можно сравнить только с ключом, который подходит только к одному замку, поэтому ферменты действуют на однотипные реакции, а немногие из них – только на одну реакци.
Ещё одной особенностью ферментов является способность к оптической изомерии. Оптическая изомерия харктерная для тех молекул, у которых есть хиральный атом. Как нельзя одеть левую перчатку на правую руку, так и невозможно заставить работать ферменты, у которых конфигурация оптического изомера не соответствует конфигурации активного центра. Поэтому в природе хиральные соединения представлены одной формой.
Ещё Луи Пастер в 1860 году подчёркивал: «Ассиметрия молекулярного строения, может быть, образует единственную чёткую границу, разделяющую химию живой и неживой природы».
Ферменты обладают высокой эффективностью. Например, в присутствии ферментов скорость реакции может возрастать в миллионы раз, по сравнению с реакциями, которые идут без ферментов. Кроме того, высокой эффектовностью объясняется быстрое восстановление ферментов в процессе их «работы».
В сыроделии используют фермент реннин, который вызывает свёртывание белков молока в количествах, которые в миллионы раз превышают его собственную массу. Такой же фермент вырабатывается в желудке у жвачных животных.
Большинство ферментов обладают эффективностью при температуре человеческого тела. Если температура тела человека ниже 35 0C или выше 42 0C, то человек погибает не столько от болезни, сколько от того, что ферменты в его организме перестают действовать и прекращаются обменные процессы.
Ферменты наиболее эффективны в опредлённой среде раствора, то есть при определённых значениях рН. рН среды может варьировать от 1,0 до 14,0. Так, фермент пепсин наиболее активен при РН от 1,5 до 2,0, то есть в сильнокислой среде, каталаза крови наиболее активная при рН около 7,0, то есть в нейтральной среде.
Каждая физиологическая жидкость в организме имеет определённое значение рН и отклонение от этой нормы может привести к тяжёлым заболеваниям. Так, желудочный сок имеет рН 1,7, плазма крови – 7,4, моча – 5,8, слюна – 6,8, сок поджелудочной железы – 8,8, сок тонкого кишечника – 6,5.

Ферменты также отличаются от неорганических катализаторов. Например, скорость ферментативной реакции гораздо выше. Так, 1 мг железа в каталазе заменяет 10 тонн неорганического железа как катализатора.
Ферменты бананов позволяют им дозревать даже после того, как их сняли с дерева (после обработки их специальными веществами – этиленом, ацетиленом, пропиленом).
Ферменты бывают однокомпонентными – простыми (как пепсин, трипсин, лизоцим), и двухкомпонентными или сложными, которые имеют компонент небелковой природы (например, аминотрансферазы, пероксидазы). Белковая часть сложных ферментов называется апоферментом, небелковая – кофактором. Кофактор, легко диссоциирующий из комплекса, называют коферментом. Кофактор, прочно связанный с апоферментом, называют простетической группой.

Основными функциями кофакторов являются:
· участие в акте катализа;
· осуществление контакта между ферментом и субстратом;
· стабилизация апофермента, особенно в присутствии денатурирующих агентов.
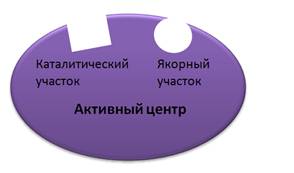
В ферментах выделяют активный центр – это область фермента, в которой происходит связывание и превращение субстрата. В активном центре выделяют два участка: якорный (контактный, связывающий) – отвечает за связывание и ориентацию субстрата в активном центре, и каталитический, который отвечает за осуществление реакции.
Выделяют два механизма действия ферментов:
· по Фишеру: субстрат подходит к ферменту (т.е. активному центру), как ключ к замку;
· по Кошланду: субстрат изменяет конформацию активного центра фермента, делая её комплементарной (рука-перчатка).
Ингибитор – вещество, специфически уменьшающее скорость ферментативной реакции. Принцип действия многих лекарств основан на процессе ингибирования. Например, при заболеваниях поджелудочной железы используют лекарственные препараты, которые ингибируют трипсин, который высвобождается в окружающие ткани и органы.
Классы ферментов:
· оксидоредуктазы – ферменты, ускоряющие окислительно-восстановительные реакции;
· трансферазы – ферменты, ускоряющие реакции переноса функциональных групп;
· гидролазы – ферменты, ускоряющие реакции гидролитического распада;
· лиазы (синтазы) – ферменты, ускоряющие негидролитическое отщепление от субстратов определенных групп атомов с образованием двойной связи или присоединение групп атомов по двойной связи;
· изомеразы – ферменты, ускоряющие пространственные или структурные перестройки в пределах одной молекулы;
· лигазы (синтетазы) – ферменты, ускоряющие реакции синтеза, сопряженные с распадом макроэргов.
Ферменты используют в проведении многих технологических процессах. Ферменты используют в процессах приготовления пищи, в производстве вина, сыра, в фармацевтической промышленности, в производстве моющих средств, текстиля, кожи и бумаги. Например, фермент амилаза расщепляет крахмал, поэтому используется в пивоварении, фермент фицин используют как добавку к зубным пастам; фермент папаин используют в мясной промышленности для умягчения мяса; фермент пепсин используют в пищевой промышленности для получения каш готовых к употреблению; фермент трипсин используют для производства продуктов для детского питания; целлюлазы и пектиназы используют для осветления сока; каталаза используется для превращения латекса в губчатую резину; бактериальные протеазы используют для получения порошков с ферментными добавками, в кожевенной промышленности для отделения волос от шкуры и текстильной промышленности для извлечения шерсти из овечьих шкур.
Таким образом, ферменты – это природные биокатализаторы. Ферменты имеют большие значения относительных молекулярных масс. Ферменты обладают избирательностью и высокой эффективностью. Ферменты могут быть простыми и сложными. Ингибиры – это вещества, которые уменьшают скорость ферментативной реакции. Ферменты имеют большое значение в жизни человека, их используют во многих технологических процессах.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 8621
8621

