Альдегиды. Свойства. Получение и применение
Каждый из вас может представить себе запах гиацинтов. Этот аромат обусловлен наличием альдегида, который так и называют – гиацинтовый. А что же представляют собой альдегиды?

Альдегиды – это производные углеводородов, в молекулах которых атом водорода замещён на группу ― CHО. Эта группа называется альдегидной и для альдегидов она является функциональной, то есть определяет принадлежность к данному классу соединений.
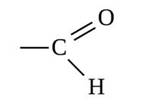
Общая формула альдегидов R – CHO, где R – углеводородный заместитель или атом водорода. Кроме этого, использую ещё и общую формулу CnH2nO, которая отражает молекулярный состав альдегидов, или такую формулу, как CnH2n+1CHO.
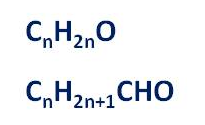
Первым представителем альдегидов является метаналь – HCHO или формальдегид, вторым альдегидом является этаналь – CH3 – CHO, или ацетальдегид, третьим представителем – пропаналь, или пропионовый альдегид – CH3 – CH2 – CHO.
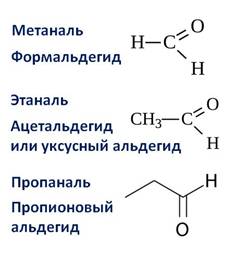
Названия альдегидов образуются от названий соответствующих алканов с добавлением суффикса –аль.

Метаналь при н.у. является бесцветным газом.
Альдегиды, у который от двух до двенадцати атомов углерода – жидкости, у которых больше атомов углерода – твёрдые вещества. Низшие альдегиды имеют резкий запах, у альдегидов, которые имеют от четырех до шести атомов углерода, неприятный запах, высшие альдегиды обладают цветочными запахами. Низшие альдегиды хорошо растворяются в воде. Сорока процентный раствор метаналя называют формалином. С увеличением молярной массы альдегидов их растворимость в воде уменьшается. Температуры кипения и плавления альдегидов с увеличением молярной массы возрастают.
Альдегиды – химически активные соединения, для которых характерны реакции присоединения по связи С=О и окисления по связи С–Н в альдегидной группе.
Например, при пропускании паров этаналя вместе с водородом над катализатором происходит присоединение водорода и образуется спирт этанол
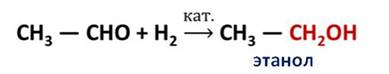
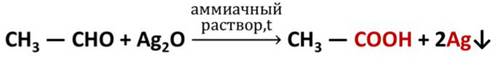
Если к аммиачному раствору оксида серебра (I) прилить раствор этаналя и смесь нагреть, то происходит окисление альдегида с образованием кислоты. Внутренняя поверхность пробирки, в которой нагревается смесь, покрывается при этом тонким слоем серебра. Это так называемая реакция «серебряного зеркала», которая может служить качественной реакцией на альдегиды.
Если приготовить гидроксид меди (II) смешением растворов гидроксида натрия и сульфата меди (II), а затем к этому свежеприготовленному осадку гидроксида меди (II) прилить раствор этаналя и смесь нагреть, то происходит окисление альдегида до кислоты, а гидроксид меди (II) превращается в оксид меди (I) красного цвета. Эта реакция также используется для качественного обнаружения альдегидов.
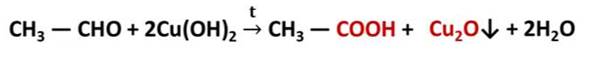
В лаборатории альдегиды получают окислением спиртов, в качестве окислителя используют оксид меди (II).
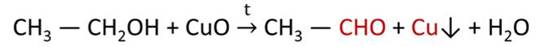
В промышленности метаналь получают окислением метанола кислородом воздуха в присутствии медного или серебряного катализатора:
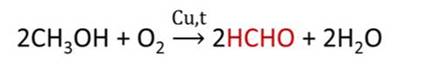
Этаналь был выделен в лаборатории немецким химиком Ю. Либихом в 1835 году, а метаналь был получен в лаборатории немецким химиком А. Гофманом в 1868 году.


Основное количество получаемого в промышленности метаналя расходуется на производство фенолформальдегидных смол и пластмасс, полиформальдегид используют для изготовления плёнок и волокон, метаналь применяют при производстве некоторых лекарственных веществ, в частности уротропина. Метаналь используется для получения формалина, который обладает сильными дезинфицирующими свойствами, поэтому его применяют для дезинфекции и дубления кож, хранения анатомических препаратов, в сельском хозяйстве – для протравливания семян. Этаналь используют в промышленных масштабах для получения уксусной кислоты и её производных.
Таким образом, альдегиды – производные углеводородов, у которых атом водорода замещён на альдегидную группу. Общая формула альдегидов – CnH2n+1CHO. Для альдегидов характерны реакции присоединения по двойной связи и окисления по связи С–Н в альдегидной группе. К основным промышленным способам получения альдегидов относят окисление спиртов. Метаналь и этаналь используют во многих отраслях производства.

 Получите свидетельство
Получите свидетельство Вход
Вход




 0
0 18267
18267

