Предельные одноосновные карбоновые кислоты.
Понятие о сложных эфирах
Карбоновые кислоты – это соединения, которые содержат карбоксильную группу – СООН. Эта группа является функциональной группой для карбоновых кислот. Общая формула предельных одноосновных карбоновых кислот R – COOH, где R — углеводородный радикал, а также можно использовать и другую общую формулу – CnH2n+1COOH, где n – число атомов углерода. Одноосновными они называются потому, что содержат одну карбоксильную группу – СООН, предельными, потому что связи между атомами углерода одинарные, то есть насыщены.
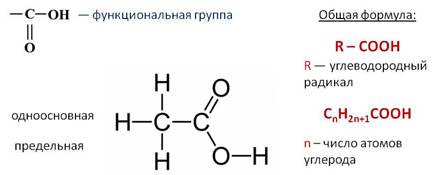
Предельные одноосновные карбоновые кислоты можно получить путём следующих превращений: предельный углеводород → непредельный углеводород → спирт → альдегид → кислота.

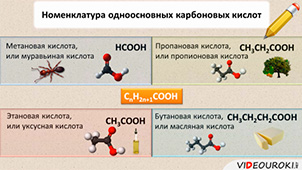
Первым представителем этого класса соединений является метановая кислота, или муравьиная – НСООН, вторым представителем – этановая кислота, или уксусная кислота – СН3СООН, третьим – пропановая, или пропионовая кислота – CH3CH2COOH, четвёртым представителем является бутановая, или масляная кислота – CH3CH2CH2COOH.
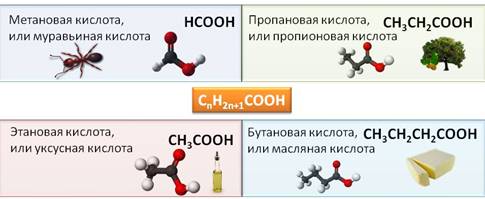
Карбоновые кислоты и их производные встречаются во многих природных объектах. Так, муравьиная кислота, или метановая – в выделениях муравьёв, изовалериановая – в корнях валерианы, бензойная – в бруснике, клюкве и чернике, щавелевая – в листьях щавеля, ревеня, малоновая – в соке сахарной свёклы, яблочная – в ягодах и фруктах, лимонная – в лимонном соке.

Чистая уксусная кислота представляет собой бесцветную жидкость с резким запахом. Смешивается с водой в любых соотношениях. Водный раствор с массовой долей уксусной кислоты 3-9% под названием уксус применяется как приправа к пище, а 70-80% кислота называется уксусной эссенцией. Безводная уксусная кислота при комнатной температуре представляет собой жидкость, при 17 0С она замерзает и превращается в льдистое вещество, которое называют ледяной уксусной кислотой.


По химическим свойствам уксусная кислота – типичная кислота. Поэтому она проявляет все свойства, характерные для неорганических кислот.
Уксусная кислота изменяет окраску индикаторов. Например, если мы нальём в пробирку уксусной кислоты и добавим несколько капель лакмуса, то раствор кислоты станет красного цвета. Таким образом, уксусная кислота в растворе диссоциирует с образованием иона водорода и аниона кислотного остатка – ацетат-иона.


Если к полученному раствору добавить раствор щёлочи – гидроксида натрия, то окраска станет фиолетового цвета. Таким образом, уксусная кислота вступает в реакции обмена со щелочами. В результате этой реакции образуется соль – ацетат натрия и вода.
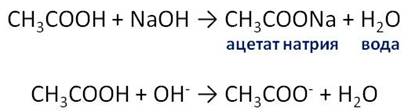
Уксусная кислота реагирует с активными металлами. Для того, чтобы в этом убедиться, в пробирку с уксусной кислотой добавим гранулу цинка. У нас появляются пузырьки газа. В результате этой реакции образуется соль – ацетат цинка и выделяется газ – водород.
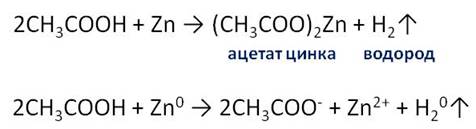
Кроме этого, уксусная кислота реагирует и с основными оксидами. Если мы в пробирку с раствором уксусной кислоты добавим оксид магния и содержимое слегка нагреем, то у нас постепенно оксид магния растворяется и образуется соль – ацетат магния.

Как и другие кислоты, уксусная кислота реагирует с солями слабых кислот – карбонатами. Например, если в пробирку с уксусной кислотой добавить соды, то происходит вскипание раствора, вследствие образования углекислого газа. Таким образом, уксусная кислота вытеснила угольную из соли. В результате реакции образовалась новая соль – ацетат натрия, углекислый газ и вода.
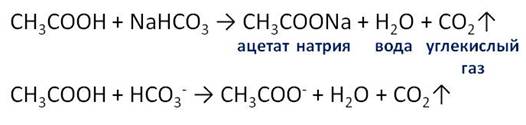
Уксусная кислота имеет и особое свойство: она реагирует со спиртами. Например, если в пробирку налить этилового спирта и столько же уксусной кислоты, добавить к этой смеси немного концентрированной серной кислоты и нагреть смесь, а затем вылить образовавшееся соединение в пробирку с водой, то полученное соединение собирается на поверхности воды. Таким образом, это соединение плохо растворяется в воде, но обладает приятным запахом.

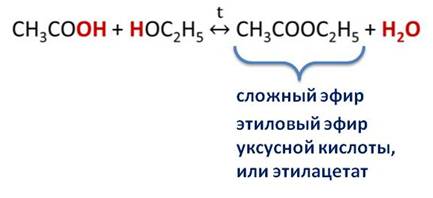
В результате реакции между уксусной кислотой и этиловым спиртом образовалось соединение, которое относится к классу сложных эфиров. Это этиловый эфир уксусной кислоты, или этилацетат. Причём в этой реакции, ОН группа отщепляется от кислоты, а водород от спирта. И образуется таким образом – вода. Эта реакция является обратимой.

Сложные эфиры способны к гидролизу в присутствии кислоты или щёлочи. Если нагреть смесь сложного эфира с разбавленной сильной кислотой, то происходит кислотный гидролиз. Например, при кислотном гидролизе этилового эфира уксусной кислоты образуется уксусная кислота и этиловый спирт.
CH3COOC2H5
+ H2O  СН3COOH
+ C2H5ОН
СН3COOH
+ C2H5ОН
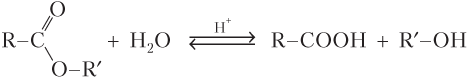
При щелочном гидролизе сложных эфиров образуется спирт и соль карбоновой кислоты. Этот гидролиз необратим. Например, при щелочном гидролизе этилацетата образуется ацетат натрия – соль уксусной кислоты и этиловый спирт.
CH3COOC2H5 + NaOH → СН3COONa + C2H5ОН
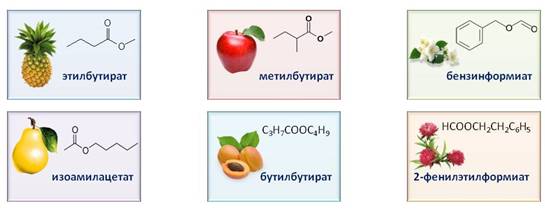
Сложные эфиры, в основном, представляют собой жидкости, обладающие приятным фруктовым вкусом. Многие сложные эфиры имеют запахи ананаса, груш, яблок, абрикос, жасмина, хризантем. Сложные эфиры находятся в ягодах, фруктах, цветах и придают им аромат.
Воски – это тоже сложные эфиры: пчелиный воск, ланолин из овечьей шерсти. Они плохо растворяются в воде, но хорошо растворимы в спиртах.

Благодаря приятному аромату некоторые сложные эфиры составляют основу эссенций для приготовления фруктовых вод, кондитерских изделий и духов. Сложные эфиры используют в лакокрасочной промышленности, в производстве искусственных волокон и некоторых полимерных материалов, они применяются как растворители органических веществ, при проведении химических реакций.

Реакцию между органической кислотой и спиртом называют реакцией этерификации, в результате этих реакций образуются сложные эфиры.
Уксусную кислоту применяют при синтезах полимеров, красителей (индиго), лекарств (аспирина), при консервировании, для получения искусственного волокна – ацетатного шёлка, киноплёнки, душистых веществ в парфюмерии и косметике, гербицидов, её применяют для получения фруктовых эссенций.

Таким образом, насыщенные одноосновные карбоновые кислоты – это производные углеводородов, в молекулах которых один атом водорода замещён на карбоксильную группу – СООН. Общая формула этих кислот CnH2n+1COOH. Уксусная кислота – представитель насыщенных одноосновных карбоновых кислот. Она проявляет свойства, характерные для большинства кислот: реагирует с активными металлами, основными оксидами, основаниями и солями слабых кислот. Для карбоновых кислот характерны реакции этерификации. Реакции этерификации – это реакции между карбоновой кислотой и спиртом, в результате которых образуются сложные эфиры. Сложные эфиры широко распространены в природе. Сложные эфиры гидролизуются растворами минеральных кислот и щелочей. Карбоновые кислоты и сложные эфиры имеют большое значение в различных областях промышленности.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 24499
24499

