Ароматические углеводороды на примере бензола
Физик Фарадэй в 1825 году выделил из светильного газа неизвестную жидкость, замерзающую при температуре 50С, кипящую при температуре 500С. Он установил, что это вещество состоит из атомов углерода и водорода и назвал его карбюрированным углеродом.

Химик Черлих получил это вещество из бензойной кислоты и установил его формулу. А химик Либих дал название этому веществу – бензол.

Бензол представляет собой особую группу веществ, принадлежащих к ароматическим углеводородам.
Структурная формула простейшего представителя ароматических углеводородов – бензола – была впервые предложена немецким химиком Кекуле. Кекуле является также одним из создателей теории химического строения органических соединений. Название «ароматические» эти соединения получили потому, что впервые выделенные из природных смесей ароматические соединения имели характерный приятный запах (от греческого арома – запах).

Молекулярная формула бензола С6Н6. На шесть атомов углерода в молекуле бензола приходится только шесть атомов водорода. Эти С – С связи в молекуле бензола ненасыщенные. Однако доказано, что бензол в обычных условиях не вступает в реакции присоединения, характерные для ненасыщенных углеводородов.

Получаются противоречия между структурной формулой бензола с двойными связями и его химическими свойствами. Поэтому молекула бензола изображается различными способами.
При изображении структурных формул бензола не всегда указываются атомы углерода или атомы углерода и водорода. Могут быть показаны три двойные связи внутри цикла или просто рисуют круг.
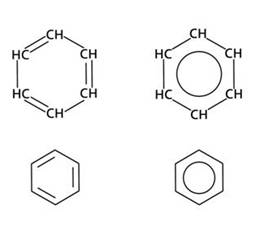
Доказано, что молекула бензола имеет плоскостное строение – все двенадцать атомов молекулы расположены в одной плоскости. Общая формула ароматических углеводородов – CnH2n-6.
Бензол – прозрачная жидкость с характерным запахом. Относится к очень ядовитым соединениям, обладающим канцерогенными свойствами.
В отличие от ненасыщенных соединений, для которых характерны реакции присоединения, для бензола характерны реакции замещения. Например, бензол вступает в химическую реакцию с бромом (или хлором) в присутствии катализатора.
В реакции с хлором один из атомов водорода в молекуле бензола замещается на атом хлора с образованием другого ароматического соединения – хлорбензола.
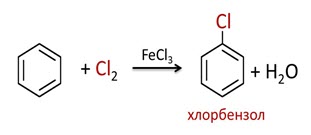
В присутствии нитрирующей смеси (азотной и концентрированной серной кислоты) в бензоле также замещается атом водорода на нитрогруппу и образуется нитробензол.
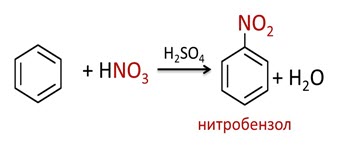
Менее характерны для бензола реакции присоединения. Например, в реакции присоединения три моль водорода к бензолу образуется циклогексан.
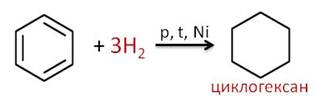
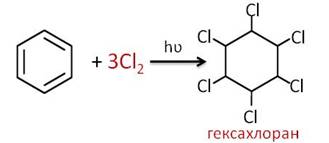
При присоединении три моль хлора к бензолу в присутствии света образуется гексахлоран.
Бензол, как и все углеводороды горит с образованием углекислого газа и воды.
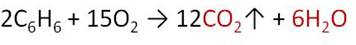
Бензол и его гомологи широко используются в промышленности для синтеза красителей, взрывчатых и душистых веществ, для получение пластмассы, фенола, их используют как растворители.

Ароматические соединения присутствуют и в пережаренном цыплёнке, табачном дыму, печной саже и выхлопных газах дизельных двигателей. Это такие соединения, как пирен и бензопирен, которые так же, как и бензол, обладают канцерогенными свойствами.

Главными источниками получения насыщенных, ненасыщенных и ароматических углеводородов являются природный газ и нефть.

Природный газ используют как топливо в металлургии и других отраслях промышленности; как сырьё в химической промышленности при получении водорода, этилена, ацетилена, сажи. Эти вещества используют при получении синтетических каучуков, полимеров, спиртов, медикаментов.
Нефть – маслянистая жидкость тёмно-бурого или почти чёрного цвета с характерным запахом, легче воды и практически в ней нерастворима.

Нефть начали использовать около 5 тыс. лет назад на Ближнем Востоке, где она по трещинам в горных породах просачивалась на поверхность. Название нефти происходит от слова напатум, которое на одном из древних языков Междуречья означало «вспыхивать, воспламеняться».

Нефть представляет собой в основном смесь ненасыщенных и циклических углеводородов, содержащих от 50 и выше атомов углерода в составе молекул.
Нефть является продуктом, образовавшимся в результате биологических и химических изменений растительных и животных остатков в течении миллионов лет. Сложный состав нефти можно наблюдать при перегонке.
Так как нефть является смесью веществ, она не имеет определённой температуры кипения, а перегоняется в широком интервале температур. Существует определённая закономерность: чем больше молекулярная масса углеводорода, тем выше его температура кипения. Это и используют на нефтеперегонных заводах: нефть перегонкой разделяют на отдельные части, или фракции – смеси различных веществ, имеющих близкие температуры кипения. Отдельные фракции различаются составом и интервалом температур перегонки. Первая фракция – газ – содержит метан, этан, пропан и два изомера бутана. Другая фракция – бензин – её применяют в автомобильных двигателях, керосин – в тракторных и авиационных двигателях, а газойль – в дизельных двигателях. Остаток после перегонки нефти – мазут – также разделяют на фракции: соляровые масла, смазочные масла, вазелин и парафин. Оставшийся после этого гудрон применяют в производстве асфальта.


Преобладающее количество добываемых углеводородов используется в качестве топлива: для обогрева жилищ и приготовления пищи, для тепловых электростанций и в двигателях внутреннего сгорания.

Основная химическая реакция, происходящая в двигателях, заключается в сгорании смеси углеводородов с кислородом воздуха и выделении большого количества теплоты.
При этом в выхлопные газы попадают продукты сгорания смеси углеводородов: углекислый газ и вода. При неполном сгорании углеводородов образуется токсичный угарный газ. По этой причине автомобиль с работающим двигателем должен находиться в хорошо проветриваемом помещении.


Для улучшения качества бензиновых фракций, получаемых при простой перегонке нефти, к ним иногда добавляют определённое количество тэтраэтилсвинца (этилированный бензин чрезвычайно ядовит). При сгорании этилированного бензина наряду с выхлопными газами, содержащими углекислый газ, воду и угарный газ, выделяется большое количество соединений свинца, оседающих на траве и деревьях вдоль магистралей.
В настоящее время основная масса применяемого бензина не содержит тэтраэтилсвинца. В бензин добавляют другие, менее токсичные вещества.

Другим побочным эффектом использования бензиновых двигателей, кроме токсичности отработанных газов, является выделение большого количества оксида углерода (IV). Оказалось, что этот оксид, метан и галогеналканы могут поглощать инфракрасное излучение земли, превращая его в теплоту, что приводит к так называемому парниковому эффекту, то есть повышению температуры нашей планеты.

Каменный уголь – тоже источник энергии и химического сырья. Одним из основных способов переработки каменного угля является коксование (сухая перегонка или пиролиз). При коксовании уголь нагревают от 1000 до 12000С без доступа воздуха и получают кокс, который используют в металлургии, коксовый газ, который содержит водород, метан и другие газы используют в качестве топлива и химического сырья.

Таким образом, бензол – простейший представитель ароматических углеводородов, общая формула которых CnH2n-6.. Для бензола характерно плоскостное строение. Характерными химическими свойствами бензола являются реакции замещения. Основными продуктами переработки нефти являются бензин, керосин и дизельное топливо. Парниковый эффект обусловлен накоплением в атмосфере оксида углерода (IV), метана и галогеналканов.

 Получите свидетельство
Получите свидетельство Вход
Вход




 0
0 4008
4008

