Алкины относятся к ненасыщенным углеводородам. Они представляют собой углеводороды, содержащие в составе молекул тройную связь.
Общая формула алкинов – CnH2n-2. Если в эту формулу подставить значения относительных атомных масс, то относительная молекулярная масса алкинов будет 14n-2.
Орбитали атомов углерода, между которыми образована тройная связь, находятся в состоянии sp-гибридизации. Тройная углерод-углеродная связь, длина которой 0,12 нм, короче двойной. Энергия тройной связи больше, то есть она является более прочной. Таким образом, молекула ацетилена имеет линейное строение и валентный угол связей 1800. Для всех остальных алкинов на одной прямой лежат только те атомы, которые непосредственно примыкают к атомам С, образовавшим тройную связь.
Названия алкинов образуются с заменой суффикса-ан в названии соответствующего насыщенного углеводорода на суффикс -ин. При составлении названия алкина выбирается самая длинная цепь, включающая тройную связь; нумерация атомов С в главной цепи проводится так, чтобы атом С, от которого начинается тройная связь, получил наименьший номер. Если тройная связь находится на одинаковом расстоянии от концов цепи, нумерацию ведут с того конца, к которому ближе находится заместитель. Заместители перечисляются в алфавитном порядке. В конце названия указывается номер атома С, от которого отходит тройная связь.
Назовём следующий алкин.
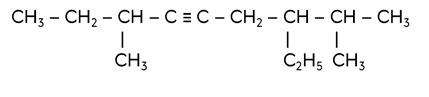
Нумерация начинаем слева направо. В главной цепи находится 9 атомов углерода. От 3 и 8иатома углерода отходят метильные радикалы, от 7 отходит радикал этил, а тройная связь от 4 атома углерода. Получается название 3,8-диметил-7-этилнонин-4.
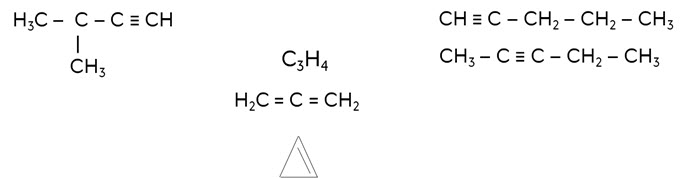
Для алкинов характерны все виды структурной изомерии: изомерия углеродного скелета, изомерия положения тройной связи и межклассовая с циклоалкенами и диенами. Например алкина с молекулярной формулой С3Н4 имеет 2 межклассовых изомера: пропадиен и циклопропен. У алкена с молекулярной формулой С5Н8 изомерами будут 3-метилбутин-1, пентин-1 и пентин-2.
Ацетилен, припин, бутин-1 – это газы, бутин-2 и до С16 – жидкости, выше С17 – твёрдые вещества. Алкины плохо растворимы в воде, но хорошо растворимы в органических растворителях. При увеличении относительной молекулярной массы алкинов идёт увеличение температуры кипения.
Для алкинов характерны реакции присоединения. Это реакции электрофильного присоединения. Они присоединяют галогены. Присоединение идёт в две стадии: сначала разрывается одна π-связь, затем на второй стадии – другая. Так, ацетилен обесцвечивает раствор брома в тетрахлорметане. На первой стадии присоединения образуется 1,2-дибромэтен, на второй – 1,1,2,2-тетрабромэтан.
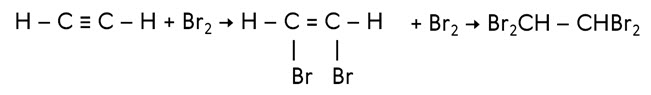
Присоединение водорода – реакция гидрирования идёт при нагревании и в присутствии катализатора. При присоединении водорода к этину, на первой стадии образуется этен, на второй – этан.
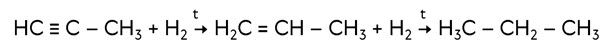
Присоединение воды к ацетилену идёт в кислой среде и в присутствии катализатора – соли ртути. Эта реакция называется ещё реакцией Кучерова.
В результате реакции гидратации ацетилена образуется неустойчивый виниловый спирт, который затем переходит в уксусный альдегид.
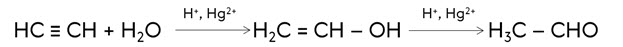
В случае алкинов с более длинной цепью в результате реакции образуются кетоны. Так, в реакции гидратации пропина образуется кетон – ацетон.
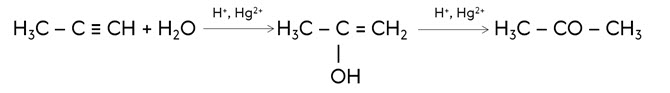
Для алкинов характерны реакции присоединения галогеноводородов. Реакция присоединения галогеноводорода также идёт в две стадии, причём на обеих стадиях выполняется правило Марковникова.
Так, в реакции этина с хлороводородом образуется сначала винилхлорид, затем 1,1-дихлорэтан:
HC ≡ CH + HCl → H2C = CHCl + HCl → H3C – CHCl2.
При
пропускании ацетилена над активированным углём при 500 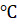 происходит
образование бензола.
происходит
образование бензола.
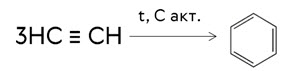
Помимо тримеризации ацетилена, возможна его димеризация. Под действием солей меди (I) образуется винилацетилен.
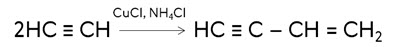
При полном окислении – горении ацетилена образуется углекислый газ и вода:
2C2H2 + 5O2 → 4CO2↑ + 2H2O.
На воздухе ацетилен горит коптящим пламенем, так как содержание углерода в его молекуле выше, чем в молекулах этана и этена.
В промышленности ацетилен получают нагреванием метана. А также окислительным пиролизом метана. Помимо ацетилена в качестве продуктов реакции образуется оксид углерода (II) и водород, которые могут быть использованы для синтеза спиртов или синтетического бензин:
2CH4 → HC ≡ CH + 3H↑
6CH4 + O2 → 2C2H2 + 2CO↑ + 10H2↑.
В лаборатории ацетилен получают обработкой карбида кальция с водой.
Сам карбид кальция получают сплавлением оксида кальция и угля в электропечах. А оксид кальция образуется при обжиге (термическом разложении) карбоната кальция:
CaC2 + 2H2O = Ca(OH)2 + HC ≡ CH
CaO + 3C = CaC2 + CO.
При воздействии на дибромпроизводное, в котором атомы галогенов находятся при соседних атомах углерода (или при одном и том же атоме), спиртового раствора щёлочи происходит отщепление двух молекул галогеноводорода (дегидрогалогенирование) и образование тройной связи. Так, в результате взаимодействия спиртового раствора щелочи на 1,2-дибромэтан или 1,1-дибромэтан образуется ацетилен:
CH2Br – CH2Br + 2KOH → CH ≡ CH + 2KBr + 2H2O.
Кроме того, алкины, в частности ацетилен, можно получить в результате взаимодействия 1,1,2,2-тетрабромэтана с цинком:
HCBr2 – CHBr2 + 2Zn → HC ≡ CH + 2ZnBr2.
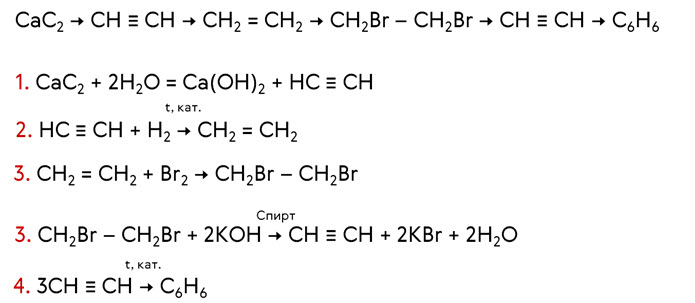
Осуществим следующие превращения: из карбида кальция следует получить ацетилен, из ацетилена получить 1,2-дибромэтан, из 1,2-дибромэтана надо получить ацетилен и из ацетилена – бензол. Для того чтобы из карбида кальция получить ацетилен, следует к карбиду кальция добавить воду. Для получения этилена проводим реакцию гидрирования. Затем к этилену присоединяем бром, получается 1,2-дибромэтан. К 1,2-дибромэтану следует добавить спиртовой раствор щёлочи, получается ацетилен. Тримеризацией ацетилена в последней реакции можно получить бензол.

 Получите свидетельство
Получите свидетельство Вход
Вход




 891
891

