Ароматические углеводороды являются циклическими соединениями, обладают свойствами непохожими на свойства ненасыщенных соединений.
Ароматические соединения – это органические соединения, которые в составе содержат бензольные кольца.
Изначально, ароматичекими соединениями была группа веществ, которая обладала приятным запахом. Однако в настоящее время понятие «ароматичность» имеет другой смысл.
Гомологический ряд ароматических углеводородов имеет общую формулу CnH2n-6.
К наиболее важным ароматическим соединениям относятся бензол – С6Н6 и его гомологи, такие, как: толуол С6Н5СН3, ксилол С6Н4(СН3)2 и другие.
Структурную формулу бензола можно изобразить несколькими способами: в первом случае мы видим наличие трёх двойных связей, во втором – наличие бензольного кольца.

Первую структурную формулу предложил немецкий учёный Ф. Кекуле.
Ф. Кекуле – немецкий химик, он внёс большой вклад в развитие учения о валентности, теорию строения органических молекул.

В 1865 году он высказал предположение, что молекула бензола имеет форму правильного шестиугольника, образованного шестью атомами углерода, с которыми связаны шесть атомов водорода. В этом шестиугольнике чередуются простые и двойные связи.

Запись
структурной формулы, предложенной Кекуле, подтверждают и экспериментальные
данные. Действительно, все атомы водорода и углерода в молекуле бензола лежат в
одной плоскости, угол связи между атомами 120 ,
как у алкенов, для гидрирования бензола нужно 3 моль водорода, как для
гидрирования трёх двойных связей.
,
как у алкенов, для гидрирования бензола нужно 3 моль водорода, как для
гидрирования трёх двойных связей.
Как видно из структурной формулы, двойные связи чередуются с одинарными. Такое расположение связей вызывает образование единого электронного облака, которое охватывает все шесть атомов углерода.
Экспериментально доказано, что в молекуле бензола нет двойных и одинарных связей, длины всех С – С-связей раны 0,140 нм. Каждый атом углерода в молекуле бензола находится в состоянии sp2-гибридизации, он связан с двумя соседними атомами углерода и одним атомом водорода σ-связями. Поэтому молекула бензола имеет вид плоского шестиугольника, где все атомы лежат в одной плоскости. Электронное облако четвёртого р-электрона, который не участвует в гибридизации, ориентировано перпендикулярно к плоскости бензольного кольца. Такие 6 р-электронов перекрываются над и под плоскостью кольца, образуя общее электронное облако и единую химическую связь для всех атомов углерода. Две области электронной плоскости расположены по обе стороны от σ-связей.
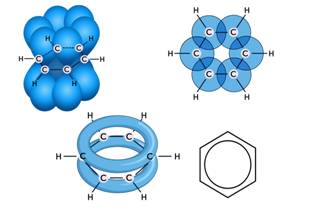
Поэтому формула бензола с окружностью символизирует равноценность связей между атомами углерода.
Рассмотрим номенклатуру аренов. Для названия этого класса соединений часто используют тривиальные названия. Например, бензол, толуол, стирол, кумол и другие. По международной заместительной номенклатуре арены рассматривают как производные бензола, где положение заместителей указывается цифрами, при чём номера атомов углерода, от которых отходят заместители, должны получить наименьшие номера.
Назовём следующие арены: первый арен называется метилбензол, или толуол, второй арен называется этилбензол, третий называется изопропилбензол, или кумол.

Рассмотрим арены, содержащие заместители с кратными связями: первый арен называется винилбензол, или стирол, второй – этинилбензол, или фенилацетилен.

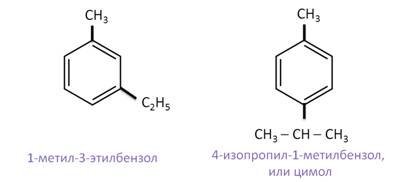
Если в аренах два одинаковых заместителя, то вместо цифр можно использовать приставки: положение 1,2 называется «орто», положение 1,3 – «мета», а положение 1,4 – «пара». Поэтому следующие гомологи бензола можно назвать так:

Если в аренах два различных заместителя, то нумерацию определяет младший заместитель.
Рассмотрим более сложные примеры, где арен содержит три заместителя. Первый арен называется 1,2,3-триметилбензол, второй – 1,2,4-триметилбензол, а третий – 1,3,5-триметилбензол.

Для аренов характерна изомерия, связанная со строением радикалов, их составом и положением.
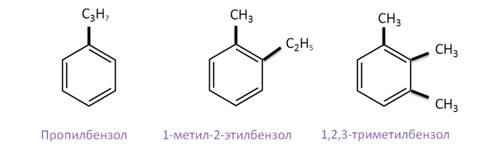
Рассмотрим изомерию, связанную со строением боковых цепей. Так, изомерами между собой являются пропилбензол, или кумол, и изопропилбензол.

Если это изомерия, связанная с числом атомов углерода в заместителях, то изомерами между собой будут пропилбензол, 1-метил-2-этилбензол и 1,2,3-триметилбензол, которые содержат в сумме по 3 атома углерода в заместителях.
Рассмотрим изомерию, связанную с положением заместителей в цикле. Такими изомерами между собой будут 1,2-диметилбензол, 1,3-диметилбензол и 1,4-диметилбензол.

Таким образом, общая формула аренов CnH2n-6, все атомы молекулы бензола лежат в одной плоскости, и длины всех С – С-связей равны 0,140 нм. Для аренов характерна изомерия, связанная со строением радикалов, их составом и положением.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 13909
13909

