Алкены – это углеводороды, которые содержат в составе молекул одну двойную С = С-связь.
Алкены называют ещё этиленовыми углеводородами, это исторически сложившееся название, потому что первым представителем алкенов является этилен. Ещё алхимики называли алкены олефинами (от лат. olefiant – «масло», так как при их гидрировании образовывались маслоподобные вещества). Но это название до сих пор широко используется в химической литературе.
Алкены довольно широко распространены в природе. Например, этилен является фитогормоном, который ускоряет созревание плодов. Насекомые выделяют феромоны, которые также являются алкенами. Натуральные экстракты растений содержат алкены в качестве основного компонента. В небольшом количестве этилен содержится в природном газе и в попутных газах.
Рассморим ещё 2 представителя алкенов. Это (R) – лимонен и альфа-пинен. Название (R) – лимонен говорит о том, что это алкен и здесь есть двойная связь. Это вещество пахнет апельсинами и придаёт апельсинам их запах. Другое вещество – альфа-пинен – тоже алкен и является основным компонентом скипидара, который используют как растворитель для масляных красок. Некоторые думают, что у скипидара неприятный запах, но это не так.

Первым представителем алкенов является этен, или этилен. Вторым алкеном является пропен, или пропилен, третьим – бутен, четвёртым – пентен. Эти углеводороды образуют гомологический ряд, в котором каждый последующий член ряда отличается на одну или несколько групп – СН2.
Алкены содержат в своей молекуле меньшее число водородных атомов, чем соответствующие им алканы (с тем же числом углеродных атомов), поэтому такие углеводороды называют непредельными или ненасыщенными. Поэтому, состав этих углеводородов выражается общей формулой CnH2n. Буква n, как и в случае алканов, показывает число атомов углерода, которое входит в состав углеводорода.
Если рассмотреть строение алкенов, то можно увидеть двойную связь между атомами углерода. При образовании этой двойной связи обобществляются две пары электронов от соседних атомов углерода. Одна пара электронов образует σ-связь, другая связь – π-связь – образуется за счёт перекрывания р-облаков по обе стороны от оси, которая соединяет центры атомов.
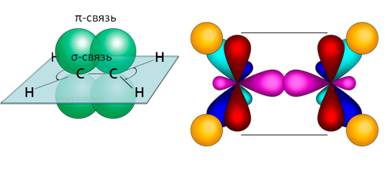
По своей природе π-связь резко отличается от σ-связи: π-связь менее прочная вследствие перекрывания электронных облаков вне плоскости молекулы. Под действием реагентов π-связь легко разрывается.
Установлено, что молекула этилена имеет плоскостное строение, валентные углы связей равны 120 °. Длина С = С-связи равна 0,134 нм. Такое плоскостное строение двойной связи характерно и для других алкенов. Молекула этилена симметрична; ядра всех атомов расположены в одной плоскости и валентные углы близки к 120°; расстояние между центрами атомов C равно 0,134 нм. У алкенов отсутствует вращение относительно двойной углерод-углеродной связи.

Название алкенов образуется с заменой суффикса -ан в названии соответствующего насыщенного углеводорода на суффикс -ен. Так, название этан заменяется на этен, а пропан – на пропен. Если в составе алкена более трёх атомов углерода, то в названии обязательно указывается положение двойной связи. Например, алкен, содержащий четыре атома углерода называется бутен, но в конце следует указать цифрой положение двойной связи. В первом случае двойная связь отходит от первого атома углерода, поэтому этот алкен называется бутен-1, у второго алкена двойная связь отходит от второго атома углерода, поэтому он называется бутен-2.
CH2 = CH – CH2 – CH3
CH3 – CH = CH – CH3
Нумерацию углеродной цепи у алкенов определяет двойная связь, при этом атом углерода около двойной связи должен получить наименьший номер.
Например, CCl3 – CH2 – CH = CH – CH3 называется 5,5,5-трихлорпентен-2, но не 1,1,1-трихлорпентен-3. Ещё одно правило: главная цепь должна содержать двойную связь, хотя может быть и не самой длинной. Например, данный углеводород называется 2-этилгексен-2, но не 3-метилгептен-3.
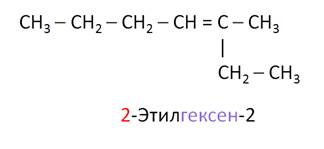
Таким образом, при названии алкенов в качестве главной цепи нужно выбрать самую длинную углеродную цепь, которая содержит двойную связь и наибольшее число заместителей. Атомы углерода нумеруют с того конца, где ближе двойная связь. После этого указывают цифрами атомы углерода, от которого отходят заместители. Далее записывают название углеводорода, заменяя суффикс -ан на -ен. В конце названия указывают атом углерода, от которого отходит двойная связь.
Назовём следующий углеводород.

Выбираем самую длинную цепь, которая содержит двойную связь и наибольшее число заместителей. В нашем случае два заместителя: метил и этил. В главной цепи 6 атомов углерода, значит, алкен называется гексен и от третьего атома углерода отходит двойная связь, значит название будет 4-метил-3-этилгексен-3.
Непредельные (алкеновые) радикалы называют тривиальными названиями или по систематической номенклатуре. Так, радикал с двумя атомами углерода и двойной связью между ними называется винил, или этенил, с тремя атомами углерода и двойной связью – аллил.
Н2С = СН –
Н2С = СН – СН2 –
Для алкенов характерно несколько видов структурной изомерии: изомерия углеродного скелета и изомерия положения двойной связи. Изомерия положения двойной связи начинается с бутена. Так, для бутена характерна изомерия углеродного скелета. Его изомером в данном случае будет 2-метилпропен. Если рассмотреть изомерию положения двойной связи, то для бутена будет характерно два изомера: бутен-1 и бутен-2.
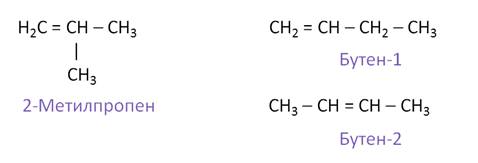
Кроме того, для алкенов характерна ещё и межклассовая изомерия с циклоалканами. Так, межклассовым изомером бутена будет циклобутан, который имеет такую же молекулярную формулу С4Н8.

Для алкенов характерна ещё и пространственная изомерия – стереоизомерия. Пространственные изомеры имеют только те алкены, которые содержат разные атомы или группы атомов у каждого атома углерода при двойной связи.
Сравним два алкена. У первого алкена у одного атома углерода при двойной связи разные атомы: Н и Cl, у второго атома углерода тоже разные. У второго же алкена при двойной связи у первого атома углерода два одинаковых атома, у второго – два разных. Потому первый алкен имеет пространственные изомеры, а второй – нет.
HCCl = CHCl
HCH = CH – CH3
Тоже самое можно проследить у бутена. Так бутен-1 не имеет пространственных изомеров, а бутен-2 имеет пространственные изомеры. Этими пространственными изомерами будут цис-бутен-2 и транс-бутен-2. В цис-изомере одинаковые заместители находятся по одну сторону плоскости двойной связи, а в транс-изомере – по разные стороны. От латинского cis – «на одной строне», trans – «через», «на другой».

Если рассмотреть физические свойства алкенов, то можно заметить, что температура кипения и плавления алкенов увеличивается с увеличением относительной молекулярной массы. Этен, пропен и бутен – газы, алкены, содержащие от С5 – С17 – жидкости, алкены, содержащие 18 и более атомов углерода – твёрдые вещества. Алкены не растворяются в воде, они легче воды, алкены растворимы в органических растворителях (бензин, бензол и другие.)
Так, этилен (этен) – бесцветный газ с очень слабым сладковатым запахом, немного легче воздуха, малорастворим в воде.
Таким образом, общая формула алкенов CnH2n. Алкены содержат одну С = С-связь. Двойная связь образована σ-связью и π-связью. Молекула этилена имеет плоскостное строение. Название алкенов образуется с заменой суффикса -ан на суффикс -ен. Для алкенов характерна структурная и пространственная изомерия.

 Получите свидетельство
Получите свидетельство Вход
Вход



 0
0 13078
13078

