Органические качественные реакции
1. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества между собой.
ВЕЩЕСТВА РЕАКТИВ
А) пропанон и пропанол-2 1) HCl(р-р)
Б) анилин и триэтиламин 2) Ag2O (NH3 р-р)
В) пентин-2 и этилацетат 3) Br2(водн.)
Г) бензол и гексен-2 4) K
5) HNO3
2. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества между собой. ВЕЩЕСТВА РЕАКТИВ
А) этанол и этиленгликоль 1) натрий
Б) муравьиная к. и уксусная к. 2) гидроксид натрия
В) бутан и бутен-2 3) гидроксид меди II
Г) бензол и толуол 4) перманганат калия
5) фенолфталеин
3. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции.
ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ
А) пропанол-1 и калий 1) выпадение белого осадка
Б) муравьиная к. и аммиачный р-р оксида серебра при нагревании 2) выпадение красного осадка
В) пропин и аммиачный р-р оксида серебра при нагревании 3) выпадение серебра в осадок
Г) ацетальдегид и гидроксид меди II при нагревании 4) выделение газа
5) образование ярко синего раствора
4. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции.
ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ
А) фенол и бромная вода 1) появление фиолетового окрашивания
Б) этен и бромная вода 2) появление жёлтого окрашивания
В) этиленгликоль и гидроксид меди II 3) обесцвечивание раствора и выпадение белого осадка
Г) белок и азотная кислота 4) обесцвечивание раствора
5) образование раствора ярко синего цвета
5. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти
вещества между собой.
ВЕЩЕСТВА РЕАКТИВ
А-Бензол и гексен 1-Бромная вода
Б-Бутин–1 и бутин–2 2-Фенолфталеин
В-Глюкоза и сорбит 3-Соляная кислота
Г-Пропионовая кислота и пропанол 4-Раствор карбоната натрия
5-Аммиачный раствор оксида серебра
6. Установить соответствие между признаками качественной химической реакции и веществами,
которые дают эту реакцию.
Признаки реакции Вещества
А-Исчезновение окраски раствора и выпадение белого осадка 1-Водный раствор КМnO4 и этилен
Б-Исчезновение окраски раствора и выпадение бурого осадка 2-Фенол и бромная вода
В-Обесцвечивание раствора без выпадения осадка 3-Раствор лакмуса и уксусная кислота
Г-Образование раствора с интенсивной синей окраской 4-Пропен и бромная вода
5-Этиленгликоль и гидроксид меди(II)
7. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества между собой.
ВЕЩЕСТВА РЕАКТИВ
А-Бензол и толуол 1-Лакмус
Б-Ацетилен и этилен 2-Бромная вода
В-Глюкоза и фруктоза 3-Соляная кислота
Г-Растворы фенола и пропанола 4-Аммиачный раствор оксида серебра
5-Подкисленный раствор перманганата калия
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
| Вещество, функциональная группа | Реактив | Схема реакции | Характерные признаки |
| Непредельные углеводороды (алкены, алкины, диены), кратные связи | р-р KMnO4 (розовый) | СН2=СН2 + Н2О + КMnO4 → КОН + MnO2↓+ СН2(ОН)-СН2(ОН) | обесцвечивание р-ра |
| р-р I2 (бурый) | СН2=СН-CН3 + I2 → СН2(I)-СН(I)-CH3 | обесцвечивание р-ра | |
| р-р Br2 желтый | СН2=СН2 + Br2 → СН2(Br)-СН2(Br) | обесцвечивание р-ра | |
| Ацетилен | аммиачный р-р Ag2O | СН≡СН + [Ag(NH3)2]OH → AgC≡CAg↓ + NH3↑ + H2O | осадок желтого цвета (взрывоопасен) |
| Бензол | нитрующая смесь HNO3 + H2SO4 | t0C, H2SO4(конц.) C6Н6 + HNO3 → C6H5-NO2 + H2O | образование тяжелой жидкости светло-желтого цвета с запахом горького миндаля |
| Толуол | р-р KMnO4 (розовый) | C6Н5-СН3 + KMnO4 + H2SO4 → C6H5-COOH + H2O + K2SO4 + MnSO4 | обесцвечивание р-ра |
| Фенол (карболовая кислота) | р-р FeCl3(светло-желтый) | C6H5OH + FeCl3 → (C6H5O)3Fe + HCl | окрашивание р-ра в фиолетовый цвет |
| р-р Br2 (бромная вода) | C6H5OH + Br2 → C6H2Br3OH↓ + HBr | образование белого осадка со специфическим запахом | |
| Анилин (аминобензол) | р-р хлорной извести CaOCl2 (бесцветный) |
| окрашивание р-ра в фиолетовый цвет |
| Этанол | насыщенный р-р I2 + р-р NaOH | C2H5OH + I2 + NaOH → CHI3↓ + HCOONa + NaI + H2O | мелкокристаллический осадка СНI3 светло-желтого цвета со специфическим запахом |
| CuO (прокаленная медная проволока) | t0C C2H5OH + CuO → Cu↓ + CH3-CHO + H2O | выделение металлической меди, специфический запах ацетальдегида | |
| Гидроксогруппа (спирты, фенол) | Металлический Na | R-OH + Na → R-O-Na+ + H2↑ C6H5-OH + Na → C6H5-O-Na+ + H2↑ | выделение пузырьков газа (Н2) |
| Эфиры (простые и сложные) | Н2О (гидролиз) в присутствии NaOH при нагревании | CH3-C(O)-O-C2H5 + H2O ↔ CH3COOH + C2H5OH | специфический запах |
| Многоатомные спирты, глюкоза | Свежеосаж-денный гидроксид меди (II) в сильно щелочной среде | CH2(OH)-CH(OH)-CH2(OH) + Cu(OH)2 → H2O + CH2-CH- CH2-OH | | O O \ | Cu | ярко-синее окрашивание р-ра |
| Карбонильная группа – СНО (альдегиды, глюкоза) | Аммиачный р-р Ag2O | t0C R-CHO + [Ag(NH3)2]OH → R-COOH + Ag↓ + NH3↑ + H2O | образование блестящего налета Ag («серебряное зеркало») на стенках сосудов |
| Свежеосаж-денный Сu(OH)2 | t0C R-CHO + Cu(OH)2 → R-COOH + Cu2O↓ + H2O | образование красного осадка Сu2O | |
| Карбоновые кислоты | лакмус |
| окрашивание р-ра в розовый цвет |
| р-р Na2CO3 | R-COOH + Na2CO3 → R-COO-Na+ + H2O + CO2↑ | выделение СО2 | |
| спирт + H2SO4 (КОНЦ.) | t0C R-COOH + HO-R1 ↔ RC(O)OR1 + H2O | специфический запах образующегося сложного эфира | |
| Муравьиная кислота | лакмус |
| окрашивание р-ра в розовый цвет |
| Свежеосаж-денный Сu(OH)2 | t0C HCOOH + Cu(OH)2 → Cu2O↓ + H2O + CO2↑ | образование красного осадка Сu2O | |
| аммиачный р-р Ag2O | t0C HCOOH + [Ag(NH3)2]OH → Ag↓ + H2O + CO2↑ | «серебряное зеркало» на стенках сосуда | |
| Олеиновая кислота | р-р KMnO4 (розовый) или I2 (бурый) или Br2 (желтый) | C17H33COOH + KMnO4 + H2O → C8H17-CH(OH)-CH(OH)-(CH2)7-COOH + MnO2↓ + KOH
C17H33COOH + I2 → C8H17-CH(I)-CH(I)-(CH2)7-COOH | обесцвечивание р-ра |
| Ацетаты (соли уксусной кислоты) | р-р FeCl3 | CH3COONa + FeCl3 → (CH3COO)3Fe + NaCl | окрашивание р-ра в красно-бурый цвет |
| Стеарат натрия (мыло) | Н2О (гидролиз) + фенолфта-леин | C17H35COONa + H2O ↔ C17H35COOH↓ + NaOH | окрашивание р-ра в малиновый цвет |
| насыщенный р-р соли кальция | C17H35COONa + Ca2+ ↔ (C17H35COO)2Ca↓ + Na+ | образование серого осадка | |
| Концентрир. неорганичес-кая кислота | C17H35COONa + H+ ↔ C17H35COOH↓ + Na+ | образование белого осадка | |
| Белок | пламя | реакция горения | запах «паленого», жженых перьев |
| НNO3 (конц.); t, °С | ксантопротеиновая реакция (происходит нитрование бензольных колец в молекуле белка) | без нагревания – появляется желтое окрашивание р-ра; при нагревании и добавлении раствора аммиака белок окрашивается в желтый цвет | |
| Свежеосаж-денный Сu(OH)2 | биуретовая реакция (образуется комплексное соединение) | сине-фиолетовое окрашивание р-ра |
НЕорганические качественные реакции
1. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции.
ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ
А) силикат натрия и соляная кислота 1) выпадение белого осадка
Б) карбонат кальция и соляная кислота 2) выпадение жёлтого осадка
В) цинк и гидроксид натрия 3) выделение газа
Г) нитрат серебра и фосфат калия 4) выделение газа и растворение осадка
5) образование бесцветного желеобразного осадка
2. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции.
ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ
А) сульфид натрия и хлорид меди II 1) выпадение белого осадка
Б) сульфид натрия и хлорид алюминия 2) выпадение чёрного осадка
В) хлорид железа III и гидроксид натрия 3) выделение газа и выпадение белого осадка
Г) нитрат серебра и медь 4) выпадение бурого осадка
5) образование серого осадка и раствора голубого цвета
3. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества между собой.
ВЕЩЕСТВА РЕАКТИВ
А) KCl u CaCl2 1) HCl
Б) BaSO4 u BaSO3 2) K3PO4
B) K2CO3 u K2SO4 3) Ba(NO3)2
Г) ZnSO4 u MgSO4 4) NaOH
5) KI
4. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества между собой.
ВЕЩЕСТВА РЕАКТИВ
А) K2SO4 u KI 1) HNO3
Б) BaCl2 u NaCl 2) Fe2(SO4)3
B) FeCl3 u FeCl2 3) AgNO3
Г) Zn(NO3)2 u NаNO3 4) KOH
5) фенолфталеин
5. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества между собой.
ВЕЩЕСТВА РЕАКТИВ
А) Na2SO4 u NaNO3 1) HCl
Б) H2SO4 u Na2SO4 2) Ba(NO3)2
B) FeCl3 u FeSO4 3) Mg(NO3)2
Г) Li2CO3 u Na2CO3 4) K3PO4
5) лакмус
1. АБВГ 2. АБВГ 3. АБВГ 4. АБВГ 5. АБВГ
5332 2345 2114 3244 2524


КАЧЕСТВЕННЫЕ РЕАКЦИИ НА КАТИОНЫ И АНИОНЫ
| Ион | Условие, реактив, катион | Признаки, сокращенное ионное уравнение реакции |
|
| Нитрат серебра | Белый творожистый осадок |
|
| Нитрат серебра | Желтоватый творожистый осадок |
|
| Нитрат серебра | Жёлтый творожистый осадок |
|
| Растворимые соли бария | Белый осадок |
|
| | Выделение бурого газа |
|
| Нитрат серебра | Ярко-жёлтый осадок |
|
| Растворимые соли бария | Жёлтый осадок |
|
| Растворимые соли меди | Чёрный осадок |
|
| Кислоты | Выделение газа без запаха |
|
|
|
|
|
|
|
|
|
| Щёлочь, | Выделение газа c резким запахом |
|
| Соляная кислота, растворы хлоридов | Белый творожистый осадок |
|
| Пламя | Красное окрашивание |
|
| Пламя | Жёлтое окрашивание |
|
| Пламя | Фиолетовое окрашивание |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Щёлочь | Желеобразный осадок белого цвета, «растворяется» в избытке раствора щёлочи |
№33 (В6) НЕорганические качественные реакции
1. Установите соответствие между веществами и реактивом, с помощью которого их можно отличить.
| Вещества |
| Реактивы |
| А) карбонат натрия и сульфат натрия Б) хлорид алюминия и хлорид калия В) сульфат аммония и сульфат лития Г) карбонат натрия и силикат натрия |
| 1) гидроксид меди (II) 2) натрий 3) соляная кислота 4) бромная вода 5) гидроксид калия
|
2. Установите соответствие между веществами и реактивом с помощью которого можно различить эти вещества.
| Вещества |
| Реактив |
| А) сульфид и бромид натрия Б) сульфат калия и нитрат калия В) хлорид алюминия и хлорид магния Г) гидроксид лития и гидроксид калия | | 1) гидроксид натрия 2) соляная кислота 3) нитрат бария 4) гидроксид меди (II) 5) фосфат натрия
|
3. Установите соответствия между веществами и признаком протекающей между ними реакции
| Реагирующие вещества |
| Признак реакции |
| А) сульфит калия (р-р) и азотная кислота (р-р) Б) гидроксид алюминия и гидроксид натрия (избыток) В) хлорид аммония и гидроксид кальция Г) нитрат бария (р-р) и соляная кислота |
| 1) растворение осадка 2) без видимых изменений 3) образование осадка 4) выделение газа 5) обесцвечивание раствора |
4. Установите соответствие между веществами и реагентом, с помощью которого их можно отличить друг от друга.
ВЕЩЕСТВА РЕАГЕНТ
А) BaSO4 и Ca3(PO4)2 1) H2SO4 (разб.)
Б) BaCl2 и MgCl2 2) HCl (разб.)
В) AgNO3 и KNO3 3) H2O
Г) Na2O и MgO 4) NaNO3
5) HNO3(конц.)
5. Установите соответствие между веществами и реагентом, с помощью которого можно различить эти вещества.
| ВЕЩЕСТВА | РЕАГЕНТ |
| А) FeCl3 и FeCl2 | 1) HCl |
| | |
6. Установите соответствие между веществами, которые необходимо различить, и реактивом, с помощью которого это можно сделать.
Вещества Реактив
А) растворы ZnCl2 и CaCl2 1) фенолфталеин
Б) растворы KOH и Ca(OH)2 2) раствор йодида калия
В) растворы KNO3 и NH4NO3 3) углекислый газ
Г) растворы Pb(NO3)2 и Mg(NO3)2 4) раствор гидроксида натрия
5) раствор хлорида бария
1. АБВГ 2. АБВГ 3. АБВГ 4. АБВГ 5. АБВГ 6. АБВГ
3553 2315 4142 5123 2135 4345

 Получите свидетельство
Получите свидетельство Вход
Вход



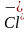
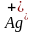
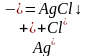
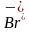
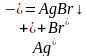
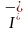
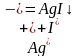
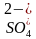
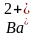
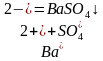
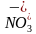
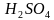 (конц.) и
(конц.) и 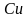
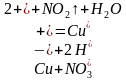
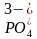
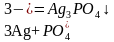









 Задачи на тему "Качественные реакции органических и неорганических веществ" (56.04 KB)
Задачи на тему "Качественные реакции органических и неорганических веществ" (56.04 KB)
 0
0 660
660 24
24 Нравится
0
Нравится
0



