Тема урока: Электролиз 11 класс
Цель: сформировать у учащихся понятие процесса электролиза, как одного из способов получения металлов.
Задачи:
обучающие:
научить учащихся определять процессы, происходящие на электродах, составлять суммарные уравнения реакции электролиза.
научить учащихся пользоваться опорными знаниями, составлять конспект урока.
углубить знание окислительно-восстановительных процессов, понимание практического значения электролиза в природе и жизни человека.
развивающие:
развивать мышление учащихся, научить их делать логические выводы из наблюдений.
закрепить умения и навыки химического эксперимента, умение работать с таблицами, справочным материалом, дополнительной литературой, опорными схемами.
воспитывающие:
формировать интерес учащихся к изучению химии, умение использовать приобретенные знания. Практическое значение электролиза в природе и жизни человека.
Тип урока: изучение нового материала.
Вид урока: проблемно-исследовательская работа
Оборудование: учебник О.С. Габриеляна "Химия 11 класс. Профильный уровень", таблица растворимости, опорный конспект "Приложение", растворы CuSO4, географическая карта России, электролизер, компьютер.
План урока
| Этапы | Виды деятельности | Время(мин.) |
| I.Организационный | Формирование групп, мотивация учебной деятельности: сообщение темы (слайд), цели урока. | 2 |
| II. Актуализация знаний | Фронтальная беседа, анализ схемы, нарисованной на доске. | 3 |
| III. Основная часть | Изучение нового материала, объяснение учителем схемы электролиза | 6 |
| IV. Работа в группах | Самостоятельная работа по изучению опорного конспекта, выполнение заданий | 10 |
| V. Отчет групп | Защита мини-проектов, демонстрация эксперимента | 20 |
| VI. Закрепление | Выводы | 2 |
| VII. Рефлексия |
| 2 |
| VIII. Домашнее задание | 18 учебник О.С. Габриелян 2010 г | - |
Ход урока
Запись на доске:
"Открытия в области электрохимии представляют собой одну из самых больших революций в химии и открывают эру новых открытий" Д.Ф. Даниэль (английский электрохимик)
I. Организационный момент
приветствие учителя;
формирование групп;
сообщение темы, цели урока.
II. Актуализация знаний
Фронтально: работа с классом.
1. Что такое электролиз?
2. Какое основное свойство металлов?
3. Что вы знаете об ОВР?
4. Самый сильный восстановитель?
5. Самый сильный окислитель?
6. Дать определение электролизу. Прочитать в книге определение (18).
III. Основная часть.
Объяснение учителем схемы электролизера (слайд);
рассмотрение случаев электролиза:
а) расплава,
б) раствора;
Алгоритм процесса
Устройство электролизера
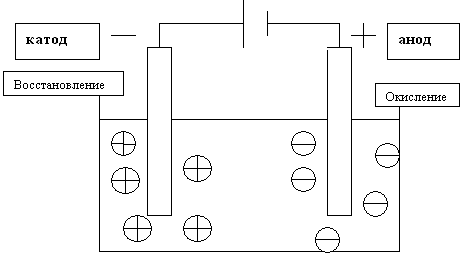
Учитель делает пояснения к схеме: На схеме изображено как в раствор электролита опущены электроды, соединенные с источником постоянного эл. тока. Отрицательно заряженный электрод называется катодом, а положительный анодом.
Приложение 1
Приложение 2
Приложение 3
Правила катодного процесса (слайд):
А - в расплавах
Что есть, то и выделяется.
Б - в растворах (мешает вода)
От Li до Al восстанавливается H2 из воды (2H2O+2e=H2+2OH-)
От Mn до H2 восстанавливается Ме+ H2 из воды.
От Cu и далее восстанавливается Me.
Правила анодного процесса (слайд):
Бескислородные анионы (кроме F-) окисляются до простых веществ
Кислородсодержащий анион. Из H2O (O2)
2H2O - 4е = О2 + 4Н+
IV. Работа в группах
(Перед началом работы в группах учитель предлагает провести динамическую паузу, необходимую для снятия напряжения и утомления мышц)
Ребята, вы приступаете к самостоятельной работе в группах.
1-я и 2-я группы - это теоретики, 3-я - экспериментаторы, 4-я - практики. Вы получаете задания для исследовательской работы.
1-я группа. Электролиз расплава KI, составить схему.
2-я группа. Электролиз раствора KI, составить схему.
3-я группа. Провести электролиз раствора CuSO4, описать свои наблюдения и сделать предположения
(перед тем, как приступить к работ, учитель напоминает учащимся инструктаж по технике безопасности при работе с электроприборами).
4-я группа. Презентация сообщений о применении и значении электролиза.
V. Отчет групп.
Представление работ всех групп, 1-я и 2-я группы вывешивают схемы на доску, и докладчики подводят итоги работы групп. Сравнить, найти общее и различия в продуктах и сформулировать выводы.
| Схема расплава | Схема раствора |
| Электролиз расплава KI - K++I- Катод K++1e = К0 - восстанавливается Анод 2I- - 2e = I20 - окисляется KI = K0 + I20 Продукты электролиза: калий, йод. | Электролиз раствора KI KI - K++I- На катоде - К+ не восстанавливается H2O + 2e - 2OH- + H2 На аноде бескислородный остаток окисляется 2I- - 2e I- 20 H2O не окисляется 2H2O+2I- - 2OH+H2+I2 2K++2H20+2I- - 2OH- +H2+I20 +2K 2KI+2H2O - 2KOH+H2+I2 Продукты электролиза: щелочь, водород, йод. |
Представление работы 3-й группы с демонстрацией результатов эксперимента и обсуждение о прохождении процесса электролиза в предположении.
Учитель: все ли вы согласны, есть ли предположения у других групп?
4-я группа отчитывается о своей работе по плакату и презентация (слайды) о роли и значении электролиза.
VI. Закрепление, подведение итогов, выводы.
Выводы:
- Электролиз - окислительно-восстановительный процесс.
- Протекает в растворах и расплавах электролитов.
- Под действием электрического тока
- Продукты электролиза определяются характером металлов и кислотных остатков солей (ряд напряжение металлов и окислительный ряд ионов)
- Электролиз растворов энергетически выгоднее, чем расплавов, т.к электролиты солей, щелочи, оксидов плавятся при очень высоких температурах.
- Тестирование (слайд № 11, если есть резервное время)
VII. Рефлексия
Я (как я прожил урок? Интересно, скучно, непонятно::..)
МЫ (как нам понравилось работать в группах?)
ДЕЛО (чему мы научились?)
VIII. Домашнее задание параграф 18. Электролиз.
Творческое задание на выбор:
- подготовить презентации и сообщения о химических заводах по производству металлов (возможен вариант в электронном и печатном виде).
РЕЗЕРВ
1. Занимательная проблема.
Институт прикладной физики Китайской академии наук сообщил о результатах исследования гробницы полководца Джоц-Чжу, похороненного в 237 г н. Спектральный анализ орнамента украшающего саркофаг показал, что он состоит из сплава содержащего 85% Al 10% меди 5% Mg как могли древние китайские мастера получить сплав
2. Тестовый контроль знаний
1. Расплав какого вещества подвержен электролизу?
а - оксид кальция б - парафин в - глюкоза г - азот
2. Что следует подвергнуть электролизу для получения хлора?
а - хлорную воду б - раствор хлората калия
в - расплав хлорида калия г - хлор электролизом не получают
3. Цвет лакмуса в околокатодном пространстве при электролизе раствора бромида натрия
а - малиновый б - фиолетовый в - красный г - синий
4. Какое вещество нельзя получить при электролизе раствора поваренной соли?
а - Na б - H2 в - Cl2 г - NaOH
5. При электролизе раствора сульфата цинка с инертными электродами на аноде выделяется
а - Zn б - O2 в - H2 г - SO2
6. При электролизе раствора нитрата меди(II) с медными электродами на аноде будет происходить
а - выделение NO2 б - выделение меди в - выделение O2 г - растворение анод.

 Получите свидетельство
Получите свидетельство Вход
Вход











 Урок по химии электролиз 11 класс (29.8 KB)
Урок по химии электролиз 11 класс (29.8 KB)
 0
0 592
592 14
14 Нравится
0
Нравится
0




