Урок 29
Тема. Понятие о оксидах. Окисления. Горения. Условия возникновения и прекращения горения
Цели: расширить представление о оксиды как продукты горения, процесс горения, самопроизвольное окисление; объяснить условия возникновения и прекращения горения, механизм действия средств пожаротушения, меры противопожарной безопасности в быту и на производстве; развивать умения составлять уравнения химических реакций взаимодействия кислорода с простыми веществами; углубить знания о составе сложных веществ на примере оксидов; совершенствовать навыки составления бинарных соединений.
Тип урока: углубление знаний.
Формы работы: групповая и индивидуальная формы работы, беседа.
Оборудование: периодическая система химических элементов, опорная схема «Кислород».
ХОД УРОКА
I. Организация класса
II. Актуализация опорных знаний
Класс делится на группы, каждая группа получает задание за изученным материалом.
Группа 1
1. Расскажите о распространении Кислорода в природе.
2. Допишите уравнения реакций и расставьте коэффициенты:
а) Mg + O2 ![]()
б) HgO ![]()
Группа 2
1. Расскажите о строении молекулы кислорода, его физические свойства.
2. Допишите уравнения реакций и расставьте коэффициенты:
а) N2 + O2 ![]()
б) KNO3 ![]()
Группа 3
1. Расскажите о химических свойствах кислорода.
2. Допишите уравнения реакций и расставьте коэффициенты:
а) S + O2 ![]()
б) KMnO4 ![]()
Группа 4
1. Расскажите о лабораторные способы получения кислорода.
2. Допишите уравнения реакций и расставьте коэффициенты:
а) Zn + O2 ![]()
б) H2O2 ![]()
Группа 5
1. Расскажите о применении кислорода.
2. Допишите уравнения реакций и расставьте коэффициенты:
а) P + O2 ![]()
б) H2O ![]()
Один представитель каждой группы устно отвечает на теоретический вопрос, второй записывает уравнение реакции в виде столбика: реакции соединения, реакции разложения.
III. Подведение итогов работы групп, оценивание
IV. Углубление знаний
На доске записаны два столбика химических уравнений. Один столбик характеризует способы получения кислорода (ученики определяют, какой именно), второй — химические свойства кислорода.
• Как называются продукты горения простых веществ в кислороде? (Оксиды)
• Назовите оксиды, записанные на доске.
(Ученики по очереди называют оксиды.)
• А могут ли гореть сложные вещества? (Так, например, бумага, ткань, бензин, природный газ. Природный газ содержит сложное вещество метан CH4. Во время горения образуются два оксиды: CH2 + 2O2 ![]() CO2 + 2H2O)
CO2 + 2H2O)
Вывод. Каждый элемент, входящий в состав сложного вещества, образует оксид.
• В каком случае горение происходит быстрее: в чистом кислороде или на воздухе? (В чистом кислороде)
А без доступа воздуха горение невозможно вообще.
• Бумага хорошо горит. А почему наши тетради не загораются сейчас? (Необходимо внести их в огонь, то есть нагреть. Для каждого вещества существует температура, при которой она загорается, например, для дерева эта температура составляет порядка 270 °С, для углерода — 350 °С, для белого фосфора — около 40 °С, для азота — около 2500 °С)
Такая температура называется температурой возгорания.
• Итак, какие условия должны выполняться для возникновения горения? (Нагрев вещества до температуры возгорания и наличие кислорода)
• А как остановить процесс горения? (Перекрыть доступ кислорода. Охладить вещество до температуры ниже температуры возгорания)
• Какие средства пожаротушения вы знаете? (Огнетушители; песок; вода и др.) Некоторые вещества могут медленно окисляться под воздействием воздуха без температуры возгорания. Например, железо ржавеет, серебро покрывается серым налетом. Такой процесс называют самопроизвольным окисненням.
V. Закрепление изученного материала
Задача 1. Составьте уравнение горения предложенных ниже веществ и расставьте коэффициенты:
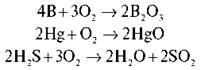
Задание 2. Вычислите массовые доли Кислорода в полученных оксидах и расположите их в порядке возрастания массовой доли Кислорода.
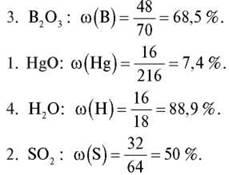
VI. Подведение итогов
Сегодня мы узнали, что реакцией горения можно управлять. У каждого вещества есть температура возгорания. Например, для Na или P она очень низкая, эти вещества называются легковоспламеняющимися и должны храниться в соответствующих условиях согласно правил техники безопасности. Подводим итоги урока. Выставляем оценки.
VII. Домашнее задание
Прочитать параграф, ответить на вопросы, повторить физические и химические свойства кислорода.
Творческое задание. Подготовить сообщение о круговороте Кислорода в природе, использование кислорода и его биологическую роль.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Урок химии в 10 классе "Решение задач на тепловой эффект" (31.48 KB)
Урок химии в 10 классе "Решение задач на тепловой эффект" (31.48 KB)
 0
0 459
459 5
5 Нравится
0
Нравится
0


