1
Открытый урок по химии
«Типы химических реакций»
Галкова Светлана Евгеньевна,
Учитель химии
Н. Новгород 2016 год
2
Самоанализ урока
Урок проводился в 8 классе. В классе обучаются учащиеся разного уровня учебных достижений. По итогам 2 четверти: КО -50% , СОУ -57% , РУД - 6. Мониторинг качества обучения по уровням : низкий уровень -0 , удовлетворительный уровень -1(17%) , средний уровень -4 (66%) , достаточный уровень -0 , высокий уровень – 1(17%). С учётом организационной структуры и состава класса ( мальчиков -2(33%) , девочек – 4 (67%)), учащиеся имеют достаточную мотивацию к учебной деятельности, общие учебные навыки, высокую организованность , активность и исполнительскую дисциплину, положительный уровень учебной культуры, стремление к усвоению не только основного материала, а также сложного и дополнительного. Уроки в данном классе проходят интересно, увлекательно. Любят творческие, нестандартные задания. Данный урок является пятым в теме “Химические ракции”. Тип урока – изучение нового материала, который позволит учащимся изучить типы химических реакций.
Цели урока: организовать деятельность учащихся направленную на: ознакомление учащихся с типами химических реакций; формирование умений и навыков различать типы химических реакций, читать и записывать уравнения химических реакций; создать условия для развития речи учащихся, логического мышления, активности, самостоятельности; способствовать воспитанию: интереса к предмету, целеустремлённости, культуры общения в процессе диалога с учителем.
Важным этапом урока является мотивация учащихся в начале урока, эффективная работа через осознание и постановку целей урока. Достижение целей урока осуществлялась через использование различных видов деятельности: коллективная (составление ЛСМ(логико-смысловой модели по теме урока), индивидуальной (решение задачи повышенного уровня), разноуровневой самостоятельной работы,а также использование элементов инфомационной технологии. Организация образовательного процесса на уроке была направлена на усвоение содержания учебного материала, эффективное овладение составлением ЛСМ, способствующая развитию познавательного интереса и самостоятельности в приобретении знаний.
Различные формы организации деятельности учащихся(индивидуальная,творческая, самостоятельная, коллективная) способствовали активизации мыслительной деятельности учащихся, развитию умения сообщать полученную информацию, делать выводы и аргументировать. На уроке все учащиеся были включены в работу. Результаты выполнения самостоятельной работы показали, что цели урока достигнуты, план реализован полностью, время на уроке было использовано рационально.
3
Цель урока. По оканчанию урока учащиеся должны знать определение типов химических реакций, узнавать типы химических реакций, уметь записывать типы химических реакций.
Задачи урока:
1) организовать деятельность учащихся, направленную на ознакомление учащихся с типами химических реакций;
2)формирование умений и навыков:
- различать типы химических реакций,
-читать и записывать уравнения химических реакций;
3)создать условия для развития речи учащихся, логического мышления, активности, самостоятельности;
4)способствовать воспитанию интереса к предмету, целеустремлённости, культуры общения в процессе диалога с учителем.
Тип урока. Изучение нового материла
Оборудование урока: цветной мел, конверты с карточками цветного картона у каждого ученика, папки “Справочные материалы “В помощь ученику”” на каждой парте, приложения “Раздаточный материал” у каждого ученика:
1. Химические уравнения
2. Типы химических реакций
3. Для работы за компьютером “Типы химических реакций”
4. Лист – “самооценка”
4
Технологическая карта урока “Типы химичеких реакций”
| № п/п | Этапы урока | Деятельность учителя | Деятельность учащихся |
| 1. | Организационный этап урока | Приветствие учащихся. Создание доброжелательной обстановки на уроке. Проводит психологический тренинг Предлагает показать карточку настроения в начале урока | Слушают учителя, участвуют в беседе и тренинге, показывают карточку настроения в начале урока |
| 2. | Организационно – мотивационный этап | Создаёт ситуацию для самоопределения учащихся на результат познавательной деятельности на уроке, используя эпиграф урока | Слушают и участвуют в обсуждении |
| 3. | Проверка домашнего задания | Вызывает к доске учащихся и организует самостоятельную работу с классом. Проверяет выполнение домашнего задания | Участвуют в проверке заданий по карточкам, помогают исправлению ошибок друг у друга |
| 4. | Объяснение нового материала | Читает эпиграф этапа урока Вместе с классом работает с уравнениями химических реакций, записанными на доске Обращает внимание на цвет, записанного уравнения Подводит учащихся к теме урока В совместной деятельности формулирует тему и цели урока Вызывает к доске ученика для составления ЛСМ, используя цветной мел | Слушают, читают уравнения химических реакций, называют исходные вещества и продукты реакций, сравнивают и находят отличия Вормулируют цели урока, исходя из темы урока В совместной деятельности составляют ЛСМ, используя цветные карандаши |
| 5. | Этап закрепления полученных знаний | Читает девиз этапа, организует работу с учебником, материалом ЛСМ, создаёт психологическую разгрузку. Снимает умственную нагрузку Организует индивидуальную и самостоятельную работу за компьютером и классом, взаимопроверку
| Слушают, работают с учебником, находят определения типов химических реакций, дополняют ЛСМ примерами, выслушивают сообщения учащегося, рассматривают схемы ЛСМ, составленные ученицей, участвуют в физкультминутке Выполняют по очереди задания за компьютером и за партой Осуществляют взаимопроверку |
| 6. | Этап информации домашнего задания | Читает подготовленную запись на доске: §17, упражнения 6, 7; Творческое задание: составить свою ЛСМ по теме “Типы химических реакций” | Записывают в дневник и слушают объяснение |
| 7. | Итоги урока | Предлагает учащимся заполнить “Лист - самооценка | Заполняют “Лист – самооценка” |
| 8. | Рефлексия | Предлагает показать карточку настороения в конце урока | Показывают карточку настороения |
5
1. Организационный этап
Учитель. Добрый день, ребята! Я рада всех вас видеть у себя на уроках, которые приносят мне минуты радости и удовольствия и это я хочу выразить стихами.
Перед долгой разлукой в свой класс я вхожу.
Наконец – то! Вот здесь только я и дышу.
Здесь дают мне энергию 6 пар глаз.
Я могу поделиться и дать про запас,
Вот взметнулся навстречу улыбок салют.
Ты, мгновенье, прекрасно, - себе говорю.
Думаю , вы чувствуете тоже, и время, которое вы проведёте со мной, принесёт вам пользу. Я хочу пожелать вам внимания, терпения и успеха на уроке.
2 . Организационно – мотивационный этап
Девиз урока:
Не позволяй душе лениться,
Чтоб в ступе воду не толочь,
Душа обязана трудиться
И день и ночь!
И день и ночь!
Учитель. Покажите карточку вашего настроения в начале урока
3 . Проверка домашнего задания
1)Упражнение 6 – у доски один ученик
Упражнение 7 – у доски второй ученик
2)Класс выполняет задание по карточкам самостоятельно:
(приложение 1)
Домашнее задание сверяют с ответами на доске
Задание по карточкам с помощью взаимопроверки
4 . Объяснение нового материала
Учитель. Девиз этапа:
Думать коллективно,
работать оперативно,
спорить доказательно,
вот что для нас обязательно!
На доске записаны примеры уравнений химических реакций мелками разного цвета
2Zn + O2 = 2ZnO (1)
2KCLO3 = 2KCL + 3O2 (2)
2HCL + Mg = MgCL2 + H2↑ (3)
1. Вопросы классу:
6
- Прочитать уравнения химических реакций;
- Указать в уравнении химической реакции исходные вещества и продукты реакции;
- Найти отличия между уравнениями химических реакций (обращает внимание, каким цветом записаны уравнения реакции)
2. Сообщение темы урока
3. Постановка целей урока
Учитель. Ребята, скажите, если бы вы были учителем, то какие бы вы поставили задачи перед учениками и что хотели бы от них добиться в конце урока.
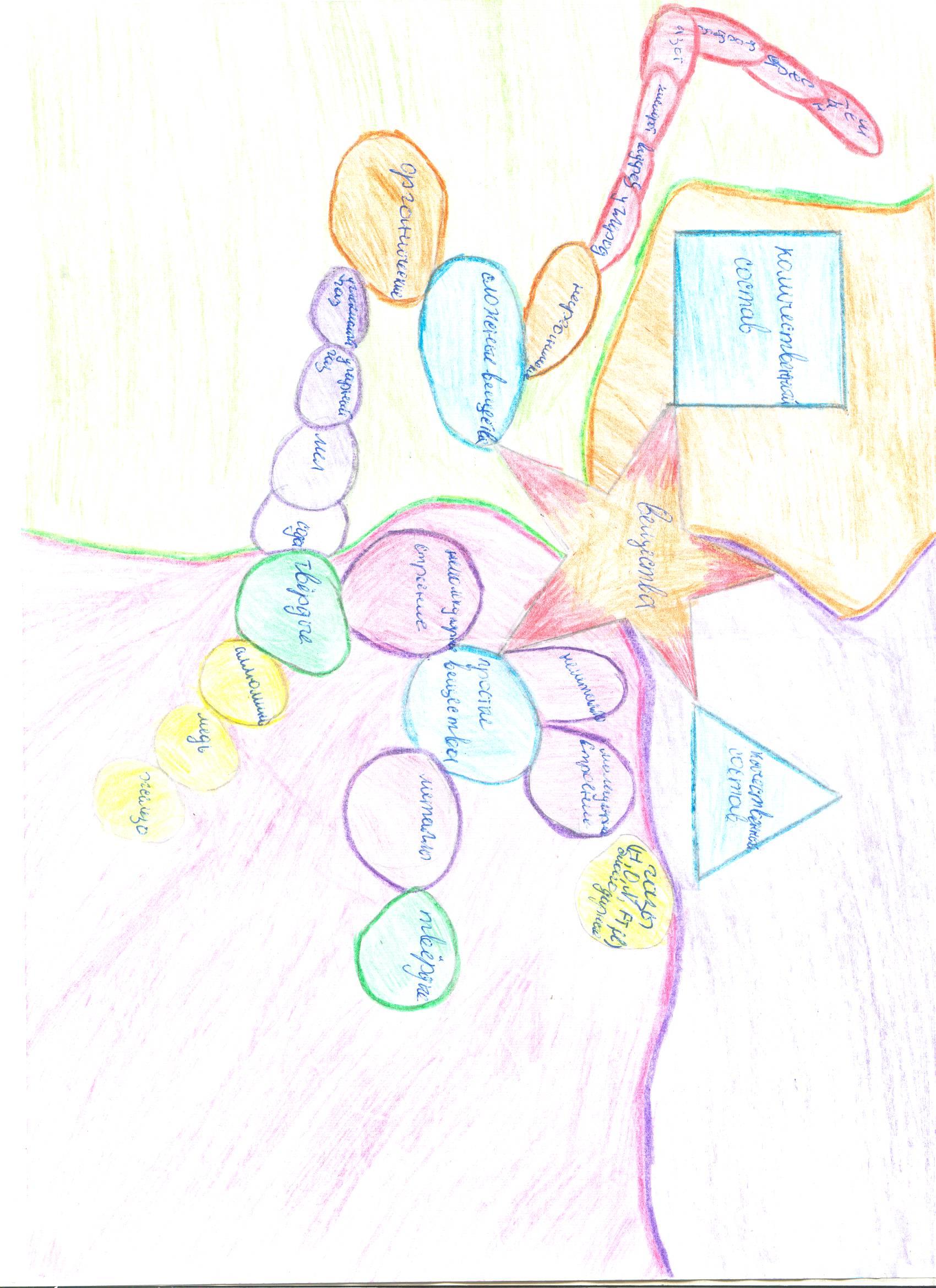
4. Составление ЛСМ (логико-смысловой модели по теме урока).
К доске вызвана ученица, используя цветные мелки и записи на доске уравнений химических реакций, составляет ЛСМ «Типы химических реакций»
5. Осмысление полученных знаний. Работа с учебником, стр.77-79.
После каждого направления учащиеся находят определение типа уравнения химической реакции и записывают по два примера на ЛСМ каждого типа. В ходе данной работы учащиеся проговаривают определения.
6. Психологическая разгрузка.
7
Чтение творческой работы ученицы класса: «Сказка «Дружба атомов»» и демонстрация творческих работ по составлению ЛСМ
5. Закрепление изученного
Девиз этапа: Знание + Внимание = Успех
1. Работа за компьютером. Учащимся предложена работа на узнавание типа уравнения химической реакции. В таблице (приложение 3), которая им предложена, они должны закрасить прямоугольник цветом каждого уравнения химической реакции, т. е. тем цветом, которым записаны уравнения реакций в таблице, на доске и ЛСМ.
8
За компьютером работают учащиеся по очереди. За партами учащиеся выполняют упражнение 2 в учебнике. Проверка осуществляется с помощью карточек цветного картона. Проверка деятельности учащихся за компьютером осуществляется с помощью ученицы класса и учителя.
Индивидуальное задание для учащегося с высокими учебными возможностями. Изучить решение примера 16* «Сборник задач по химии» на стр. 42 и решить задачу № 242*
VI. Физкультминутка. Учитель показывает формулы. Если простое вещество, то два хлопка над головой, если сложное вещество, то два притопа ногами. Надевание колечек на кисти пальцев.
Самостоятельная работа по карточкам (приложение 3)
9
VII. Дом задание. §17, упр. 6,7. Творческое задание. Составить ЛСМ по теме «Типы химических реакций»
VIII. Итоги урока. Заполнение « Лист – самооценка» (приложение 5)
IX. Минута благодарения
Отметки за урок: 10баллов, 7 баллов, 7 баллов, 6 баллов, 5 баллов, 5 баллов
Учитель. Покажите карточки вашего настроения в конце урока
10
11
Список использованной литературы
1. Шиманович И. Е. Химия 8 класс / Минск «Народная асвета», 2005 г.
2. Хвалюк В. Н. Сборник задач по химии /Минск «Народная асвета»», 2006 г.
3.Мянник Т. Н. Химия «Сборник самостоятельных работ» /Минск «Сэр – Вит», 2010 г.
4. Иванютина З. М. Химия 8 класс Карточки – задания /ОДО «Аверсэв», 2007 г.
5. Химия: Праблемы выкладання», №2, 2011 г.
6. Химия: Праблемы выкладання», №3, 2011 г.
7. Химия: Праблемы выкладання», №12, 2011 г.
8. Химия: Праблемы выкладання», №1, 2012 г.
9. Химия: Праблемы выкладання», №2, 2012 г.
10. Старикова М. Г. Современный урок: пособие для педагогов, администрации учреждений / Белый ветер, 2010 г.
11. Городович А. М. Организационно-управленческая модель учреждения образования: пособие для руководителей учреждений образования, их заместителей и педагогов
Приложение 1
Проверочная работа «Химические уравнения»
1. В уравнении реакции 2NH3 = N2 + 3H2:
А) подчеркните коэффициенты;
Б) выделите знаком О индексы;
В) выпишите формулы продуктов реакции______________________________
______________________;
Г) укажите формулу исходного вещества
2. Поставьте недостающие коэффициенты:
А) H2 + CL2 = …HCL;
Б) … HI = H2 + I2;
В) Zn + …HCL = ZnCL2 + H2;
Г) Mg + …HCL = MgCL2 + H2
Приложение 2
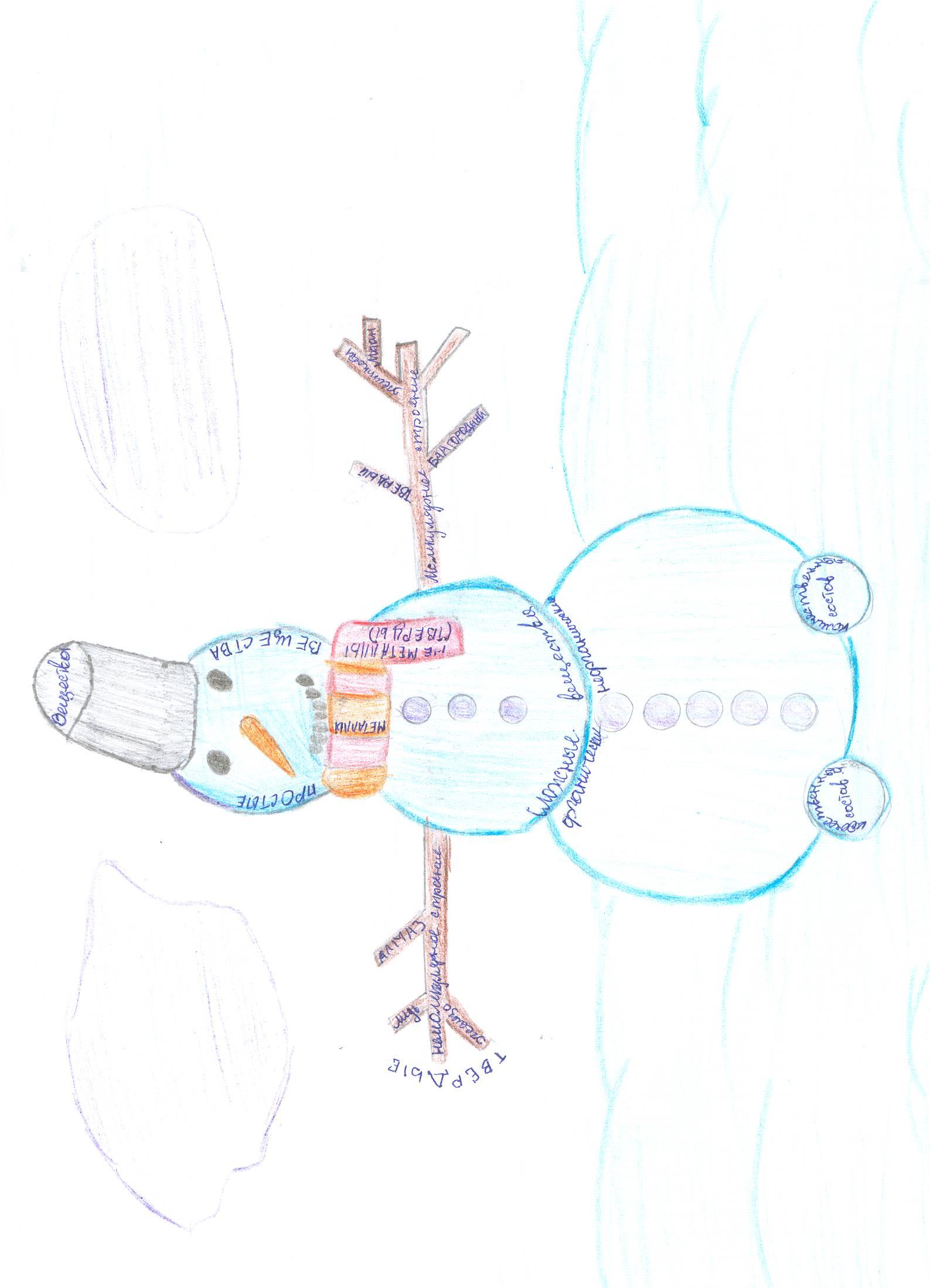
Творческие работы ученицы класса Ворогушиной Елизаветы
Сказка «Дружба атомов»
Всё случилось в далёком, далёком прошлом, когда науке было ещё многое неизвестно. Жил-был на свете атом золота, он был печальный от того, что был всегда один. Ему было скучно, грустно и вот он решил найти себе друга и никогда с ним не расставаться. Но он хотел найти себе не просто хорошего товарища, а такого друга, который был бы на него похож, даже не похож, а был бы полной его копией. И вот он начал своё путешествие в поисках друга. Атом очень долго искал друга и вот, кажется, нашёл. Он нашёл себе друга-атома серебра. Казалось, они сдружились, но вот атом золота начал находить различия между собой и атомом серебра: то это не так, то другое не так как у него. Атомы поняли, что они разные, и перестали дружить. Атом золота пошёл дальше искать друга. Метался, метался он по свету и нашёл атом кремния и стали они дружить, но тоже поняли, что разные. И отправился атом дальше искать друга. Прошло немного времени, и он нашёл себе друга, который был бы тоже атомом золота и копией другого атома. Стали они жить рядом, не отрываясь друг от друга даже на один миллиметр. И этим показали пример другим атомам, которые стали объединяться в группы не только по 2, но и по 4 и больше атомов…. Такие группы называются молекулы. А те, кто не захотел быть рядом друг с другом и по сей день остались одни.


Приложение 3.
Тренировочная таблица «Типы химических реакций»
|
Уравнения реакции Соединения Разложения Замещения |
Тип реакции |
|
P2O5 + H2O = 2 HPO4 |
|
|
CO2 + CaO = CaCO3 |
|
|
Zn + 2HCL = ZCL2 + H2↑ |
|
|
Cu(OH)2 = CuO + H2O |
|
|
K2O + H2O = 2KOH |
|
|
Ni + CuSO4 = NiSO4 + Cu↓ |
|
|
H2CO3 = CO2↑ + H2O |
|
|
2HCL = CL2 + H2 |
|
Приложение 4.

Приложение 5.
Лист – «самооценка»
Фамилия, имя ученика _____________________________________
Моё восприятие темы урока (нужное подчеркнуть):
1. Усвоил всё; 2. Усвоил почти всё;
3. Усвоил частично, нуждаюсь в помощи
Как я работал на уроке (нужное подчеркнуть):
1. Отлично
2. Хорошо
3. Удовлетворительно
4. Неудовлетворительно
Я оцениваю свою работу в баллах (нужной подчеркнуть)
1, 2, 3, 5, 6, 7, 8, 9, 10

 Получите свидетельство
Получите свидетельство Вход
Вход
















 Типы химических реакций (разработка урока) (0.87 MB)
Типы химических реакций (разработка урока) (0.87 MB)
 0
0 1436
1436 193
193 Нравится
0
Нравится
0






