Предмет ___химия______ Класс _______9_____________
Базовый УМК :_Габриелян. О. С. Химия. 9 кл. Базовый уровень. - М.: Дрофа_________________________________
Тема урока:_Щелочные металлы________________________________
Цель урока: формирование систематизированных понятий об щелочных металлах, их свойствах и практическом применении.
Планируемые результаты освоения основной образовательной программы
| Личностные | Метапредметные | Предметные |
| - формирование ответственного отношения к учению, готовности и способности обучающихся к саморазвитию и самообразованию; - формирование целостного мировоззрения; - формирование ценности здорового и безопасного образа жизни; - формирование основ экологической культуры. | - умение устанавливать причинно-следственные связи; - умение создавать, применять и преобразовывать знаки и символы; - работать индивидуально и в группе; -владение устной и письменной речью, монологической контекстной речью;
| - формирование систематизированных представлений о веществах, овладение символическим языком химии; - осознание объективной значимости основ химической науки; - формирование умений устанавливать связи между реально наблюдаемыми химическими явлениями и процессами, происходящими в микромире; - приобретение опыта использования различных методов изучения веществ. |
Планируемое формирование и развитие универсальных учебных действий
| Личностные | Регулятивные | Познавательные | Коммуникативные |
| - установление учащимся значения результатов своей деятельности для удовлетворения своих потребностей, мотивов, жизненных интересов; | - целеполагание как постановка учебной задачи на основе соотнесения того, что уже известно и усвоено учащимися, и того, что ещё неизвестно; - оценка — выделение и осознание обучающимся того, что уже усвоено и что ещё нужно усвоить, осознание качества и уровня усвоения; оценка результатов работы;
| А. Общеучебные действия: - структурирование знаний; - осознанное и произвольное построение речевого высказывания в устной и письменной форме; - рефлексия способов и условий действия, контроль и оценка процесса и результатов деятельности; Б. Знаково-символические действия: - преобразование объекта в пространственно-графические или знаковосимволические модели; В. Логические действия: - анализ объектов с целью выделения признаков (существенных, несущественных); -) установление причинно-следственных связей; Г. Постановка и решение проблемы: - формулирование проблемы. | - постановка вопросов — инициативное сотрудничество в поиске и сборе информации; - умение с достаточной полнотой и точностью выражать свои мысли в соответствии с задачами и условиями коммуникации; -владение монологической и диалогической формами речи. |
Задачи урока:
познакомиться с группой щелочных металлов учащихся на лично-значимом уровне;
подвести обучающихся к понимаю необходимых знаний о химических свойствах щелочных металлах в повседневной жизни;
помочь обучающимся выявить особенности химических свойств щелочных металлах и их соединений;
подвести обучающихся к постановки цели учебной деятельности, выбору способа и средств ее реализаций;
подвести обучающихся к самостоятельному формулированию правил обращения с щелочными металлами;
организовать рефлексию учебной деятельности.
Тип урок: комбинированный
Необходимое оборудование : Li, Na2O, K2O, NaOH, KOH, Na2CO3, K2CO3, NaCl, Ca(OH)2, NH4Cl, H2Oспиртовка, спички, индикатор, периодическая система химических элементов Д.И.Менделеева, компьютер, проектор
План урока:
I. Организационный момент (1-2 мин).
II. Опрос-повторение (5-7 мин.).
III. Изучение нового материала (25-30 мин.) по плану (записывается на доске по мере объяснения).
IV. Подведение итогов объяснения, рефлексия, закрепление знаний (3-5 мин.).
V. Домашнее задание, выставление оценок (1-2 мин.).
Содержание урока
I. Организационный момент (1-2 мин.)
II. Опрос-повторение (5-7 мин.)
3 ученика выходят к доске для выполнения индивидуальных заданий;
10 учеников получают письменные задания на месте по карточкам. (Карточки прилагаются).
Остальные учащиеся отвечают на вопросы устно (фронтальный опрос по пройденным темам).
III. Изучение нового материала (25-30 минут)
Учитель: Ребята у каждого из нас, есть на кухне такое вещество как поваренная соль, все вы с ней прекрасно знакомы, одним из химических элементов в составе поваренной соли входит калий. Он относиться к группе щелочных металлов. И сегодня на уроке мы свами более подробно познакомимся с этой группой металлов. Запишите тему урока: "Щелочные металлы".
1) Строение атомов щелочных металлов .
Рассмотрим атомное строение первых тех щелочных металлов в периодической системе химических элементов Д.И. Менделеева (слайд).
Запишите схему в тетради:
Li+3))
2 1
Na+11)))
281
K+19))))
2881
Определить какие свойства характерны для этих элементов.
(работа с учебником).
2) Восстановительные свойства
Обсуждение восстановительных свойств и их роли в соединении с другими химическими элементами.
3) Получение и физические свойства щелочных металлов
Учитель демонстрирует опыты: а)2Li +H2O=2LiOH.
В ходе проведения эксперимента с учащимися по результатам наблюдения проводится беседа.
Проблема: Почему индикаторы меняют свой цвет в щелочном растворе?
Li + H2O ![]() LiOH (основание)
LiOH (основание) ![]() Li+ + ОН-.
Li+ + ОН-.
Связь с жизнью. Как можно распознать гидроксид лития (щелочь)?
Физические свойства щелочных металлов. Серебристо-белые мягкие вещества (режутся ножом), с характерным блеском на свежесрезанной поверхности. Все они легкие и легкоплавкие, причем, как правило, плотность их возрастает от Li к Cs, а температура плавления, наоборот, уменьшается. (ТБ, Экология)
4) Химические свойства щелочных металлов
Демонстрация опытов. Горения лития. (4Li + O2 = 2Li2O – изменения цвета пламени в малиновый).
(Причинно-следственная связь «строение – свойство»).
Механизм образования взаимодействия щелочных металлов с неметаллами (слайд): 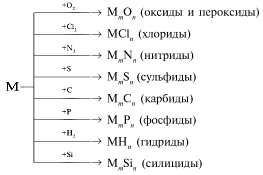
5) Применение щелочных металлов
Работа с учебником. (Причинно-следственная связь «свойство-применение»).
6) Физические свойства соединений щелочных металлов
Демонстрация соединений и рассказ о их свойствах, запись в тетрадь (слайды):
Na2O, K2O, NaOH, KOH, Na2CO3, K2CO3, NaCl
7) Химические свойства солей аммония
Прогнозирование. Каковы свойства соединений щелочных металлов?
(демонстрируются соответствующие реакции):
![]()
![]()
![]()
Обсуждение реакций.
8) Применение соединений щелочных металлов (слайд)
(Причинно-следственная связь «свойство-применение»).
IV. Закрепления знаний, формулировка правил обращения с щелочными металлами. (3-5 мин.)
Учитель: Запишите формулы следующих веществ: сульфат калия, гидроксид натрия, карбонат натрия, хлорид лития.
- Как отличить литий от калия?
- Запишите уравнения реакций следующих превращений:
Натрий→ пероксид натрия → оксид натрия → гидроксид натрия → сульфид натрия.
V. Подведение итогов урока, рефлексия Выставление (дополнительно) отметок. Домашнее задание: §_11__ упр. _2__. Окончание урока, рефлексия, прощание с классом.
Составила Саранина А.А.
Учитель химии и биологии.
МБОУ Субботинская СОШ им. Героя Советского Союза С.У. Кривенко
4

 Получите свидетельство
Получите свидетельство Вход
Вход











 "Щелочные металлы" (41.94 KB)
"Щелочные металлы" (41.94 KB)
 0
0 588
588 5
5 Нравится
0
Нравится
0






