
8 - 11 классы
Учитель химии Пономарева Л.Л.
г. Рязань
МБОУ «Школа № 66»
2020 г .

- Решение типовых задач базового уровня по химии.
Для решения задач I – го типа по химическим формулам, необходимо записать химические формулы.
Записываем в тетрадь химические формулы.

ФОРМУЛЫ.
I. Расчет по химическим формулам
n- количество вещества (моль).
N -число частиц
N- число Авогадро = 6 10
m- масса (Г)
M- молярная масса (г/моль)
V- объем (л)
V - молярный объем = 22,4 л/моль
А
N
V
m
n =
=
=
N
V
M
A
m
m

Задача № 1
- Сколько молекул содержится в 5 моль воды?
- Дано: Решение:
- n (H O ) = 5 моль
- N (H O ) = ?
2
23
23
.
N (H O ) = 5 моль 6 10 = 30 10 молекул
2
2
.
N
.
N = n N
n =
A
23
.
N
A
Ответ: N ( H O )= 30 10 молекул
2
23
.
N = 6 10 молекул
A

Задача № 2
- Найти массу 10 моль серы ?
- Дано: Решение:
- n (S) = 10 моль
- m ( S ) = ?
m (S) = 10 моль 32 г/моль =320 г
m
Ответ: m (S ) =320 г
.
n =
m = n M
M
M (S) = 32 г/моль (берем в периодической таблице Ar (S) = M(S)

Задача № 3
- Какой объем занимает 2 моль водорода ?
- Дано: Решение:
- n (H ) = 2 моль
- V ( H ) = ?
2
.
V ( H ) = 2 моль 22,4 л/моль = 44,8 л
2
2
V
n =
.
V = n V
V
m
Ответ: V ( H )= 44,8 л/моль
m
2
V = 22,4 л/моль ( молярный объем, надо знать, см. в формулах)
m

Задача № 4
- Найти массу 10 л азота ?
- Дано: Решение:
- V(N ) = 10 л
2
28 г/моль 10 л
m (N ) =
= 12,5 г
m (N ) = ?
2
2
22,4 л/моль
m
.
M V
V
m =
=
Ответ: m (N ) = 12,5 г
M
2
V
m
V
m
.
M (N )=2 14 =28 г/моль ( Ar азота берем из период. табл.)
2
V ( N ) = 22,4 л/моль
m
2

Задача № 5
- 5 г железа сгорает в кислороде. Найти массу оксида? Дано: Решение: m(Fe)=5 г Fe + O = Fe O m(Fe O )- ?
- 5 г железа сгорает в кислороде. Найти массу оксида?
- Дано: Решение:
- m(Fe)=5 г
- Fe + O = Fe O
- m(Fe O )- ?
M(Fe)=56 г/моль
n(Fe)=
- M(Fe)=56 г/моль n(Fe)=
Х моль
0,09моль
4
3
2
3
2
2
4 моль
2 моль
2
3
m
.
0,09 2
х
.
0,09
n =
n M
m =
= 0,05 моль
х =
=
M
4
4
2
.
m(Fe O )= 0,05 моль 160г/моль =8 г
5 г
2
3
=
0,09моль
56г/моль
.
.
M(Fe O )=2 56 +3 16 =160 г/моль
Ответ: m (Fe O ) = 8 г.
2
3
2
3

Задача № 6
- 3 моль фосфора соединяется с кислородом. Найти массу оксида?
Дано : Решение:
n (Р) =3 моль
m(P O ) - ?
2
5
4
P + O = P O
5
2
5
2
2
m
.
.
m = n M
n =
x
X =
M
=
2
.
.
M( P O )= 2 31 + 5 16 = 142г/моль
.
m ( P O ) = 1,5моль 142 г/моль = 213 г
Ответ: m( P O ) = 213 г

Задача № 7
- 10 л азота взаимодействует с водородом. Найти объем аммиака?
- Дано: Решение:
- V(N ) = 10 л
- V(N H ) = ?
- n =
Х моль
0,4моль
2
N + 3 H = 2 N H
2
2
3
1 моль
2моль
3
.
.
0,4
х
0,4 2
V
=
Х =
= 0,8 моль
.
V = n V
1
2
1
m
V
m
.
V(N H )=0,8 моль 22,4л/моль=18л
3
V = 22,4 л / моль
m
Ответ: V( N H )=18 л
3
10 л
= 0,4 моль
n =
22,4 л/моль

Задача № 8
- 10 г алюминия взаимодействуют с хлором. Найти объем хлора ?
- Дано: Решение:
- m(Al) = 10 г
- V(Cl ) = ?
Х моль
0,4 моль
2 Al + 3 Cl = 2 Al Cl
2
3
3 моль
2 моль
2
m
.
х
0,4 3
0,4
n =
0,6моль
Х =
=
=
.
V = n V
M
m
2
3
2
.
M(Al)=27 г/моль
V(Cl ) = 0,6моль 22,4 л/моль = 13 л
2
10 г
n(Al) =
0,4 моль
=
27 г/моль
Ответ: V (Cl ) = 13 л
2
V = 22,4 л/моль
m
 0,06 Na в избытке. Расчет по Br M(Na)= 23 г/моль 2 10 г 0,03 Х n(Na)= . = 0,4 моль Х = 0,03 2 = 0,06моль 23г/моль = 1 2 . M(Br ) = 2 80 =160 г/моль 2 m(NaBr) =0,06 моль . 103г/моль= 6 г 5 г n(Br )= = 0,03моль 2 160г/моль Ответ: m(NaBr) = 6 г M(NaBr)=23+80 = 103 г/моль " width="640"
0,06 Na в избытке. Расчет по Br M(Na)= 23 г/моль 2 10 г 0,03 Х n(Na)= . = 0,4 моль Х = 0,03 2 = 0,06моль 23г/моль = 1 2 . M(Br ) = 2 80 =160 г/моль 2 m(NaBr) =0,06 моль . 103г/моль= 6 г 5 г n(Br )= = 0,03моль 2 160г/моль Ответ: m(NaBr) = 6 г M(NaBr)=23+80 = 103 г/моль " width="640"
Расчет избытка одного из реагирующих веществ в химической реакции.
- 10 г натрия взаимодействуют с 5 г брома. Найти массу соли ?
- Дано: Решение:
- m(Na) =10 г
- m(Br ) =5 г
- m(NaBr ) = ?
y
0,4моль 0,03моль х моль
2 Na + Br = 2 NaBr
2
2
2моль 1моль 2моль
.
y 0,03
m
=
y = 2 0,03 = 0,06 моль
.
n =
m =n M
2 1
M
0,4 0,06 Na в избытке. Расчет по Br
M(Na)= 23 г/моль
2
10 г
0,03 Х
n(Na)=
.
= 0,4 моль
Х = 0,03 2 = 0,06моль
23г/моль
=
1 2
.
M(Br ) = 2 80 =160 г/моль
2
m(NaBr) =0,06 моль . 103г/моль= 6 г
5 г
n(Br )=
= 0,03моль
2
160г/моль
Ответ: m(NaBr) = 6 г
M(NaBr)=23+80 = 103 г/моль

Расчет массовой доли выхода продукта в результате химической реакции.
- Найти массовую долю выхода аммиака, который получили при взаимодействии 100г водорода с азотом, масса практического выхода его равна 500г.
- Дано: Решение:
- m(H ) = 100 г
- m(NH ) пр. = 500 г
- W(NH ) вых. = ?
50моль Х теор. моль
2
N + 3H = 2NH
3
2
2
3
3 моль 2моль
.
50 2
50 Хтеор.
=33моль
Хтеор.=
=
3
3 2
m
.
n =
m = n M
.
m (NH ) теор.= 33моль 17г/моль=561г
M
3
m( пр.)
M(H ) = 2 г/моль
.
2
W( вых.) =
100%
100г
m( теор.)
n(H )= = 50 г/моль
.
2
2г/моль
500г 100%
W(NH ) вых.=
=89%
M(NH )= 14 + 2 =17 г/моль
561г
3
3
Ответ: W(NH ) =89%
3

Расчет по химическим уравнениям, если реагирующие вещества имеют примеси.
- Найти массу оксида кальция, который получили в результате прокаливания 100г известняка с примесью 20 %.
- Дано: Решение:
- m( смеси) =100г
- W( прим.) = 20%= 0,2
- m(CaO) = ?
m( прим.)
W( прим.)=
m( смеси)
.
.
m( прим.)= W m( смеси)=0,2 100г=20 г
m(CaCO )= 100г- 20г = 80 г
3
m
0,8моль Хмоль
.
n =
m = n M
M
CaCO = CaO + CO
2
3
1 моль 1моль
M(CaCO )= 40+12+48=100 г/моль
3
80 г
=0,8моль
n(CaCO )=
=
Х =0,8 моль
3
100г/моль
1 1
.
m(CaO)= 0,8 моль 56г/моль=45 г
M(CaO) =40 +16 = 56 г/моль
Ответ: m(CaO) = 45 г

- 100 г 20% раствора соляной кислоты взаимодействуют с гидроксидом натрия. Найти массу гидроксида натрия.
- Дано: Решение :
m( р-ра) =100г
W(HCl) =20% = 0,2
m(NaOH) =?
.
.
m( в-ва)
m( в-ва)= W m( р-ра )
W =
;
m( р-ра)
.
m(HCl) =0,2 100 г =20г
0,5моль Хмоль
m
HCl + NaOH = NaCl + H O
.
n =
2
m = n M
M
1моль 1моль
M(HCl) =1 + 35,5 = 36,5 г/моль
0,5 Х
=
Х = 0,5 моль
1 1
20 г
.
n(HCl) =
= 0,5моль
36,5г/моль
m(NaOH) = 0,5моль 40г/моль= 20г
M(NaOH)=23 + 16 + 1 =40 г/моль
Ответ: m(NaOH) = 20 г

- II Расчет массовой доли элементов в химических соединениях.
- W =
m ( эл-та)
100%
.
M
W – массовая доля элемента (%)
m – масса элемента
M – молярная масса в-ва

Задача № 1
- Найти массовые доли элементов в азотной кислоте ?
- Дано: Решение:
- HNO
- W(H) =?
- W(N) =?
- W(O) =?
m( эл-та)
3
.
W( эл-та) =
1
100%
M(HNO )
3
1
.
w (H)=
100% = 1,6 %
63
14
.
.
W(N)=
100% =22,2 %
63
M (HNO )=1+14+ 48= 63 г/моль
3
H
O
N
48
.
W(O)=
100% =76,2 %
63

- III Расчет массовой доли компонентов смеси или раствора
- W =
m ( в-ва )
.
100 %
m ( смеси )
W – массовая доля вещества (% )
m – масса вещества
m – масса смеси или раствора

Задача № 1
- 10 г соли растворили в 100 г воды. Найти массовую долю соли в р-ре ?
- Дано: Решение:
10 г
m ( соли )
соли
.
W =
100 %
m ( р-ра )
.
10 г 100 %
W =
100г
=
9 %
H O
110 г
2
110 г р-ра w = ?
Ответ: w = 9 %

Задача № 2
- 10 г воды добавили к 100г 10 % р-ра. Найти W полученного р-ра ?
- Дано: Решение:
10г
m ( в-ва )
.
W =
m ( в-ва) = w m ( р-ра)
;
воды
m ( р-ра )
.
m( в-ва) в 100г 10%р-ра = 0,1 100г=10г
100г
10 % р-ра=0,1
10 г
.
W =
= 0,09 100% =9%
110г
110 г р-ра W = ?
Ответ: w = 9%

Задача № 3
- 10 г в-ва растворили в 100 г 10 % р-ра. Найти W полученного р-ра ?
- Дано: Решение:
m( в-ва)
10г
.
W =
m( в-ва)= W m( р-ра)
;
m( р-ра)
в-ва
.
m( в-ва) в 100г 10%р-ра=0,1 100г=10г
m( в-ва) в 110г W %р-ра=10г+10г=20г
10% р-ра=0,1
100 г
20 г
.
=0,18 100% =18%
W =
110 г р-ра W = ?
110г
Ответ: W= 18%
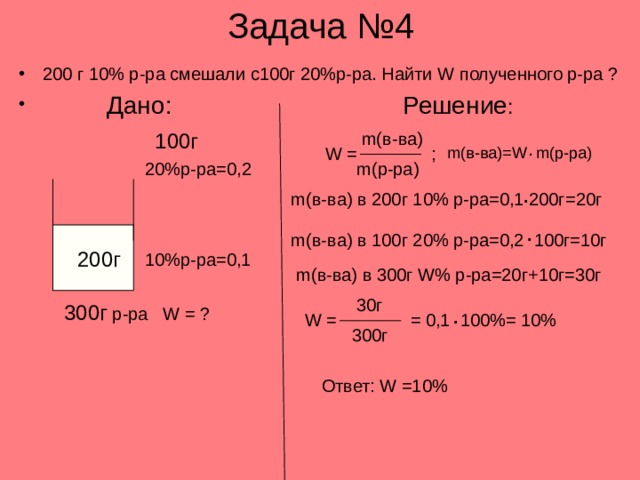
Задача №4
- 200 г 10% р-ра смешали с100г 20%р-ра. Найти W полученного р-ра ?
- Дано: Решение :
m( в-ва)
100г
.
;
W =
m( в-ва)= W m( р-ра)
m( р-ра)
20%р-ра=0,2
.
m( в-ва) в 200г 10% р-ра=0,1 200г=20г
.
200г
m( в-ва) в 100г 20% р-ра=0,2 100г=10г
10%р-ра=0,1
m( в-ва) в 300г W% р-ра=20г+10г=30г
30г
300г р-ра W = ?
.
W =
=
0,1 100%= 10%
300г
Ответ: W =10%

Вывод химических формул.
- Углеводород содержит 92,3% углерода и 7,7% водорода. Плотность паров его по водороду равна 39. Определить формулу углеводорода?
- Дано: Решение :
- W(C) =92,3%
- W(H) =7,7%
- Д =39
М( C H )
x
у
.
;
M(C H )= Д M(H )
Д =
2
H
x у
H
2
2
М (H )
2
.
M(C H ) = 39 2 г/моль= 78г/моль
H
2
х у
W(C) W(H)
C H = ?
92,3 7,7
x
у
:
=
Х : У =
=
:
12 1
Ar(C) Ar(H)
M(H ) = 2 г/моль A r (C) = 12 A r (H) =1
2
7,7 7,7
:
= 1 : 1
=7,7 : 7,7 =
7,7 7,7
Простейшая формула – CH M(CH) =12 + 1 = 13 г/моль
M(C H ) M(CH)
78 г/моль 13г/моль
х у
=
= 6
Формула углеводорода C H
6 6

- При сжигании 8,6г углеводорода получили 26,4г CO и 12,6г H O . Найти молекулярную формулу углеводорода, если его плотность по воздуху равна 2,91.
- Дано: Решение:
- m(CO ) = 26,4 г
- m(H O) =12,6 г
- Д(возд.) =2,97
C H = ?
М(возд.) = 29 г/моль
M(CO ) = 12+32 =44 г/моль
M(H O) =2 + 16 =18 г/моль Ar(C) = 12 Ar(H) = 1
Простейшая формула - СН
2
2
М( C H )
х у
.
2
Д(возд.) =
; C H = Д(возд.) М(возд.)
х у
M (возд.)
2
.
М( C H ) = 2,9 1 29 = 8 4г/моль
х у
m(C H ) = 8,6 г
.
х у
26,4 12
44г(СО ) - 12г(С) 26,4г(СО ) - Хг (С)
2
Х(С)=
= 7,2г
;
х у
44
2
.
18г(Н О) - 2г (Н) 12,6г(Н О) – Хг(Н)
12,6 2
2
2
= 1,4г
;
Х(Н)=
18
2
2
m(C H ) = 7,2 г + 1,4г = 8,6г
х у
7,2 1,4
m(C) m(H)
:
:
=
=0,6 : 1,4=
Х : У =
2
12 1
Ar(C) Ar(H)
0,6 1,4
M(CH ) =12 + 2 = 14 г/моль
2
M(C H )
;
х у
84
:
=
= 1 : 2
= 6
=
0,6 0,6
M(CH )
2
14
Формула углеводорода – C H
6 12

 Получите свидетельство
Получите свидетельство Вход
Вход











 Решение задач по химии (1.09 MB)
Решение задач по химии (1.09 MB)
 0
0 2002
2002 91
91 Нравится
0
Нравится
0








