Цель: продолжить изучение по теме «Строение и свойства вещества». Познакомиться с определениями молекула, атом, элемент.
Организационный момент.
Приветствие.
Здравствуйте, ребята! Как ваше настроение?
Кто отсутствует на уроке? Все готовы к уроку?
Актуализация опорных знаний учащихся
Мы продолжаем рассматривать большую тему «Строение и свойства вещества». Сегодня нам предстоит познакомиться с молекулами, атомами, элементами, но для начала давайте повторим то, что мы с вами уже изучили.
Повторение. Фронтальный опрос.
Что такое тело?
Что мы называем веществом?
В каких состояниях может находится вещество?
Жидкое, газообразное, твердое. (Агрегатное состояние вещества)
Приведите пример вещества, которое мы чаще всего встречаем в трех состояниях?
Любое тело, например вода, воздух.
Назовите свойства, которыми обладают твердые тела, жидкости, газы. (Слайд)
В твёрдом состоянии вещество сохраняет как форму, так и объём.
В жидком состоянии вещество сохраняет объём, но не сохраняет форму.
Газообразное состояние характерно тем, что оно не сохраняет ни форму, ни объём. Газ заполняет всё доступное пространство и проникает в любые его закоулки. Это состояние, свойственное веществам с малой плотностью.
Какой вклад в науку внес Ломоносов?. (Слайд)
Карточки «Тело – Вещество»
Дети называют вещество из которого это тело состоит.
Например: Стол – дерево. Мяч – резина. Ваза – глина…
Перед вами табличка. Соедините стрелочками тело и вещество из которого оно состоит.
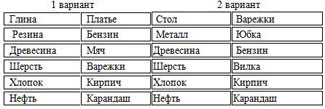
Взаимопроверка. Поменяйтесь с соседом. Проверяем. Поставьте оценку.
Формирование новых умений и навыков.
Мы с вами узнали, что тела состоят из веществ.
А из чего состоят вещества, как вы думаете? (Слайд)
Давайте посмотрим опыт. В наполненный до краев стакан с водой, мы осторожно всыпаем в воду соль. Помещается примерно 1 ложечка. Почему? И мы видим соль растворилась, поменялся цвет. Это опыт и многие другие наблюдения, о которых вы узнаете позже, позволяет сделать вывод, что вещества из которых образованы тела не сплошные, а состоят из частиц. Частицы соли разместились между частицами воды в нашем опыте.
Частицы, невидимые человеческому невооруженному глазу, из которых состоят все вещества называются молекулы. Записываем в тетрадь.
Молекулы – мельчайшие частицы вещества, сохраняющая его свойства.
Но есть современные приборы - электронные микроскопы, которые позволяют увидеть и сфотографировать наиболее крупные молекулы.
Давайте посмотрим «Портрет» молекулы: стр 50. Прочитайте.
Молекула - наименьшая частица вещества;
Молекулы одного и того же вещества одинаковые;
Размеры молекул очень малы;
Между молекулами есть промежутки;
Молекулы находятся в постоянном движении.
Физкультминутка. Все встали. Ильнар показывает упражнения. Все повторяют.
Мы сказали, что молекулы можно увидеть. Как вы думаете, а можно ли разделить молекулу?
Оказывается можно, хотя молекулы маленькие частицы вещества, их можно делить.
Частицы, на которые делится молекула, называли атомами( в переводе с греч. Атмос - неделимый). Ещё 2500 лет назад древнегреческий философ - Демокри́т, высказал мысль о том, что все тела в природе состоят из мельчайших невидимых, непроницаемых, неделимых, вечно движущихся частиц – атомов.
Конечно позже учёные доказали, что и атом делим. Он настолько мал, что ни в один микроскоп увидеть его не удаётся.
И так мы узнали, что молекулы состоят из атомов Например молекула воды состоит из одного атома кислорода и двух атомов водорода,
У вас на стр. 50 рис. 31 показана молекула воды, условно атомы изображают в виде шариков разного цвета, и разного размера. показать макет, попробовать сделать самим.
А давайте мы с вами попробуем сделать молекулы из атомов.
Молекула кислорода состоит из 2 - х атомов кислорода. В составе молекулы могут входить не только 2 - 3 атома, а несколько десятков разнообразных атомов.
Конечно, количество атомов на Земле огромно. Но разнообразие их ограничено - сейчас известно 109 видов различных атомов. Они в разных сочетаниях друг с другом образуют все вещества окружающего нас мира - живого и неживого.
Определенный вид атома это химический элемент. Записываем в тетрадь. Например водород обозначается латинской буквой Н, железо - Fe, рис. 32. и т. д.
Все химические элементы собраны в таблицу. Создал ее Д. И. Менделеев.
Весь материал – смотрите документ.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Разработка урока по природоведению на тему:"Молекулы. Атомы. Элементы" (85.5 КB)
Разработка урока по природоведению на тему:"Молекулы. Атомы. Элементы" (85.5 КB)
 0
0 1384
1384 292
292 Нравится
0
Нравится
0


