
Окислительно-восстановительные реакции
Химия
8 класс
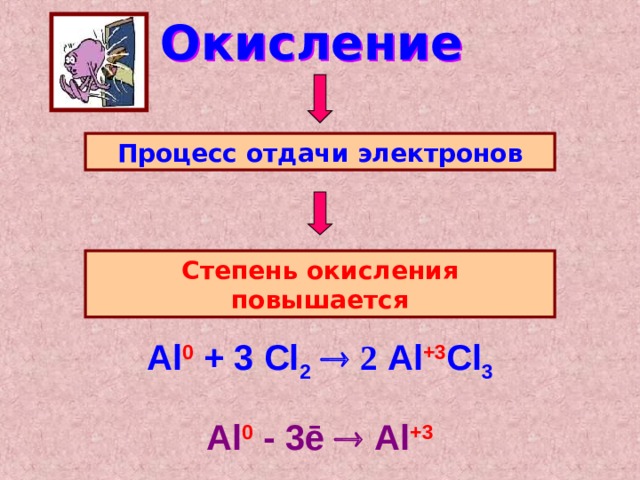
Окисление
Процесс отдачи электронов
Степень окисления повышается
Al 0 + 3 Cl 2 2 Al +3 Cl 3
Al 0 - 3ē Al +3
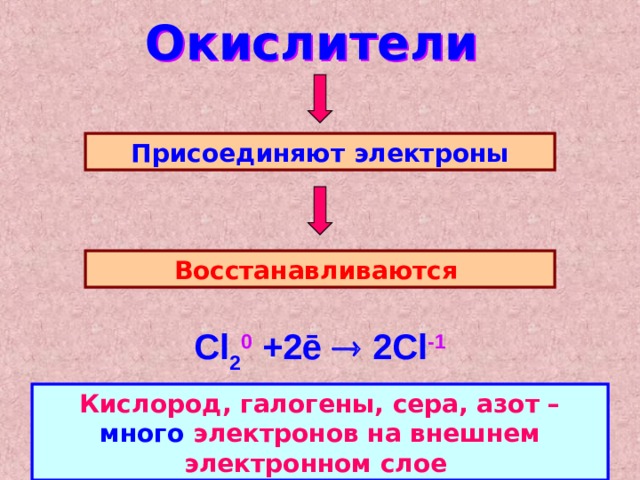
Окислители
Присоединяют электроны
Восстанавливаются
Cl 2 0 +2ē 2Cl - 1
Кислород, галогены, сера, азот – много электронов на внешнем электронном слое
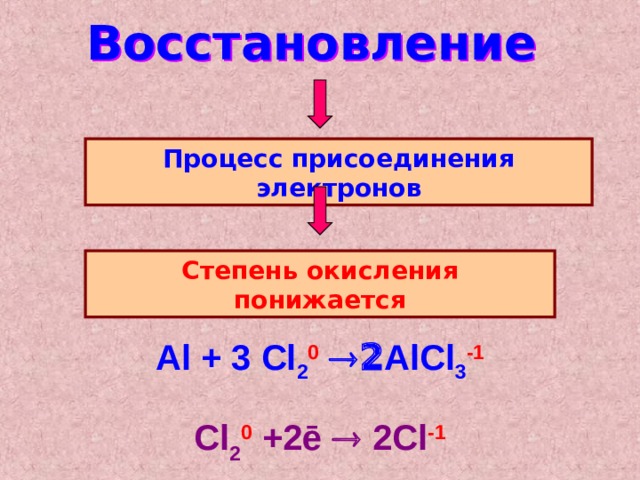
Восстановление
Процесс присоединения электронов
Степень окисления понижается
Al + 3 Cl 2 0 AlCl 3 -1
Cl 2 0 +2ē 2Cl - 1
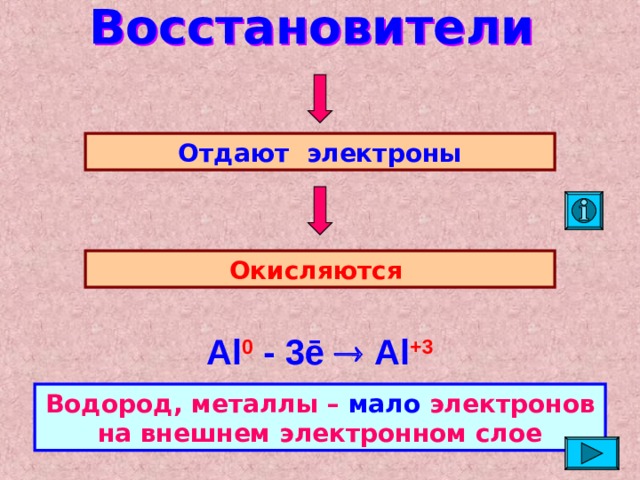
Восстановители
Отдают электроны
Окисляются
Al 0 - 3ē Al +3
Водород, металлы – мало электронов на внешнем электронном слое

ОВР – окислительно-восстановительные реакции
Реакции, в которых происходит изменение степени окисления элементов
Zn 0 + 2H +1 Cl Zn +2 Cl 2 + H 2 0
Восстановитель, окисляется, окисление
Zn 0 – 2е Zn + 2
2 H +1 + 2е H 2 0
Окислитель, восстанавливается, восстановление

Окислитель восстанавливается , его степень окисления уменьшается
Восстановитель окисляется , его степень окисления увеличивается
2 Na 0 + Cl 2 0 = 2 Na +1 Cl -1
Na 0 – 1 е = Na +1
Восстановитель, окисляется, окисление
Окислитель, восстанавливается, восстановление
Cl 2 0 +2е = 2 Cl -1
Положительный
Восстановился

Упражнения
В данных реакциях определите окислитель и восстановитель
1. NH 3 + O 2 = NO + H 2 O
2. CuO + H 2 = Cu + H 2 O
3. P + N 2 O = N 2 + P 2 O 5
4. Na + H 2 O = H 2 + NaOH
5. CuSO 4 + Fe = FeSO 4 + Cu
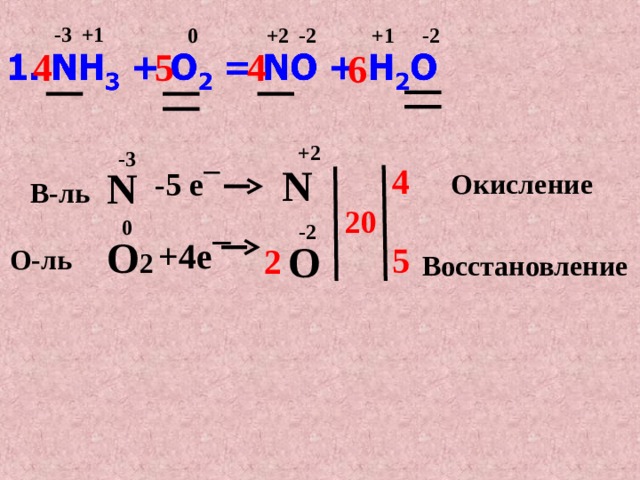
-3
+1
+1
-2
+2
-2
0
4
5
4
6
+2
-3
4
N
N
-5 e¯
Окисление
В-ль
20
0
-2
O 2
+4е¯
O
5
2
О-ль
Восстановление
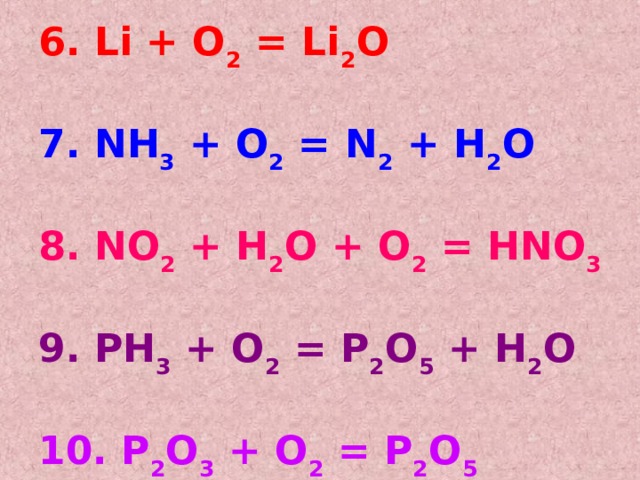
6. Li + O 2 = Li 2 O
7. NH 3 + O 2 = N 2 + H 2 O
8. NO 2 + H 2 O + O 2 = HNO 3
9. PH 3 + O 2 = P 2 O 5 + H 2 O
10. P 2 O 3 + O 2 = P 2 O 5

 Получите свидетельство
Получите свидетельство Вход
Вход












 Презентация "Окислительно-восстановительные реакции" (368 KB)
Презентация "Окислительно-восстановительные реакции" (368 KB)
 0
0 1476
1476 175
175 Нравится
0
Нравится
0


