
Предмет органической химии
Что изучает органическая химия. Понятие об углеводородах
Ключевой вопрос Каковы особенности органических веществ? Чем они отличаются от неорганических?
Органическая химия изучает органические вещества, их состав, строение, свойства и применение.
В настоящее время известно более 20 млн органических соединений, причем ежегодно эта цифра значительно увеличивается. В то же время неорганических веществ известно порядка нескольких сотен тысяч. Что же объединяет все органические вещества?
Почему они столь многочисленны? Очевидно, вы вспомнили: во всех органических веществах есть углерод !
Задание с открытым ответом
Проблемный вопрос
Почему именное углерод – центральный элемент органической химии? Почему ни один другой элемент в природе не может дать такого огромного количества соединений. Выскажите своё предположение.

«Углерод встречается в природе как в свободном состоянии, так и в соединительном состоянии, в весьма различных формах и видах… Способность атомов углерода соединяться между собой и давать сложные частицы проявляется во всех углеродистых соединениях… Ни в одном из элементов…способности к усложнению не развито такой степени, как в углероде… Ни одна пара элементов не дает столь много соединений, как углерод с водородом»
Д.И.Менделеев , учебник «Основы химии» Д.И. Менделеева

История развития органической химии
- IX – X вв. - разделение всех органических веществ по их происхождению на три царства: минеральные, растительные и животные вещества.
- Начало XIX в. – объединение химии веществ растительного и животного происхождения в единую науку.
- 1808г. – науке, изучающей органические вещества, дано название - органическая химия.

История развития органической химии
- - возникновение ложного учения ВИТАЛИЗМА, приверженцы которого считали, что синтез органических соединений из неорганических вне живых организмов невозможен.
- 1828г. – осуществлен синтез органического соединения мочевины из неорганического вещества цианата аммония. (крах витализма)
- 1854г. – получен жир в пробирке.
- 1861г. - осуществлен синтез сахаристого вещества .
Берцелиус Йёнс Якоб (1779 – 1848)
предложил науку изучающую органические вещества называть органической химией. С 1808 года ведет отсчет органическая химия.
Научные исследования Берцелиуса охватывают все главные проблемы общей химии первой половины XIX в. Он экспериментально проверил и доказал достоверность законов постоянства состава и кратных отношений применительно к неорганическим и органическим соединениям. Одним из важнейших достижений Берцелиуса стало создание системы атомных масс химических элементов. Берцелиус определил состав более чем двух тысяч соединений и рассчитал атомные массы 45 химических элементов . Берцелиус также ввёл современные обозначения химических элементов и первые формулы химических соединений.
Берцелиус пользовался огромным авторитетом у химиков-современников. В 1808 г. он стал членом шведской Королевской Академии наук, в 1810-1818 гг. был её президентом.
Шведский химик. Родился в селении Веверсунде на юге Швеции. Берцелиус рано потерял родителей
и уже во время обучения в гимназии зарабатывал частными уроками, тем не менее получил медицинское образование в Упсальском университете в 1797-1801 гг.
В 1807 г. Берцелиус был избран на должность профессора химии и фармации в Медико-хирургическом институте Стокгольма.
Фридрих Вёлер (1800-1882)
Вёлера с ранних лет привлекала химия. Еще студентом-первокурсником в химической лаборатории университета он приготовил цианид йода ICN при взаимодействии сухого цианида калия с йодом. Хирургом он не стал, а упросил шведского химика Берцелиуса дать ему возможность поработать лаборантом под его руководством.
Вёлер первым получил в чистом виде очень многие вещества: алюминий, аморфный бор, бериллий, иттрий, карбид кремния SiC и карбид кальция CaC2, силан SiH4 и трихлорсилан SiHCl3. Он предложил новый способ получения белого фосфора P4 нагреванием смеси ортофосфата кальция Ca3(PO4)2, угля и песка (диоксида кремния) SiO2. Этот способ до сих пор применяют в промышленности почти во всех странах мира.
Но самым знаменитым синтезом Вёлера стало получение карбамида (NH2)2CO (мочевины) при упаривании раствора цианата аммония NH4NCO (1828г.) - органического вещества из неорганического.
Немецкий химик.
Родился в городе Эшерхейме недалеко от Франкфурта-на-Майне в семье именитого бюргера. По настоянию родителей он окончил медицинский факультет Марбургского университета и в 1823 году получил звание доктора медицины - хирурга.

Пьер-Эжен-Марселен БЕРТЛО (Berthelot) (25.10.1827- 18.3.1907)
Профессор химии , член Парижской АН (1873 г.) , член-корреспондент Петербургской АН (1876 г.).
Бертло синтезировал огромное число органических соединений, относящихся к различным классам. Взаимодействием глицерина и жирных кислот Бертло получил (1853- 1854 гг.) аналоги природных жиров и таким образом доказал возможность их синтеза. Попутно он установил, что глицерин - трёхатомный спирт. Принципиальное значение имел синтез этилового спирта гидратированием этилена в присутствии серной кислоты (1854 г.); до этого этиловый спирт получали только брожением сахаристых веществ.
Другим направлением работ Бертло были синтезы многих простейших углеводородов - метана, этилена, ацетилена, бензола, а затем на их основе - более сложных соединений.
Французский химик. Родился в Париже в семье врача. Вначале изучал медицину, но под влиянием лекций Т.Пелуза и Ж.Дюма решил посвятить себя химии.

Бутлеров Александр Михайлович
(03.09.1828г. - 05.08.1886г.)
В 1851 г. защитил магистерскую диссертацию «Об окислении органических соединений», а в 1854 г. – докторскую диссертацию «Об эфирных маслах».
Открыв (1858 г.) новый способ синтеза иодистого метилена, выполнил серию работ, связанных с получением его производных. Синтезировал диацетат метилена, получил продукт его омыления - полимер формальдегида, а на основе последнего впервые получил (1861 г.) гексаметилентетрамин (уротропин) и сахаристое вещество "метиленитан", то есть осуществил первый полный синтез сахаристого вещества.
По свидетельству современников, Бутлеров был одним из лучших лекторов своего времени: он безраздельно владел аудиторией благодаря ясности и строгости изложения, которые сочетались у него с образностью языка.
Русский химик. Родился в Чистополе Казанской губернии в семье помещика, офицера в отставке. В первые годы студенчества увлекался ботаникой и зоологией, но затем под влиянием лекций К. К. Клауса и Н. Н. Зинина заинтересовался химией и решил посвятить себя этой науке.
Однако, вы знаете примеры и неорганических веществ, в которых содержатся атомы углерода – это карбонаты, гидрокарбонаты, карбиды, оксиды углерода и др.
Специфическая природа органических веществ подчеркивается в определении органической химии, которое в 70-х годах XIX в. дал немецкий ученый К. Шоллермер :
Органическая химия – это химия углеводородов и их производных.
Углеводороды – это соединения углерода с водородом.
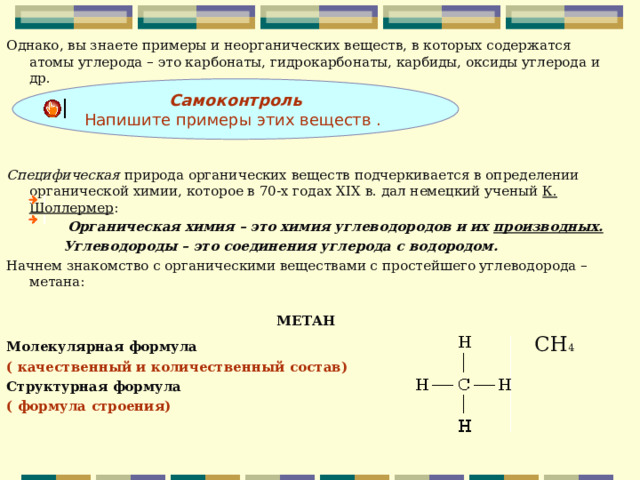
Начнем знакомство с органическими веществами с простейшего углеводорода – метана:
МЕТАН
Молекулярная формула СН 4
( качественный и количественный состав)
Структурная формула
( формула строения)
Самоконтроль
Напишите примеры этих веществ .
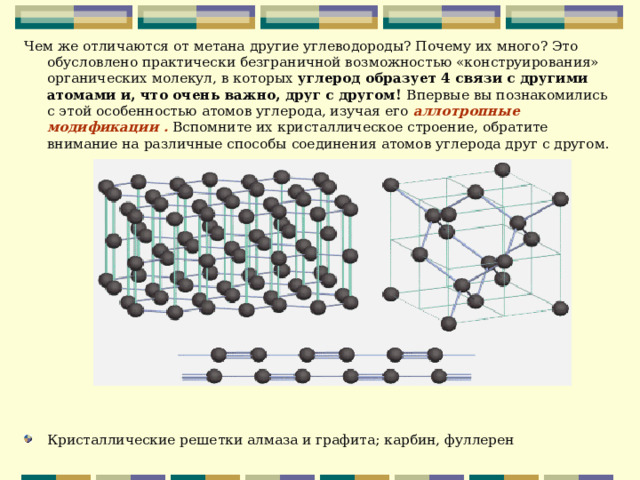
Чем же отличаются от метана другие углеводороды? Почему их много? Это обусловлено практически безграничной возможностью «конструирования» органических молекул, в которых углерод образует 4 связи с другими атомами и, что очень важно, друг с другом! Впервые вы познакомились с этой особенностью атомов углерода, изучая его аллотропные модификации . Вспомните их кристаллическое строение, обратите внимание на различные способы соединения атомов углерода друг с другом.
- Кристаллические решетки алмаза и графита; карбин, фуллерен
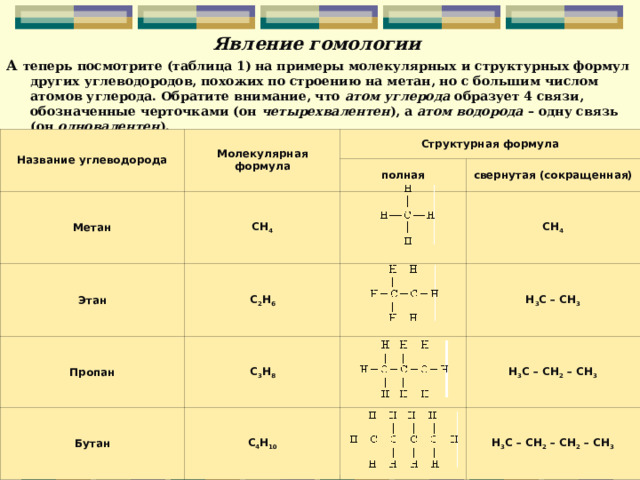
Явление гомологии
А теперь посмотрите (таблица 1) на примеры молекулярных и структурных формул других углеводородов, похожих по строению на метан, но с большим числом атомов углерода. Обратите внимание, что атом углерода образует 4 связи, обозначенные черточками (он четырехвалентен ), а атом водорода – одну связь (он одновалентен ).
Название углеводорода
Молекулярная формула
Структурная формула
Метан
СН 4
полная
Этан
С 2 Н 6
свернутая (сокращенная)
Пропан
С 3 Н 8
СН 4
Бутан
С 4 Н 10
Н 3 С – СН 3
Н 3 С – СН 2 – СН 3
Н 3 С – СН 2 – СН 2 – СН 3

Метан, этан, пропан, бутан называют гомологами (от греч. homologos – подобный).
- Гомологи – это органические вещества, сходные по строению, но отличающиеся по составу на одну или несколько групп –СН 2 –. СН 2 – гомологическая разность
Рис. 1. Гомологи
- Гомологи имеют сходные химические свойства и более или менее закономерно изменяющиеся физические свойства, что облегчает изучение огромного количества органических соединений. Явление гомологии было обнаружено французским химиком Ш. Жераром в XIX в.
Посмотрите на рис. 1 и ответьте на вопрос: Что вам напоминают эти конструкции из кубиков? Попробуйте собрать из оставшихся кубиков еще одну конструкцию, продолжающую начатый ряд.

Явление изомерии
В органической химии существует еще одно интересное явление – изомерия . В 30-е годы XIX в. шведский ученый Й. Я. Берцелиус назвал изомерами вещества, имеющие одинаковый состав, но разные свойства. Позднее, благодаря трудам великого русского химика А.М. Бутлерова, было установлено, что изомеры имеют разный порядок соединения атомов, т.е. разное строение.
Изомеры – это вещества, имеющие одинаковый состав молекул (молекулярную формулу) и разное строение, а потому и разные свойства.
Изомеры (греч. isos – равный, meros - часть)
Изомеры состава С 4 Н 10
Бутан
Н 3 С ─ СН 2 ─ СН 2 ─ СН 3
Ткип. = - 0,5С
Изобутан
Ткип. = - 11,7С

Самоконтроль
Сравните 2 ключевых понятия органической химии, заполнив таблицу 2.
Гомологи и изомеры
Таблица 2.
Тест «Гомологи и изомеры»
Для пентана СН 3 ─ СН 2 ─ СН 2 ─ СН 2 ─ СН 3 среди перечисленных ниже предложенных веществ найдите:
1) Формулу гомолога
2) Формулу изомера
Понятия
Гомологи
Состав
Строение
Изомеры
Свойства
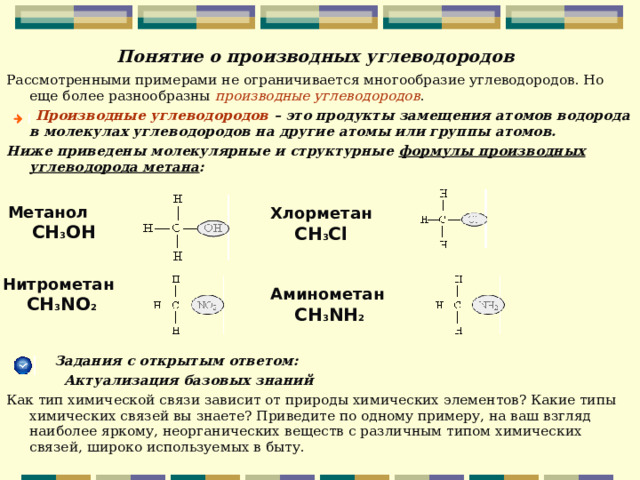
Понятие о производных углеводородов
Рассмотренными примерами не ограничивается многообразие углеводородов. Но еще более разнообразны производные углеводородов .
Производные углеводородов – это продукты замещения атомов водорода в молекулах углеводородов на другие атомы или группы атомов.
Ниже приведены молекулярные и структурные формулы производных углеводорода метана :
Задания с открытым ответом:
Актуализация базовых знаний
Как тип химической связи зависит от природы химических элементов? Какие типы химических связей вы знаете? Приведите по одному примеру, на ваш взгляд наиболее яркому, неорганических веществ с различным типом химических связей, широко используемых в быту.
Метанол СН 3 ОН
Хлорметан СН 3 Cl
Нитрометан CH 3 NO 2
Аминометан СН 3 NH 2

Органические вещества – вещества молекулярного строения
Органические вещества в большинстве своем образованы атомами неметаллов – это, конечно, углерод С, водород Н, а также азот N, кислород О, галогены и др. Поэтому предметом изучения в органической химии являются преимущественно вещества с ковалентным типом химических связей и молекулярного строения
В связи с этим, типичные органические вещества – это чаще всего
жидкости или твердые вещества со сравнительно низкими
температурами кипения и плавления, неэлектрлиты, многие
не растворимы или плохо растворимы в воде.
Рис. 1. Модель кристаллической решетки метана СН4

Роль органических веществ в нашей жизни
Молекулы органических веществ играют исключительную роль в нашей жизни.
В настоящее время органическая химия – это развивающаяся отрасль химической науки и производства.
Рис.2. Современные материалы и продукты на основе органических веществ. 1-пластмассы (синтетические), 2-лекарственные средства, 3-средства для борьбы с насекомыми, 4-моющие средства, 5,6-искусственные волокна и ткани, 7-целлулоид (искусственная пластмасса), 8-краски, эмали, 9-фотопленка, 10-клеи, 11-бездымный порох, 12-синтетические волокна и ткани, 13-синтетические каучуки, 14-удобрения.
В любом организме протекает множество превращений одних органических веществ в другие. Без знания органической химии невозможно понять, как осуществляется функционирование систем, образующих живой организм. Т.е. органическая химия служит фундаментом для многих наук, изучающих живую природу, в частности для молекулярной биологии, биохимии, фармакологии, медицины.

Некоторые особенности превращений органических веществ
Важной составной частью органической химии, как и химии вообще, является изучение общих закономерностей, определяющих химические свойства веществ, направление их реакций.
Но многие органические соединения имеют очень сложный состав, строение, огромную молекулярную массу ( например, белки, углеводы, нуклеиновые кислоты), поэтому для них характерны и некоторые особенности в химическом поведении: обычно органические вещества менее стойки, особенно термически, легко окисляются, многие горючи, а в результате горения образуют углекислый газ и воду ( т. к. содержат атомы углерода и водорода) и др.

 Получите свидетельство
Получите свидетельство Вход
Вход











 Предмет органическая химия (1.77 MB)
Предмет органическая химия (1.77 MB)
 0
0 770
770 6
6 Нравится
0
Нравится
0



