
Практическая работа №5
«Экспериментальное решение задач по теме «Неметаллы» 9 класс ФГОС-3

Оборудование:
- пробирки, штатив химический, спиртовка,спички, держатель для пробирок.

Реактивы:.
- согласно методичке

Цель работы:
- научиться 1.распознавать вещества С ПОМОЩЬЮ КАЧЕСТВЕННЫХ РЕАКЦИЙ 2. проводить экспериментальные доказательства данных веществ.

инструктаж по правилам техники безопасности
- 1. работа с кислотами, щелочами, солями
- 2. работа с пузырьками и капельницами
- 3. работа со спиртовкой
- 4. нагревание веществ
- 5. организация рабочего места

Инструктаж по ТБ правильно организуй своё рабочее место!

ПРАВИЛА ВЫЖИВАНИЯ = ЗДРАВЫЙ СМЫСЛ + ТБ
- ЕСЛИ НЕ УСВОИЛИ ЭТИХ ПРАВИЛ, НЕ ВХОДИТЕ В ЛАБОРАТОРИЮ.

общий объём жидкости д.б. не более 2 мл

Правила нагревания
- 1. закрепить пробирку в держателе.
- 2. прогреть всю пробирку 3 раза в пламени
- 3. медленно, не допуская бурного кипения, прогревать пробирку с водой в верхней части пламени.
- 4. отверстие пробирки д.б. направлено в ту сторону, где никого нет!
- 5. нельзя:
- греть пробирку на границе жидкость- воздух!
- касаться холодным фитилём раскалённого дна пробирки!
- допускать бурное кипение жидкости!

Приемы нагревания

Ход работы
- вариант№ 1 вариант № 2
- Задачи № 4 и № 1 № 6 и № 2
- вариант № 3 вариант № 4
- Задачи № 8 и № 1 № 6 и № 2

Таблица (на 2 страницы)
№ з
А
Формулы и названия исходных веществ
д
Наблюдения признакиов химических реакций
…
Уравнения химических реакций
Вы
вод

Инструктаж по работе
- эталон должен остаться чистым
2. сделать пробы для работы
3. Таблица чертится на 2 страницы

№
Формулы и названия исходных веществ
1
н 2SO 4 - серная кислота
Наблюдения признаков химических реакций
Лакмус
Уравнения химических реакций
При добавлении к кислоте лакмуса, он меняет свой цвет с фиолетового на красный при ….
вывод
ВаСl2 – хлорид бария
Пишем в трёх видах:
Молекулярном
Доказали наличие ионов Н +
Полном ионном
Кратком ионном

Формулы и названия исходных веществ
н 2SO 4- серная кислота
Наблюдения признаков химических реакций
Уравнения химических реакций
Zn- Ц инк
При добавлении к кислоте цинка наблюдаем выделение газа без цвета,без запаха, без вкуса – это водород
ОВР
вывод

Задача №4
реактив
лакмус
а)НCl
BaCl 2
красный
б)Н2SO4
красный
-
в)Na OH
Ход определения
- Сделать пробы
- Прилить лакмус
- Из 2х оставшихся пробирок снова сделать пробы
- Прилить BaCl2
№ пробирки
ВаSO4↓ белый мучнист
синий
-
К
А
С
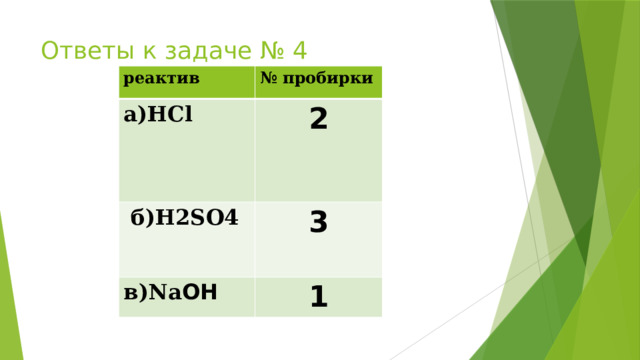
Ответы к задаче № 4
реактив
№ пробирки
а)НCl
2
б)Н2SO4
3
в)Na OH
1
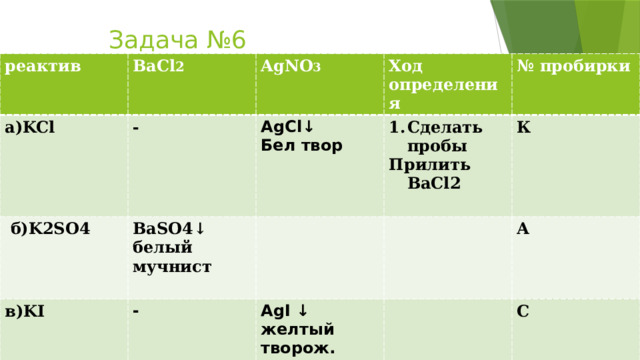
Задача №6
реактив
BaCl 2
а)KCl
б)K2SO4
AgNO 3
-
Ход определения
в)KI
AgCl↓
ВаSO4↓ белый мучнист
-
- Сделать пробы
Бел твор
№ пробирки
К
AgI ↓ желтый творож.
Прилить BaCl2
А
С
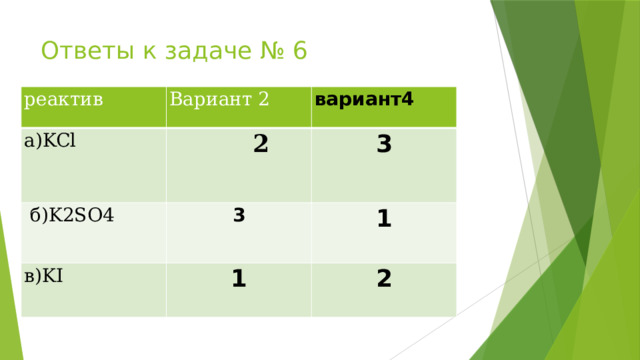
Ответы к задаче № 6
реактив
Вариант 2
а)KCl
вариант4
2
б)K2SO4
3
3
в)KI
1
1
2
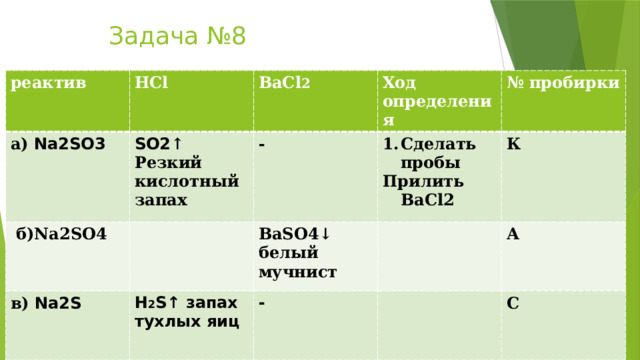
Задача №8
реактив
HCl
а) Na2SO3
б)Na2SO4
BaCl 2
SO2 ↑
Ход определения
Резкий кислотный запах
-
в) Na2S
H 2 S↑ запах тухлых яиц
ВаSO4↓ белый мучнист
- Сделать пробы
№ пробирки
К
Прилить BaCl2
-
А
С

Ответы к задаче № 8
реактив
№ пробирки
а) Na2SO3
3
б)Na2SO4
1
в) Na2S
2

Инструкция по окончанию работы
- 1. Приведи в порядок рабочее место:
- Расположи оборудование и реактивы так, как они располагались до начала работы
- Вытри пролитое, собери просыпанное
- Закрой плотно спиртовку во избежание испарения спирта из неё
- Закрой все пробки на флаконах с реактивами и поставь их в должном порядке
- Вымой тщательно пробирки
- 2. Собери мусор и выбрось его в контейнер с мусором в коридоре.
- 3. Сдай штатив физический в вытяжной шкаф
- 4. Лоток с оборудованием поставь на полку в стенке согласно маркировке
- 5. Пропуск вложи в тетрадь, а тетрадь вложи в тетрадь соседа и сдайте учителю

внимание
- Не соблюдение правил ТБ приводит к: несчастью
- Снижению оценки за практическое выполнение работы на балл

СПАСИБО ЗА РАБОТУ
СОГЛАСНО ПРАВИЛАМ ТЕХНИКИ БЕЗОПАСНОСТИ!
О.А.

 Получите свидетельство
Получите свидетельство Вход
Вход












 Практическая работа Экспериментальное решение задач по теме " Неметаллы" (503.51 KB)
Практическая работа Экспериментальное решение задач по теме " Неметаллы" (503.51 KB)
 0
0 42
42 0
0 Нравится
0
Нравится
0


