Гетероциклические соединения
Гетероциклические соединения содержат в цикле не только атомы углерода, но и атомы других элементов (N, O, S).
Гетероциклические соединения входят в состав многих природных веществ (хлорофилл, нуклеиновые кислоты, витамины, алкалоиды, пенициллин). Более половины лекарственных веществ содержат в структуре гетероциклы.
Классификация и номенклатура
Гетероциклические соединения могут быть насыщенными, ненасыщенными, в том числе ароматическими. Чаще встречаются ненасыщенные. Названия, как правило, тривиальные, принятые ИЮПАК.
4
3
тиофен
фуран
1

2
5
4
3



S
1
2
5
4
3



5
N1
H
2



пиррол
Пятичленные гетероциклы с двумя гетероатомами.
3
N
3
N
тиазол
S
1
2
5
4



N1
H
2
5
4



имидазол
пиразол
N1
H
2
5
4
3



Шестичленные гетероциклы с одним и двумя гетероатомами.
4
3 N
4
N
5
3
5
4
4
5
3
3
5

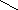

![]()
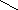

![]()
![]()
2N
N
1
2
N
1
N
1
N
1
6
2
6
6
2

![]()






пиразин
пиримидин
пиридазин
пиридин
Конденсированные системы гетероциклов
H
N
3
4



![]()




![]()




![]()


N
индол
(бензопиррол)
пурин
хинолин
2
7
6
5

N
N1
H

N
N
Нумерация начинается от гетероатома.
В гетероциклах с одним гетероатомом атомы углерода иногда обозначаются через …буквы (пиррол, пиридин) В гетероциклах с несколькими равноценными гетероатомами нумеруют так, чтобы гетероатомы получили наименьшие номера (пиримидин). Если имеются два атома азота с различным электронным строением (N= и NH), то нумеруют от NH (пиразол). В гетероциклах с различными гетероатомами старшим считается кислород, далее сера, затем азот.
Названия производных гетероциклов строятся по общим правилам.
COOH
4


![]()
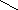
пиридин-4-карбоновая кислота
3
N1
![]()

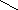

\
СН3
2-метилпиридин
2
N
Ароматичность
Наибольшее значение представляют ароматические гетероциклические соединения, которые имеют электронное строение, подобное бензолу.
Пиридин – шестичленный гетероцикл с одним атомом азота. Все атомы углерода и азот находятся в состоянии sp2-гибридизации, но одна гибридная орбиталь азота содержит неподеленную пару электронов. Такой атом азота называется пиридиновым.
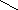

![]()

N
Пиррол – пятичленный гетероцикл с одним атомом азота. Все атомы также находятся в состоянии sp2-гибридизации. Но атом азота имеет иное электронное строение. Неподеленная пара электронов находится на негибридной р-орбитали. Она принимает участие в сопряжении с р-электронами четырех атомов с образованием единого шестиэлектронного облака, а три гибридных sp2-орбитали образуют три -связи. Такой атом N называется пиррольным. Примерами ароматических гетероциклов с двумя гетероатомами является:
имидазол, пиразол (по одному N- пирольного типа, по одному N – пиридинового типа), пиримидин (имеет 2N пиридинового типа).
Кислотно – основные свойства
![]()

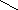
 Основные свойства – имеет пиридиновый атом N, способный присоединять протон (Н+).
Основные свойства – имеет пиридиновый атом N, способный присоединять протон (Н+).
N
![]()

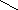
 + HBr
+ HBr
Br -
пиридиний бромид
N+
H
пиридин
Кислотные свойства – имеет пиррольный атом азота.







гидролиз


 + Na + NaOH
+ Na + NaOH
N
H
N-
N+
N
H
НОН
(протекает легко)
-H2
пиррол
пиррол натрий
Амфотерные свойства
Гетероциклы, содержащие атомы азота пиридинового и пиррольного типа, проявляют основные и кислотные свойства.
N :






N
H
N+H
пиразол
+ HBr Br -
N
H
пиразолнитробромид






N
N
+ Na
N
H
N
Na
-H2
пиразолнатрий


 Получите свидетельство
Получите свидетельство Вход
Вход


















 Материал по химии по теме "Гетероциклические соединения" (26.02 КB)
Материал по химии по теме "Гетероциклические соединения" (26.02 КB)
 0
0 858
858 73
73 Нравится
0
Нравится
0



