Учитель химии: Түктібаева А.Қ.
Дата:_______________________
План урока по химии для 11классa
Тема урока:
Ненасыщенные углеводороды. Алкены: гомологический ряд и общая формула, строение молекулы этилена и других алкенов, номенклатура и изомерия.
1. Цель урока: изучить гомологический ряд, строение молекулы алкенов, номенклатуру и изомерию.
2. Задачи
2.1 Образовательные – познакомить учащихся с гомологическим рядом алкенов, рассмотреть особенности их химического и электронного строения, изомерию и номенклатуру. Развить полученные ранее теоретические представления об изомерии и умения давать названия соединений по систематической номенклатуре. Рассмотреть промышленные и лабораторные способы получения алкенов, развить общие представления о типах и механизмах химических реакций на примере алкенов. Показать место и значение алкенов среди углеводородов.
2.2 Воспитательные – продолжить формирование естественнонаучной картины мира, а также общеучебных навыков: внимания, эстетики оформления записей лекционного материала, умения наблюдать, формулировать выводы и обобщать информацию.
2.3 Развивающие – развить умение учащихся на основе теоретических знаний сравнивать, анализировать, обобщать, логически рассуждать, устанавливать взаимосвязь строения и свойств веществ, умения составлять уравнения химических реакций с участием непредельных углеводородов.
Тип урока
Урок формирования и совершенствования знаний.
Методы обучения – словесные, наглядные.
4. Средства обучения:
мультимедийный проектор
компьютер
шаростержневые модели
Ход урока
Организационный этап с актуализацией изучаемой на уроке темы
Учитель: Здравствуйте, ребята! Садитесь, пожалуйста, на свои места и мы начнём наш урок, который, я надеюсь, будет для вас продуктивным, а главное - полезным!
Этап повторения и совершенствования знаний.
Учитель: Новый материал запоминается легче, если он называется на уже полученные знания. Поэтому сейчас предстоит работа с извлечением этого материала из памяти.
Какие углеводороды относят к алканам?
Запишите формулы возможных изомеров гексана и назовите их по систематической номенклатуре.
Напишите формулы возможных продуктов крекинга октана.
Каковы природные источники получения алканов?
Назовите области применения алканов
Мы с вами провели проверочную работу по теме: "Алканы", а теперь познакомимся с другой группой органических веществ.
У меня на столе шаростержневые модели двух веществ. Сравните их между собой, найдите сходства и отличия.
Этот углеводород относится к непредельным углеводородам класса "Алкенов", изучению которого мы и посвящаем наш урок.
На экране проектора высвечивается тема урока "Алкены» (Слайд №2)
Учитель: Алкены – ненасыщенные углеводороды с общей формулой СnH2n , в молекулах которых имеется одна двойная связь.
Простейший представителем алкенов является этилен С2Н4. Поскольку гомологический ряд алкенов начинается с этилена, их и называют углеводородами ряда этилена. Раньше этиленовые углеводороды (алкены – по систематической номенклатуре ИЮПАК) называли также олефинами.
Название составляют аналогично алканам с заменой суффикса -ан на -ен и указанием после него локанта двойной связи. Например:
|
|
|
|
| 3-трет-бутил-7-метилоктен-2 | 4,5-диметил-3-пропилгексен-1 | 2,3,5-триметилгексен-3 |
| За основу выбрана самая длинная цепь, содержащая двойную связь. Нумерация начинается с того края, к которому ближе расположена двойная связь. | За основу выбрана самая длинная и самая разветвленная цепь, содержащая двойную связь. | Двойная связь расположена симметрично. Направление нумерации определяют минимальные локанты заместителей (2,3,5 при нумерации слева меньше, чем 2,4,5 при нумерации справа). |
Радикалы алкенов называются аналогично радикалам алканов: СН2=СН – этенил(винил).
Строение алкенов.
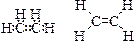
В молекуле алкена ненасыщенные атомы углерода находятся в sp2-гибридизации, а двойная связь между ними образована σ– и π-связью. sp2-Гибридные орбитали направлены друг к другу под углом 120°, и одна негибридизованная 2р-орбиталь, расположена под углом 90° к плоскости гибридных атомных орбиталей.
Пространственное строение этилена:
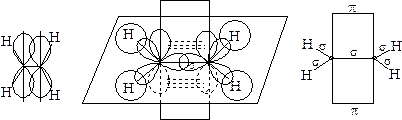
Длина связи С=С 0,134 нм, энергия связи С=С Ес=с = 611 кДж/моль, энергия π-связи Еπ = 260 кДж/моль.
Для алкенов характерно несколько видов изомерии.
1. У алкенов, как и у алканов, изомерия обусловлена строением углеродного скелета. Например, изомеры бутена (С4Н8):
![]() 2-метилпропен-1
2-метилпропен-1
СН2=СН-СН2 - СН3 бутен-1
2. Изомерия, связанная с положением двойной связи.
В зависимости от положения двойной связи молекула бутена имеет два изомера. Двойная связь может находиться у концевого углерода или у срединного атома углерода:
СН2=СН-СН2 - СН3 бутен-1
СН3 - СН=СНСН3 бутен-2
3. Межклассовая изомерия. Общая формула алкенов и циклоалканов одинакова CnH2n. Согласно межклассовой изомерии, изомеры бутена С4Н8 – циклобутан и метилциклопропан:

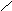
 СН2
СН2
Н2С СН-СН3
4. Пространственная изомерия (цис и транс).Геометрическая изомерия
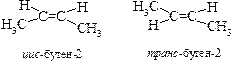
Если одинаковые заместители СН3 в изомере находятся по одну сторону плоскости двойной связи, то образуется цис – изомер, если находятся по разные стороны-транс –изомер.
Эти изомеры обладают различными физическими и химическими свойствами. Транс-изомер является более устойчивым, чем цис-изомер.
Учитель:В чём заключается особенность строения молекул алкенов? (ответ: в наличии двойной связи)
Мы знаем, что от строения вещества зависят его свойства и применение. Какова активность алкенов по сравнению с алканами, «органическими мертвецами»? Почему? (ответ:алкены наиболее химически активны из-за наличия непрочной π-связи)
Этап закрепления пройденного материала
Учитель:
Как классифицируются ненасыщенные углеводороды? (алкены, алкадиены,алкины).
Какой тип гибридизации атома углерода характерен для алкенов? (SP2 )
Этап подведения итогов урока. «РЕФЛЕКСИЯ»
Составить синквейн по теме. Посмотрите на слайд и вспомните, как надо правильно составить его.
Пример:
1ТЕМА Алкены
2 ПРИЛАГАТЕЛЬНЫХ Непредельные, ненасыщенные
3 ГЛАГОЛА Присоединяют, горят, полимеризуются
4 ЗНАЧЕНИЕ Широко используются в промышленности
5 Углеводороды
Ребята, сегодня на уроке вы хорошо поработали. Выскажите ваши впечатления об уроке, что понравилось, а что можно было бы изменить, (учащиеся высказывают свое мнение об уроке).
Домашнее задание по теме «Алкены».
Сегодня вы все молодцы, хорошо поработали на уроке,
Учитель: А теперь пришло время немного отдохнуть и записать домашнее задание.
Учащиеся: записывают домашнее задание
стр. 78, табл.7; §2.6, упр. 6-9, стр. 83-84
Спасибо за урок!

 Получите свидетельство
Получите свидетельство Вход
Вход



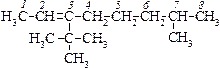
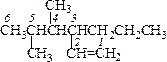
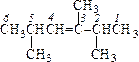









 Конспект урока на тему: "Ненасыщенные углеводороды. Алкены: гомологический ряд и общая формула, строение молекулы этилена и других алкенов, номенклатура и изомерия." (95.85 KB)
Конспект урока на тему: "Ненасыщенные углеводороды. Алкены: гомологический ряд и общая формула, строение молекулы этилена и других алкенов, номенклатура и изомерия." (95.85 KB)
 0
0 2535
2535 245
245 Нравится
0
Нравится
0


